Водород пероксид
 Ball stick model of the hydrogen peroxide molecule
| |||
| |||
Назив според МСЧПХ Водород пероксид | |||
Други називи Диоксидан | |||
| Назнаки | |||
|---|---|---|---|
| 7722-84-1 | |||
| ChEBI | CHEBI:16240 | ||
| ChEMBL | ChEMBL71595 | ||
| ChemSpider | 763 | ||
| EC-број | 231-765-0 | ||
| |||
| 2448 | |||
| 3Д-модел (Jmol) | Слика | ||
| KEGG | D00008 | ||
| PubChem | 784 | ||
| RTECS-бр. | MX0900000 (>90% soln.) MX0887000 (>30% soln.) | ||
| |||
| UNII | BBX060AN9V | ||
| ОН-бр. | 2015 (>60% soln.) 2014 (20–60% soln.) 2984 (8–20% soln.) | ||
| Својства | |||
| Хемиска формула | |||
| Моларна маса | 0 g mol−1 | ||
| Изглед | Светло сина течност | ||
| Мирис | малку остар | ||
| Густина | 1.11 g/cm3 (20 °C, 30% (w/w) solution)[1] 1.450 g/cm3 (20 °C, pure) | ||
| Точка на топење | |||
| Точка на вриење | |||
| Мешлив | |||
| Растворливост | растворлив во диетил етер, етанол нерастворлив во петрол етер | ||
| log P | -0.43[2] | ||
| Парен притисок | 5 mmHg (30 °C)[3] | ||
| Киселост (pKa) | 11.75 | ||
| −17.7·10−6 cm3/mol | |||
| Показател на прекршување (nD) | 1.4061 | ||
| Вискозност | 1.245 cP (20 °C) | ||
| Диполен момент | 2.26 D | ||
| Термохемија | |||
| Ст. енталпија на формирање ΔfH |
−187.80 kJ/mol | ||
| Специфичен топлински капацитет, C | 1.267 J/(g·K) (gas) 2.619 J/(g·K) (liquid) | ||
| Pharmacology | |||
| ATC код | A01AB02 D08, D11, S02 | ||
| Опасност | |||
| GHS-ознаки: | |||
Пиктограми
|
  
| ||
Сигнални зборови
|
Опасност | ||
Изјави за опасност
|
H271, H302, H314, H332, H335, H412 | ||
Изјави за претпазливост
|
P280, P305+P351+P338, P310 | ||
| NFPA 704 | |||
| Температура на запалување | {{{value}}} | ||
| Смртоносна доза или концентрација: | |||
LD50 (средна доза)
|
1518 mg/kg[се бара извор] 2000 mg/kg (орално, глушец)[4] | ||
LC50 (средна концентрација)
|
1418 ppm (стаорец, 4 ч)[4] | ||
LCLo (најниска објавена)
|
227 ppm (глушец)[4] | ||
| NIOSH (здравствени граници во САД): | |||
PEL (дозволива)
|
TWA 1 ppm (1.4 mg/m3)[3] | ||
REL (препорачана)
|
TWA 1 ppm (1.4 mg/m3)[3] | ||
IDLH (непосредна опасност)
|
75 ppm[3] | ||
| Безбедносен лист | ICSC 0164 (>60% soln.) | ||
| Дополнителни податоци | |||
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |||
| Наводи | |||
Водород пероксид е хемиско соединение со формула H
2O
2. Во својата чиста форма, таа е многу бледо сина[5] течност која е малку повеќе вискозна од водата. Се користи како оксиданс, средство за белење и антисептик, обично како разреден раствор (3 % – 6 % масен удел) во вода за потрошувачки употреби и во повисоки концентрации за индустриска употреба. Концентрираниот водороден пероксид, или „пероксид со висок тест“, експлозивно се распаѓа кога се загрева и се користи како погонско гориво во ракетирањето.[6]
Водород пероксид е реактивен вид на кислород и наједноставниот пероксид, соединение кое има единечна кислород-кислород врска. Полека се распаѓа кога е изложен на светлина и брзо во присуство на органски или реактивни соединенија. Обично се чува со стабилизатор во слабо кисел раствор во темно шише за да се блокира светлината. Водород пероксид се наоѓа во биолошките системи вклучувајќи го и човечкото тело. Ензимите кои користат или разградуваат водороден пероксид се класифицирани како пероксидази.
Својства[уреди | уреди извор]
Точката на вриење на H
2O
2 е екстраполирана како 150,2 °C (302,4 °F), приближно 50 °C (90 °F) повисока од водата. Во пракса, водород пероксид ќе претрпи потенцијално експлозивно термичко распаѓање ако се загрее до оваа температура. Може безбедно да се дестилира на пониски температури под намален притисок.[7]
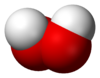
Структура[уреди | уреди извор]
Водород пероксид (H
2O
2) е нерамна молекула со (извиткана) C2 симетрија; ова првпат го покажа Пол-Антоан Гигуер во 1950 година со помош на инфрацрвена спектроскопија. Иако врската O−O е единечна врска, молекулата има релативно висока ротациона бариера од 386 cm−1 (4,62 kJ/mol) за ротација помеѓу енантиомери преку trans конфигурацијата и 2460 cm−1 (29,4 kJ/mol) преку cis конфигурацијата.[8] Овие бариери се должат на одбивноста помеѓу слободните електронски парови на соседните атоми на кислород и диполните ефекти помеѓу двете O-H врски. За споредба, ротационата бариера за етанот е 1040 cm−1 (12,4 kJ/mol).
Приближно 100° е диедралниот агол помеѓу двете O-H врски и ја прави молекулата хирална. Тоа е најмалата и наједноставната молекула која покажува енантиомеризам. Предложено е дека енантиоспецифичните интеракции на едниот наместо на другиот може да доведат до засилување на една енантиомерна форма на рибонуклеински киселини и затоа е потеклото на хомохиралност во светот на РНК.[9]
Молекуларните структури на гасовит и кристален H
2O
2 се значително различни. Оваа разлика се припишува на ефектите на водородната врска, која е отсутна во гасовита состојба.[10] Кристалите на H
2O
2 се тетрагонални со просторната група D4
4 или P41212.[11]
Водни раствори[уреди | уреди извор]
Во водени раствори, водородниот пероксид се разликува од чистата супстанција поради ефектите на водородното поврзување помеѓу молекулите на водата и водород пероксидот. Водород пероксид и вода формираат еутектичка мешавина, покажувајќи депресија на точката на замрзнување до -56 °C; чистата вода има точка на замрзнување од 0 °C и чист водороден пероксид од -0,43 °C. Точката на вриење на истите мешавини е исто така намалена во однос на средната вредност на двете точки на вриење (125,1 °C). Се јавува на 114 °C. Оваа точка на вриење е 14 °C поголема од онаа на чистата вода и 36,2 °C помала од онаа на чистиот водороден пероксид.[12]

2O
2 и вода: Областа над сината линија е течна. Испрекинатите линии ги одделуваат цврсто-течните фази од цврсто-цврстите фази.
| H 2O 2 (w/w) |
Густина (g/cm3) |
Тем. (°C) |
|---|---|---|
| 3% | 1.0095 | 15 |
| 27% | 1.10 | 20 |
| 35% | 1.13 | 20 |
| 50% | 1.20 | 20 |
| 70% | 1.29 | 20 |
| 75% | 1.33 | 20 |
| 96% | 1.42 | 20 |
| 98% | 1.43 | 20 |
| 100% | 1.45 | 20 |
Споредба со аналози[уреди | уреди извор]
Водород пероксид има неколку структурни аналози со H
mX–XH
n сврзувачки аранжмани (водата е прикажана и за споредба). Има највисока (теоретска) точка на вриење од оваа серија (X = O, S, N, P). Неговата точка на топење е исто така прилично висока, споредлива со онаа на хидразинот и водата, при што само хидроксиламинот се кристализира значително полесно, што укажува на особено силна водородна врска. Дифосфан и водород дисулфид покажуваат само слаби водородни врски и имаат мала хемиска сличност со водород пероксид. Структурно, сите аналози усвојуваат слични искривени структури, поради одбивноста помеѓу соседните слободни електронски парови.
| Име | Формула | Моларна
маса |
Точка на
топење (°C) !! Точка на вирење (°C) | |
|---|---|---|---|---|
| Вода | HOH | 18.02 | 0.00 | 99.98 |
| Водород пероксид | HOOH | 34.01 | −0.43 | 150.2* |
| Водород дисулфид | HSSH | 66.15 | −89.6 | 70.7 |
| Хидразин | H2NNH2 | 32.05 | 2 | 114 |
| Хидроксиламин | NH2OH | 33.03 | 33 | 58* |
| Дифосфан | H2PPH2 | 65.98 | −99 | 63.5* |
Откритие[уреди | уреди извор]
Понекогаш се вели дека Александар фон Хумболт бил првиот што го пријавил првиот синтетички пероксид, бариум пероксид, во 1799 година како нуспроизвод на неговите обиди да го разложи воздухот, иако тоа е оспорено поради двосмислената формулација на фон Хумболт.[13] Деветнаесет години подоцна Луј Жак Тенар препознал дека ова соединение може да се користи за подготовка на претходно непознато соединение, кое го опишал како eau oxygénée („оксигенирана вода“) – подоцна познато како водороден пероксид.[14][15][16] Денес, терминот „оксигенирана вода“ може да се појави на малопродажното пакување што се однесува на мешавини што содржат или вода и водороден пероксид или вода и растворен кислород. Ова може да предизвика лична повреда ако разликата не е правилно разбрана од корисникот.[17]
Подобрената верзија на процесот на Тенард користела хлороводородна киселина, проследена со додавање на сулфурна киселина за да се таложи нуспроизводот на бариум сулфат. Овој процес се користел од крајот на 19 век до средината на 20 век.[18]
Ефектот на белење на пероксидите и нивните соли на природните бои беше познат уште од експериментите на Тенард во 1820-тите, но раните обиди за индустриско производство на пероксиди не успеаја. Првата фабрика за производство на водород пероксид била изградена во 1873 година во Берлин. Откривањето на синтезата на водород пероксид со електролиза со сулфурна киселина го воведе поефикасниот електрохемиски метод. За прв пат беше комерцијализиран во 1908 година во Вајсенштајн, Корушка, Австрија. Процесот на антрахинон, кој сè уште се користи, беше развиен во текот на 1930-тите од германскиот хемиски производител IG Farben во Лудвигсхафен. Зголемената побарувачка и подобрувањата во методите на синтеза резултираа со пораст на годишното производство на водород пероксид од 35.000 тони во 1950 година, на над 100.000 тони во 1960 година, на 300.000 тони до 1970 година; до 1998 година достигна 2,7 милиони тони.[19]
Раните обиди не успеаја да произведат уреден водороден пероксид. Безводниот водороден пероксид најпрво бил добиен со вакуум дестилација.[20]
Одредувањето на молекуларната структура на водород пероксид се покажа како многу тешко. Во 1892 година, италијанскиот физико-хемичар Џакомо Карара (1864–1925) ја одредил неговата молекуларна маса со депресија на точката на замрзнување, што потврдило дека неговата молекуларна формула е H
2O
2.[21] Се чинеше дека H
2O=O е исто толку возможна како модерната структура и дури во средината на 20 век, најмалку половина дузина хипотетички изомерни варијанти на две главни опции се чинеше дека се во согласност со достапните докази.[22] Во 1934 година, англискиот математички физичар Вилијам Пени и шкотскиот физичар Гордон Сатерленд предложија молекуларна структура за водород пероксид која беше многу слична на моментално прифатената.[23][24]
Претходно, водород пероксид се подготвуваше индустриски со хидролиза на амониум персулфат:
кој самиот бил добиен со електролиза на раствор од амониум бисулфат ([NH
4]HSO
4) во сулфурна киселина:[25]
Производство[уреди | уреди извор]

Денес, водород пероксидот се произведува речиси исклучиво со процесот на антрахинон, кој првично беше развиен од BASF во 1939 година. Започнува со редукција на антрахинон (како 2-етилантрахинон или 2-амил дериват) до соодветниот антрахидрохинон, обично со хидрогенирање на паладиумски катализатор. Во присуство на кислород, антрахидрохинонот потоа се подложува на автооксидација: лабилните водородни атоми на хидрокси групите се пренесуваат во молекулата на кислородот, за да се добие водороден пероксид и да се регенерира антрахинонот. Повеќето комерцијални процеси постигнуваат оксидација со клокотот на компримиран воздух низ раствор на антрахидрохинон, при што водородниот пероксид потоа се екстрахира од растворот и антрахинонот се рециклира назад за последователни циклуси на хидрогениеање и оксидациј..[26][27]
Нето реакцијата за процесот катализиран од антрахинон е :[26]
- H
2 + O
2 → H
2O
2
Економичноста на процесот во голема мера зависи од ефективното рециклирање на растворувачите за екстракција, катализаторот за хидрогенизација и скапиот хинон.


Други извори[уреди | уреди извор]
Мали, но забележливи количини на водород пероксид може да се формираат со неколку методи. Мали количества се формираат со електролиза на разредена киселина околу катодата каде што водородот еволуира околу меурчињата на кислородот кој се додаваат околу неа. Исто така, се произведува со изложување на вода на ултравиолетови зраци од живина ламба или електричен лак додека ја затворате во проѕирен УВ сад (на пример, кварц). Тој е забележлив во ледена вода по согорување на проток на водороден гас насочен кон неа, а може да се забележи и на лебдечки мраз. Брзо ладениот влажен воздух продуван низ јазот на искри од приближно 2.000 °C резултира во забележливи количини.[28]
Комерцијално остварлив процес за производство на водород пероксид директно од околината е од интерес многу години. Ефикасна директна синтеза е тешко да се постигне, бидејќи реакцијата на водородот со кислородот термодинамички го фаворизира производството на вода. Развиени се системи за директна синтеза, од кои повеќето користат фино дисперзирани метални катализатори слични на оние што се користат за хидрогенирање на органски супстрати.[29][30] Една економска пречка беше тоа што директните процеси даваат разредено решение неекономично за транспорт. Ниту еден од нив сè уште не достигнал точка каде што може да се користи за синтеза во индустриски размери.
Достапност[уреди | уреди извор]
Водород пероксид најчесто е достапен како раствор во вода. За потрошувачите, обично е достапен во аптеките во концентрации од 3 и 6 wt%. Концентрациите понекогаш се опишуваат во однос на волуменот на генерираниот гас на кислород; еден милилитар раствор од 20 волумени генерира дваесет милилитри кислороден гас кога целосно ќе се распадне. За лабораториска употреба, најчести се растворите од 30 wt%. Достапни се и комерцијални концентрации на растворот од 70 % до 98 %, но поради потенцијалот растворите од повеќе од 68 % водород пероксид целосно да се претворат во водена пареа и кислород (со зголемување на температурата на пареата како што концентрацијата се зголемува над 68 %) овие концентрации на растворите се потенцијално многу поопасни и бараат посебна грижа во посебни места за складирање. Купувачите обично мора да дозволат инспекција од страна на комерцијалните производители.
Во 1994 година, светското производство набеше околу 1,9 милиони тони и порасна на 2,2 милиони во 2006 година,[31] од кои повеќето беа во концентрација од 70 % или помалку. Во таа година, најголемиот дел од 30 % H
2O
2 се продаваше за околу 0,54 USD/kg, што е еквивалентно на US$1.50/kg (US$0.68/lb) на "100 % основа".[26]
Природна појава[уреди | уреди извор]
Водород пероксид се јавува во површинските води, во подземните води и во атмосферата. Се формира при осветлување или природно каталитичко дејство од супстанции содржани во водата. Морската вода содржи од 0,5 до 14 μg/L водород пероксид, а слатката вода содржи од 1 до 30 μg/L.[19] Концентрациите во воздухот се околу 0,4 до 4 μg/m3, кои варираат во неколку реда на величина во зависност од условите како што се сезоната, надморска височина, дневна светлина и содржина на водена пареа. Во руралниот ноќен воздух тој е помал од 0,014 μg/m3, а кај умерен фотохемиски смог е од 14 до 42 μg/m3.[32]
Реакции[уреди | уреди извор]
Распаѓање[уреди | уреди извор]
Водород пероксид се распаѓа за да формира вода и кислород со ΔHo од –2884.5 kJ/kg[33] и ΔS од 70.5 J/(mol·K):
Стапката на распаѓање се зголемува со порастот на температурата, концентрацијата и pH вредноста (H
2O
2 е нестабилен во алкални услови), при што студените, разредените и киселите раствори покажуваат најдобра стабилност. Распаѓањето се катализира од различни редокс-активни јони или соединенија, вклучувајќи ги повеќето преодни метали и нивните соединенија (на пример, манган диоксид (MnO
2), сребро и платина).[34] Одредени метални јони, како што се Fe2+ или Ti3+, Одредени метални јони, може да предизвика разградувањето да заземе поинаков пат, така што да дојди до формирање на слободни радикали како што се хидроксил радикал (HO•
) и хидропероксил (HOO•
). Неметалните катализатори вклучуваат калиум јодид (KI), кој реагира особено брзо и ја формира основата на демонстративниот експеримент наречен слонова паста за заби. Водород пероксид, исто така, може да се разложи биолошки од ензимот каталаза. Распаѓањето на водород пероксид ослободува кислород и топлина; ова може да биде опасно, бидејќи истурањето на водород пероксид со висока концентрација на запалива материја може да предизвика моментален пожар.
Редокс реакции[уреди | уреди извор]
Редокс својствата на водород пероксид зависат од pH вредноста бидејќи киселите услови ја влошуваат моќта на оксидирачките агенси, а базните услови ја влошуваат моќта на редукционите агенси. Бидејќи водородниот пероксид покажува амбивалентни редокс својства, истовремено и оксидатор или редуктор, неговото редокс однесување веднаш зависи од pH вредноста.
Во киселите раствори, H
2O
2 е моќен оксидатор, посилен од хлорот, хлор диоксидот и калиум перманганат. Кога се користи за чистење на лабораториски стакларија, растворот од водород пероксид и сулфурна киселина се нарекува Пирана раствор.
H
2O
2 е извор на хидроксилни радикали (•
OH), кои се многу реактивни.
| Оксидирачки
реактант |
Редуциран
продукт |
Оксидирачки
потенцијал (V) |
|---|---|---|
| F 2 |
HF | 3.0 |
| O 3 |
O 2 |
2.1 |
| H 2O 2 |
H 2O |
1.8 |
| KMnO 4 |
MnO 2 |
1.7 |
| ClO 2 |
HClO | 1.5 |
| Cl 2 |
Cl− |
1.4 |
Во киселите раствори, Fe2+ се оксидира до Fe3+ (водороден пероксид делува како оксидирачки агенс):
и сулфит (SO2−
3) се оксидира до сулфат (SO2−
4). Сепак, калиум перманганат се редуцира до Mn2+ со кисел H
2O
2.
Во алкални услови, сепак, некои од овие реакции се менуваат; на пример, Mn2+се оксидира до Mn4+ (како MnO
2).
Во базните раствори, водород пероксидот е силен редуктор и може да редуцира различни неоргански јони. Кога H
2O
2 делува како редукционо средство, се произведува и кислороден гас. На пример, водород пероксид ќе го редуцира натриум хипохлорит и калиум перманганат, што е пригоден метод за подготовка на кислород во лабораторија:
Органски реакции[уреди | уреди извор]
Водород пероксид често се користи како оксидирачки агенс. Илустративно е оксидацијата на тиоетерите во сулфоксиди:[36][37]
Алкалниот водороден пероксид се користи за епоксидација на алкени со дефицит на електрони како што се дериватите на акрилна киселина,[38] и за оксидација на алкилборани во алкохоли, вториот чекор на хидроборација-оксидација. Исто така, тој е главниот реагенс во процесот на Дакин оксидација.
Преткурсор на други пероксид соединенија[уреди | уреди извор]
Водород пероксид е слаба киселина, која формира хидропероксид или пероксидни соли со многу метали.
Исто така, ги претвора металните оксиди во соодветните пероксиди. На пример, при третман со водород пероксид, хромна киселина (CrO
3 и H
2SO
4) формира син пероксид CrO(O
2)
2.
Овој вид на реакција се користи индустриски за производство на пероксоаниони. На пример, реакцијата со боракс води до натриум перборат, белило што се користи во детергентите за перење:
H
2O
2 и конвертира карбоксилните киселини (RCO
2H) во перокси киселини (RC(O)O
2H), кои самите се користат како оксидирачки агенси. Водород пероксид реагира со ацетон за да формира ацетон пероксид и со озон за да формира триоксидан. Водород пероксид формира стабилни адукти со уреа (Хидроген пероксид - уреа), натриум карбонат (натриум перкарбонат) и други соединенија.[39] Киселинско-базен додаток со трифенилфосфин оксид е корисен „носител“ за H
2O
2 во некои реакции.
Водород пероксид е и оксидирачки и редуцирачки агенс. Оксидацијата на водород пероксид со натриум хипохлорит дава синглет кислород. Нето реакцијата на фери јон со водород пероксид е феро јон и кислород. Ова се одвива преку оксидација на еден електрон и хидроксилни радикали. Ова се користи во некои оксидации во органска хемија, на пр. во Фентоновиот реагенс. Потребни се само каталитички количества железен јон бидејќи пероксидот исто така оксидира феро јон во фери јон. Нето реакцијата на водород пероксид и перманганат или манган диоксид е манган јон; сепак, додека не се потроши пероксидот, некои јони на манган се реоксидираат за да се направи реакцијата каталитичка. Ова ја формира основата за обичните ракети со монопропелант.
Биолошка функција[уреди | уреди извор]

Водород пероксид се формира кај луѓето и другите животни како краткотраен производ во биохемиските процеси и е токсичен за клетките. Токсичноста се должи на оксидација на белковините, мембранските липиди и ДНК од пероксидните јони.[40] Класата на биолошки ензими наречена супероксид дисмутаза (SOD) е развиена во скоро сите живи клетки како важен антиоксиданс. Тие промовираат диспропорција на супероксид во кислород и водород пероксид, кој потоа брзо се разградува од ензимот каталаза до кислород и вода.[41]
Пероксизомите се органели кои се наоѓаат практично во сите еукариотски клетки.[42] Тие се вклучени во катаболизмот на масни киселини со многу долг ланец, масни киселини со разгранет ланец, D-аминокиселини, полиамини и биосинтеза на плазмалогени, етер фосфолипиди кои се клучни за нормалната функција на мозокот и белите дробови на цицачите.[43] По оксидација, тие произведуваат водороден пероксид во следниот процес катализиран од флавин аденин динуклеотид (FAD):[44]
Каталаза, друг пероксизомален ензим, го користи овој H
2O
2 за оксидација на други супстрати, вклучувајќи феноли, мравја киселина, формалдехид и алкохол, со помош на реакција на пероксидација:
со што се елиминира отровниот водороден пероксид во процесот.
Оваа реакција е важна во клетките на црниот дроб и бубрезите, каде што пероксизомите ги неутрализираат различните токсични материи кои влегуваат во крвта. Некои од етанолот што го пијат луѓето се оксидираат во ацеталдехид на овој начин.[45] Покрај тоа, кога вишокот H
2O
2 се акумулира во клетката, каталазата ја претвора во H
2O преку оваа реакција:
Друго потекло на водород пероксид е разградувањето на аденозин монофосфат кој дава хипоксантин. Хипоксантинот потоа оксидативно се катаболизира прво во ксантин, а потоа во мочна киселина, а реакцијата се катализира од ензимот ксантин оксидаза:[46]

Со разградувањето на гванозин монофосфат се добива ксантин како меѓупроизвод кој потоа на ист начин се претвора во мочна киселина со формирање на водороден пероксид.[46]
Јајцата од морски еж, кратко време по оплодувањето со сперма, произведуваат водород пероксид. Потоа брзо се дисоцира на HO• радикали. Радикалите служат како иницијатор на радикалната полимеризација, која ги опкружува јајцата со заштитен слој од полимер.[47]
Бомбардер бумбарот има уред кој ѝ овозможува да пука со меурчиња со корозивни и непријатни мириси кон своите непријатели. Бубачката произведува и складира хидрохинон и водород пероксид, во два посебни резервоари на задниот врв на абдоменот. Кога е загрозена, бубачката ги собира мускулите кои ги принудуваат двата реактанта низ цевки со вентили во комората за мешање што содржи вода и мешавина од каталитички ензими. Кога ќе се спојат, реактантите се подложени на насилна егзотермна хемиска реакција, зголемувајќи ја температурата до точката на вриење на водата. Течноста што врие, со непријатен мирис делумно станува гас (испарување со блиц) и се исфрла преку излезниот вентил со силен звук на пукање.[48][49][50]
Водород пероксид е сигнална молекула за одбрана на растенијата од патогени.[51]
Водород пероксид има улоги како сигнална молекула во регулирањето на широк спектар на биолошки процеси.[52] Соединението е главен фактор вмешан во теоријата на стареење од слободните радикали, заснована на тоа колку лесно водород пероксид може да се распадне во хидроксилен радикал и како нуспроизводите од радикалниот супероксид на клеточниот метаболизам можат да реагираат со амбиенталната вода за да формираат водороден пероксид.[53] Овие хидроксилни радикали за возврат лесно реагираат и ги оштетуваат виталните клеточни компоненти, особено оние на митохондриите.[54][55][56] Најмалку една студија исто така се обиде да го поврзе производството на водород пероксид со ракот.[57] Овие студии често се цитирани во лажни тврдења за третман.
Количината на водород пероксид во биолошките системи може да се процени со помош на флуорометриска анализа.[58]
Употреба[уреди | уреди извор]
Белење[уреди | уреди извор]
Околу 60 % од светското производство на водород пероксид се користи за белење на целулоза и хартија.[31] Втората голема индустриска примена е производството на натриум перкарбонат и натриум перборат, кои се користат како благи избелувачи во детергентите за перење. Натриум перкарбонат, кој е додаток на натриум карбонат и водород пероксид, е активна состојка во производите за перење како што се детергентот за перење OxiClean и Tide. Кога се раствора во вода, ослободува водород пероксид и натриум карбонат,[18] Самите овие средства за белење се ефективни само на температури на миење од 60 °C (140 °F) или повисоки и така, често се користат заедно со активатори за белење, кои го олеснуваат чистењето на пониски температури. Се користи и како средство за избелување на брашно и средство за избелување на забите.
Производство на органски соединенија[уреди | уреди извор]
Се користи во производството на различни органски пероксиди, при што дибензоил пероксид е пример со голем волумен. Перокси киселини, како што се пероцетна киселина и мета-хлоропероксибензоева киселина, исто така, се произведуваат со употреба на водород пероксид. Водород пероксид се користи за создавање експлозиви базирани на органски пероксид, како што е ацетон пероксид. Се користи како иницијатор при полимеризации.
Третман на отпадни води[уреди | уреди извор]
Водород пероксид се користи во одредени процеси за третман на отпадни води за отстранување на органските нечистотии. Во напредната оксидациска обработка, Фентоновата реакција[59][60] го дава високо реактивниот хидроксилен радикал (•OH). Ова ги разградува органските соединенија, вклучувајќи ги и оние кои се обично робусни, како што се ароматичните или халогенираните соединенија.[61] Исто така, може да ги оксидира соединенијата на база на сулфур присутни во отпадот; што е корисно бидејќи генерално го намалува нивниот мирис.[62]
Средство за дезинфекција[уреди | уреди извор]
Водород пероксид може да се користи за стерилизација на различни површини,[63] вклучувајќи хируршки алатки[64] и може да се користи како пареа (VHP) за стерилизација на просторијата.[65] H
2O
2 покажува ефикасност со широк спектар против вируси, бактерии, квасци и бактериски спори.[66][67] Генерално, поголема активност е забележана против грам-позитивни од грам-негативни бактерии; сепак, присуството на каталаза или други пероксидази во овие организми може да ја зголеми толеранцијата во присуство на пониски концентрации.[68] Пониските нивоа на концентрација (3 %) ќе делуваат против повеќето спори; повисоките концентрации (7 до 30 %) и подолго време на контакт ќе ја подобрат спорицидната активност.[67][69]
Водородниот пероксид се смета за еколошки безбедна алтернатива на избелувачите базирани на хлор, бидејќи се разградува за да формира кислород и вода и генерално е препознаен како безбеден како антимикробно средство од страна на Управата за храна и лекови на САД (FDA).[70]
Пропелент[уреди | уреди извор]

H
2O
2 со висока концентрација се нарекува „пероксид со висок тест“ (HTP). Може да се користи или како монопропелант (не се меша со гориво) или како оксидаторска компонента на бипропелантна ракета. Употребата како монопропелант го користи разградувањето на водород пероксид од 70 - 98 % концентрација во пареа и кислород. Пропелентот се пумпа во комората за реакција, каде што катализаторот, обично сребрен или платински екран, предизвикува распаѓање, произведувајќи пареа на над 600 °C (1.100 °F), која се исфрла преку млазницата, генерирајќи потисок. Монопропелантот H
2O
2 произведува максимален специфичен импулс (Isp) од 161 s (1.6 kN·s/kg). Пероксидот беше првиот голем монопропелант усвоен за употреба во ракетни апликации. Хидразин на крајот ги замени водород-пероксид монопропелантните потисни апликации првенствено поради 25% зголемување на вакуум-специфичниот импулс.[71] Хидразин (токсичен) и водород пероксид (помалку токсичен [ACGIH TLV 0,01 и 1 ppm соодветно]) се единствените два монопропеланти (освен ладни гасови) кои биле широко прифатени и користени за погонски и енергетски апликации. Бел ракетен појас, системи за контрола на реакцијата за X-1, X-15, Кентаур, Меркур, Малиот Џо, како и генераторите на гас со турбо-пумпа за X-1, X-15, Јупитер, Редстон и Викинг користеа водород пероксид како монопропелант.[72]
Како бипропелант, H
2O
2 се распаѓа за да согорува гориво како оксидатор. Може да се постигнат специфични импулси до 350 s (3.5 kN·s/kg) во зависност од горивото. Пероксидот што се користи како оксидатор дава нешто понизок Isp од течниот кислород, но е густ, може да се складира, некриоген и може полесно да се користи за возење гасни турбини за давање високи притисоци користејќи ефикасен затворен циклус. Може да се користи и за регенеративно ладење на ракетни мотори. Пероксидот беше многу успешно користен како оксидатор во германските ракетни мотори од Втората светска војна (на пр. T-Stoff, кој содржи стабилизатор на оксихинолин, и за системот за засилување на монопропелантот Walter HWK 109-500 Starthilfe RATO со надворешно натрупување и за ракетата Walter HWK 109- серии на мотори кои се користат за Me 163B), најчесто користени со C-Stoff во самозапаллива хиперголна комбинација, и за евтините фрлачи на British Black Knight и Black Arrow. Во моментов, HTP се користи на суборбиталните ракети ILR-33 AMBER[73] и Nucleus.[74]
Во 1940-тите и 1950-тите, турбината замислена од Hellmuth Walter KG користела водород пероксид за употреба во подморници додека била потопена. Утврдено е дека е премногу бучен и бара премногу одржување во споредба со дизел-електричните системи. Некои торпеда користеле водород пероксид како оксидатор или погонско средство. Како можни причини за потонувањето на ХМС Сидон и руската подморница Курск, беше наведена грешка на операторот во употребата на торпеда со водород пероксид.[75] SAAB Underwater Systems го произведува Торпедо 2000. Ова торпедо, користено од шведската морнарица, се напојува со клипен мотор придвижуван од HTP како оксидатор и керозин како гориво во бипропелантниот систем.[76][77]
Употреба во домаќинството[уреди | уреди извор]

Водород пероксид има различни домашни намени, првенствено како средство за чистење и дезинфекција.
- Белење на косата
Разреден H
2O
2 (помеѓу 1,9 % и 12 %) измешан со воден амонијак се користи за избелување на човечка коса. Својството за избелување на хемикалијата го дава неговото име на фразата „пероксид русокоса“.[78] Водород пероксид се користи и за белење на забите. Може да се најде во повеќето пасти за заби за избелување. Водород пероксидот покажа позитивни резултати кои вклучуваат параметри за светлост на забите и хроматска нијанса.[79] Работи со оксидација на обоени пигменти на глеѓта каде што сенката на забот може да стане посветла. Водород пероксид може да се меша со сода бикарбона и сол за да се направи домашна паста за заби.[80]
- Отстранување на дамки од крв
Водород пероксид реагира со крвта како средство за белење, и затоа, ако дамката од крв е свежа или не е премногу стара, либералната примена на водород пероксид, доколку е потребно во повеќе од еднократно нанесување, ќе ја избели дамката целосно. По околу две минути од нанесувањето, крвта треба да биде избришана.[81][82]
- Третман на акни
Водород пероксид може да се користи за лекување на акни,[83] иако бензоил пероксид е почест третман.
Друга употреба[уреди | уреди извор]

- Светлечки стапчиња
Водород пероксид реагира со одредени ди-естери, како што е фенил оксалат естер (циалум), за да произведе хемилуминисценција; оваа апликација најчесто се среќава во форма на светлечки стапчиња.
- Хортикултура
Некои хортикултуристи и корисници на хидропоника се залагаат за употреба на слаб раствор на водород пероксид во растворите за наводнување. Нејзиното спонтано распаѓање ослободува кислород кој го подобрува развојот на коренот на растението и помага во лекувањето на гниењето на коренот (смрт на клеточниот корен поради недостаток на кислород) и на различни други штетници.[84][85]
За општи концентрации на наводнување се користи околу 0,1 % и тоа може да се зголеми до еден процент за антигабични дејства.[86] Тестовите покажуваат дека растителното зеленило може безбедно да толерира концентрации до 3 %.[87]
- Чување риби
Водород пероксид се користи во аквакултурата за контролирање на смртноста предизвикана од различни микроби. Во 2019 година, FDA на САД го одобри за контрола на сапролегнијаза кај сите риби со ладноводни перки и кај сите рипчиња со прсти и возрасни ладни и топловодни риби, за контрола на болеста надворешен колонарис кај топловодните перки и за контрола на Gyrodactylus spp. кај салмонидите кои се одгледуваат во слатководна вода.[88] Лабораториските тестови спроведени од одгледувачи на риби покажаа дека обичниот водороден пероксид може безбедно да се користи за да се обезбеди кислород за малите риби. Водородниот пероксид ослободува кислород со распаѓање кога е изложен на катализатори како што е манган диоксид.
- Отстранување на пожолтувањето од застарената пластика
Водород пероксид може да се користи во комбинација со извор на УВ светлина за да се отстрани пожолтувањето од пластиката од бела или светло сив акрилонитрил бутадиен стирен (ABS) за делумно или целосно враќање на оригиналната боја. Во ретрокомпјутерската сцена, овој процес најчесто се нарекува retrоbright.
Безбедност[уреди | уреди извор]
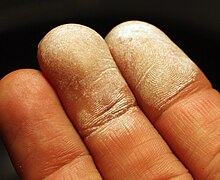
2O
2
Прописите варираат, но ниските концентрации, како 5 %, се широко достапни и легални за купување за медицинска употреба. Повеќето раствори на пероксид без рецепт не се погодни за ингестија. Повисоките концентрации може да се сметаат за опасни и обично се придружени со безбедносен лист со податоци (SDS). Во високи концентрации, водород пероксидот е агресивен оксидатор и ќе кородира многу материјали, вклучувајќи ја и човечката кожа. Во присуство на редукционен агенс, високите концентрации на H
2O
2 ќе реагираат бурно.[89] Додека концентрациите до 35 % произведуваат само „бели“ кислородни меурчиња во кожата (и некои болки од нагризување) кои исчезнуваат со крвта во рок од 30 - 45 минути, концентрациите од 98 % раствораат хартија. Сепак, концентрациите до 3 % може да бидат опасни за окото поради еволуцијата на кислород во окото.[90]
Струите на водород пероксид со висока концентрација, обично над 40%, треба да се сметаат за опасни поради тоа што концентрираниот водороден пероксид ја исполнува дефиницијата за DOT оксидатор според прописите на САД, доколку се испуштат во животната средина. Известената количина на EPA (RQ) за опасниот отпад D001 е 100 lbs (45 kg) или приближно 10 американски галони (38 L) концентриран водороден пероксид.
Водород пероксид треба да се чува на ладно, суво, добро проветрено место и подалеку од извори на пламен или запаливи материи. Треба да се чува во контејнер составен од нереактивни материјали како што се нерѓосувачки челик или стакло (други материјали, вклучително и некои пластика и алуминиумски легури, исто така може да бидат соодветни).[91] Бидејќи брзо се распаѓа кога е изложен на светлина, треба да се чува во непроѕирен контејнер, а фармацевтските формулации обично доаѓаат во кафени шишиња кои ја блокираат светлината[92]
Водород пероксид, било во чиста или во разредена форма, може да претставува неколку ризици, а главниот е тоа што формира експлозивни смеси при контакт со органски соединенија.[93] Дестилацијата на водород пероксид при нормален притисок е многу опасна. Тој е исто така корозивен, особено кога е концентриран, но дури и растворите со домашна јачина може да предизвикаат иритација на очите, мукозните мембрани и кожата.[94] Голтањето раствори на водород пероксид е особено опасно, бидејќи со распаѓање во желудникот се ослободуваат големи количини гас (десет пати поголем од волуменот на раствор од 3 %), што доведува до внатрешна надуеност. Вдишување над 10 % може да предизвика тешка пулмонална иритација.[95]
Со значителен притисок на пареа (1,2 kPa на 50 °C),[96] пареата на водород-пероксид е потенцијално опасна. Според американскиот NIOSH, границата веднаш опасна по животот и здравјето (IDLH) е само 75 ppm.[97] Управата за безбедност и здравје при работа на САД (OSHA) воспостави дозволена граница на изложеност од 1,0 ppm пресметана како временски пондерирана просек од 8 часа (29 CFR 1910.1000, Табела Z-1).[93] Водород пероксид, исто така, е класифициран од страна на Американската конференција на владини индустриски хигиеничари (ACGIH) како „познат животински канцероген, со непозната важност кон луѓето“.[98] За работните места каде што постои ризик од изложеност на опасните концентрации на пареите, треба да се користат континуирани монитори за водород пероксид. Информациите за опасностите од водород пероксид се достапни од OSHA[93] и од ATSDR.[99]
Заздравување на раните[уреди | уреди извор]
Историски гледано, водород пероксид се користел за дезинфекција на рани, делумно поради неговата ниска цена и брза достапност во споредба со другите антисептици.[100]
Постојат спротивставени докази за ефектот на водород пероксид врз заздравувањето на раните. Некои истражувања наоѓаат корист, додека други истражувања откриваат одложувања и инхибиција на заздравувањето.[101] Неговата употреба за домашно лекување на рани е генерално контраиндицирана.[102] 1,5 – 3 % водород пероксид се користи како средство за дезинфекција во стоматологијата, особено во ендодотски третмани заедно со хипохлорит и хлорхексидин и 1 - 1,5 % е исто така корисен за третман на воспаление на унмиците.[103]
Употреба во алтернативна медицина[уреди | уреди извор]
Практичарите на алтернативна медицина се залагаат за употреба на водород пероксид за различни состојби, вклучувајќи емфизем, грип, СИДА, а особено рак.[104] Нема докази за ефикасност и во некои случаи се покажало како фатално.[105][106][107][108][109]
И ефикасноста и безбедноста на терапијата со водород пероксид е научно сомнителна. Водород пероксид се произведува од имунолошкиот систем, но на внимателно контролиран начин. Клетките наречени фагоцити ги голтаат патогените и потоа користат водород пероксид за да ги уништат. Пероксидот е токсичен и за клетката и за патогенот и затоа се чува во посебен оддел, наречен фагозом. Слободниот водороден пероксид ќе го оштети секое ткиво со кое ќе се сретне преку оксидативен стрес, процес кој исто така е предложен како причина за рак.[110] Не се поддржани тврдењата дека терапијата со водород пероксид ги зголемува клеточните нивоа на кислород. Од администрираните количини би се очекувало да обезбедат многу малку дополнителен кислород во споредба со она што е достапно од нормалното дишење. Исто така, тешко е да се подигне нивото на кислород околу клетките на ракот во туморот, бидејќи снабдувањето со крв има тенденција да биде слабо, ситуација позната како туморска хипоксија.
Големи орални дози на водород пероксид во концентрација од 3 % може да предизвикаат иритација и појава на меурчиња во устата, грлото и стомакот, како и абдоминална болка, повраќање и дијареа.[105] Голтање на водород пероксид во концентрации од 35 % или повисоки е вмешано како причина за бројни настани на гасна емболија што резултира со хоспитализација. Во овие случаи, хипербарична кислородна терапија била користена за лекување на емболиите.[111]
Интравенското вбризгување на водород пероксид е поврзано со неколку смртни случаи.[107][108][109] Американското здружение за рак наведува дека „нема научен доказ дека водород пероксидот е безбеден, ефикасен или корисен третман за рак“.[106] Понатаму, терапијата не е одобрена од американската FDA.
Историски инциденти[уреди | уреди извор]
- На 16 јули 1934 година, во Кумерсдорф, Германија, резервоар за гориво што содржеше експериментална монопропелантна смеса која се состои од водород пероксид и етанол експлодираше за време на тест, при што загинаа три лица.[112]
- За време на Втората светска војна, лекарите во германските концентрациони логори експериментирале со употреба на инјекции со водород пероксид во убивањето на човечки субјекти.[113]
- Во април 1992 година, се случи експлозија во фабриката за водород пероксид во Жари во Франција, поради технички дефект на компјутеризираниот систем за контрола и што резултираше со еден фатален исход и широко уништување на постројката.[114]
- Неколку луѓе добија полесни повреди по истурање на водород пероксид на летот меѓу американските градови Орландо и Мемфис на 28 октомври 1998 година.[115]
- Руската подморница К-141 Курск отплови за да изведе вежба со гаѓање кукла торпеда кон „Пјотр Великиј“, борбен крстосувач од класата „Киров“. На 12 август 2000 година, во 11:28 часот по локално време (07:28 UTC), се случи експлозија додека се подготвуваше да ги испука торпедата. Единствениот веродостоен извештај до денес е дека тоа се должи на неуспехот и експлозијата на едно од торпедата на Курск со водород пероксид. Се верува дека HTP, форма на високо концентриран водороден пероксид што се користи како погонско гориво за торпедото, се влеал низ неговиот контејнер, оштетен или од 'рѓа или во постапката на товарење назад на копно, каде што инцидентот со едно од торпедата случајно допрел до земја останал непријавен. Садот беше изгубен со сите раце. Сличен инцидент беше одговорен за загубата на ХМС Сидон во 1955 година.[116]
- На 15 август 2010 година, на 54-тиот кат на 1515 Бродвеј, на Тајмс Сквер, Њујорк, се случи истурање од околу 30 американски галони (110 литри) течност за чистење. Излевањето, за кое портпаролот на Њујоршката противпожарна служба рече дека е од водород пероксид, го затвори Бродвеј помеѓу улиците Западна 42-та и Западната 48-ма додека противпожарните возила реагираа на хазматската ситуација. Нема пријавени повредени.[117]
Наводи[уреди | уреди извор]
- ↑ Easton MF, Mitchell AG, Wynne-Jones WF (1952). „The behaviour of mixtures of hydrogen peroxide and water. Part 1.—Determination of the densities of mixtures of hydrogen peroxide and water“. Transactions of the Faraday Society. 48: 796–801. doi:10.1039/TF9524800796. S2CID 96669623. Архивирано од изворникот 15 February 2022. Посетено на 30 November 2019.
- ↑ „Hydrogen peroxide“. www.chemsrc.com. Архивирано од изворникот 8 August 2017. Посетено на 3 May 2018.
- ↑ 3,0 3,1 3,2 3,3 „Џебен водич за опасните хемиски материи #0335“. Национален институт за безбедност и здравје при работа (NIOSH). (англиски)
- ↑ 4,0 4,1 4,2 „Hydrogen peroxide“. Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ↑ Housecroft CE, Sharpe AG (2005). Inorganic Chemistry (2. изд.). Pearson Prentice-Hall. стр. 443. ISBN 0130-39913-2.
- ↑ Hill CN (2001). A Vertical Empire: The History of the UK Rocket launch and Space Programme, 1950–1971. Imperial College Press. ISBN 978-1-86094-268-6. Архивирано од изворникот 13 April 2021. Посетено на 24 August 2020.
- ↑ Brauer G, уред. (1963). Handbook of preparative inorganic chemistry. 1. Translation editing by Reed F. (2. изд.). New York: Academic Press. стр. 140. ISBN 978-0-12-126601-1.
- ↑ Hunt RH, Leacock RA, Peters CW, Hecht KT (1965). „Internal-Rotation in Hydrogen Peroxide: The Far-Infrared Spectrum and the Determination of the Hindering Potential“ (PDF). The Journal of Chemical Physics. 42 (6): 1931. Bibcode:1965JChPh..42.1931H. doi:10.1063/1.1696228. hdl:2027.42/71115. Архивирано (PDF) од изворникот 9 April 2014. Посетено на 9 April 2014.
- ↑ Ball R, Brindley J (March 2016). „The Life Story of Hydrogen Peroxide III: Chirality and Physical Effects at the Dawn of Life“. Origins of Life and Evolution of the Biosphere. 46 (1): 81–93. Bibcode:2016OLEB...46...81B. doi:10.1007/s11084-015-9465-y. PMID 26399407. S2CID 9564774.
- ↑ Dougherty DA, Anslyn EV (2005). Modern Physical Organic Chemistry. University Science. стр. 122. ISBN 978-1-891389-31-3.
- ↑ Abrahams SC, Collin RL, Lipscomb WN (1 January 1951). „The crystal structure of hydrogen peroxide“. Acta Crystallographica. 4 (1): 15–20. doi:10.1107/S0365110X51000039.
- ↑ „Hydrogen Peroxide Technical Library“ (PDF). Архивирано од изворникот (PDF) на 29 December 2009. Посетено на 3 March 2016.
- ↑ Flohé L (December 2020). „Looking Back at the Early Stages of Redox Biology“. Antioxidants. 9 (12): 1254. doi:10.3390/antiox9121254. PMC 7763103 Проверете ја вредноста
|pmc=(help). PMID 33317108 Проверете ја вредноста|pmid=(help).I checked Humboldt’s pertinent publication carefully, but was unable to find an unambiguous proof of this assumption; the description of the starting materials (“Alaun-Erden” or “schwere Erden”) were just too unprecise to understand what kind of chemical experiments he performed.
- ↑ Gilbert LW (1820). „Der tropfbar flüssige Sauerstoff, oder das oxygenierte Wasser“. Annals of Physics (германски). 65–66 (1): 3. Bibcode:1820AnP....64....1T. doi:10.1002/andp.18200640102.
- ↑ Thénard LJ (1818). „Observations sur des nouvelles combinaisons entre l'oxigène et divers acides“. Annales de chimie et de physique. 2nd series. 8: 306–312. Архивирано од изворникот 3 September 2016. Посетено на 9 February 2016.
- ↑ Giguère PA. „Hydrogen peroxide“. Access Science. McGraw-Hill Education. doi:10.1036/1097-8542.329200. Архивирано од изворникот 30 November 2018. Посетено на 28 November 2018.
Hydrogen peroxide was discovered in 1818 by the French chemist Louis-Jacques Thenard, who named it eau oxygénée (oxygenated water).
- ↑ Preiato D (5 March 2020). „What is oxygenated water?“. Healthline. Healthline Media. Архивирано од изворникот 31 October 2020. Посетено на 23 September 2020.
- ↑ 18,0 18,1 Jones CW, Clark JH (1999). Applications of Hydrogen Peroxide and Derivatives. Royal Society of Chemistry. ISBN 978-0-85404-536-5.
- ↑ 19,0 19,1 Offermanns H, Dittrich G, Steiner N (2000). „Wasserstoffperoxid in Umweltschutz und Synthese“. Chemie in unserer Zeit. 34 (3): 150. doi:10.1002/1521-3781(200006)34:3<150::AID-CIUZ150>3.0.CO;2-A.
- ↑ Wolffenstein R (October 1894). „Concentration und Destillation von Wasserstoffsuperoxyd“. Berichte der Deutschen Chemischen Gesellschaft (германски). 27 (3): 3307–3312. doi:10.1002/cber.189402703127. Архивирано од изворникот 13 February 2016. Посетено на 29 June 2014.
- ↑ Carrara G (1892). „Sul peso molecolare e sul potere rifrangente dell' acqua ossigenata“ [On the molecular weight and on the refracting power of hydrogen peroxide]. Atti della Reale Accademia dei Lincei. 1 (2): 19–24. Архивирано од изворникот на 4 September 2016.
Carrara's findings were confirmed by: W. R. Orndorff and John White (1893) "The molecular weight of hydrogen peroxide and of benzoyl peroxide," Архивирано на 4 септември 2016 г. American Chemical Journal, 15 : 347–356. - ↑ See, for example:
- In 1882, Kingzett proposed as a structure H
2O=O. See: Kingzett T (29 September 1882). „On the activity of oxygen and the mode of formation of hydrogen dioxide“. The Chemical News. 46 (1192): 141–142. Архивирано од изворникот 3 September 2016. Посетено на 9 February 2016. - In his 1922 textbook, Joseph Mellor considered three hypothetical molecular structures for hydrogen peroxide, admitting (p. 952): "... the constitution of this compound has not been yet established by unequivocal experiments". See: Joseph William Mellor, A Comprehensive Treatise on Inorganic and Theoretical Chemistry, vol. 1 (London, England: Longmans, Green and Co., 1922), p. 952–956. Архивирано на 3 септември 2016 г.
- W. C. Schumb, C. N. Satterfield, and R. L. Wentworth (1 December 1953) "Report no. 43: Hydrogen peroxide, Part two" Архивирано на 26 февруари 2015 г., Office of Naval Research, Contract No. N5ori-07819 On p. 178, the authors present six hypothetical models (including cis-trans isomers) for hydrogen peroxide's molecular structure. On p. 184, the present structure is considered almost certainly correct—although a small doubt remained. (Note: The report by Schumb et al. was reprinted as: W. C. Schumb, C. N. Satterfield, and R. L. Wentworth, Hydrogen Peroxide (New York, New York: Reinhold Publishing Corp. (American Chemical Society Monograph), 1955).)
- In 1882, Kingzett proposed as a structure H
- ↑ Penney WG, Sutherland GB (1934). „The theory of the structure of hydrogen peroxide and hydrazine“. Journal of Chemical Physics. 2 (8): 492–498. Bibcode:1934JChPh...2..492P. doi:10.1063/1.1749518.
- ↑ Penney WG, Sutherland GB (1934). „A note on the structure of H2O2 and H4N2 with particular reference to electric moments and free rotation“. Transactions of the Faraday Society. 30: 898–902. doi:10.1039/tf934300898b.
- ↑ „Preparing to manufacture hydrogen peroxide“ (PDF). IDC Technologies. Архивирано (PDF) од изворникот 3 August 2021. Посетено на 14 February 2022.
- ↑ 26,0 26,1 26,2 Campos-Martin JM, Blanco-Brieva G, Fierro JL (October 2006). „Hydrogen peroxide synthesis: an outlook beyond the anthraquinone process“. Angewandte Chemie. 45 (42): 6962–6984. doi:10.1002/anie.200503779. PMID 17039551. S2CID 23286196.
- ↑ H. Riedl and G. Pfleiderer, U.S. Patent 2,158,525 (2 October 1936 in USA, and 10 October 1935 in Germany) to I. G. Farbenindustrie, Germany
- ↑ Mellor JW (1922). Modern Inorganic Chemistry. Longmans, Green and Co. стр. 192–195.
- ↑ Noritaka Mizuno Gabriele Centi, Siglinda Perathoner, Salvatore Abate "Direct Synthesis of Hydrogen Peroxide: Recent Advances" in Modern Heterogeneous Oxidation Catalysis: Design, Reactions and Characterization 2009, Wiley-VCH. doi:10.1002/9783527627547.ch8
- ↑ Edwards JK, Solsona B, N EN, Carley AF, Herzing AA, Kiely CJ, Hutchings GJ (February 2009). „Switching off hydrogen peroxide hydrogenation in the direct synthesis process“. Science. 323 (5917): 1037–1041. Bibcode:2009Sci...323.1037E. doi:10.1126/science.1168980. PMID 19229032. S2CID 1828874. Архивирано од изворникот 15 February 2022. Посетено на 30 November 2019.
- ↑ 31,0 31,1 Hage R, Lienke A (December 2005). „Applications of transition-metal catalysts to textile and wood-pulp bleaching“. Angewandte Chemie. 45 (2): 206–222. doi:10.1002/anie.200500525. PMID 16342123. Архивирано од изворникот 25 January 2022. Посетено на 14 February 2022.
- ↑ Special Report No. 10. Hydrogen Peroxide. OEL Criteria Document. CAS No. 7722-84-1. July 1996. ISSN-0773-8072-10.
- ↑ „Decomposition of Hydrogen Peroxide - Kinetics and Review of Chosen Catalysts“ (PDF). Архивирано (PDF) од изворникот 22 December 2018. Посетено на 30 August 2019.
- ↑ Petrucci RH (2007). General Chemistry: Principles & Modern Applications (9. изд.). Prentice Hall. стр. 606. ISBN 978-0-13-149330-8.
- ↑ Housecroft CE, Sharpe AG (2005). Inorganic Chemistry (2. изд.). Pearson Prentice-Hall. стр. 444. ISBN 0130-39913-2.
- ↑ Ravikumar KS, Kesavan V, Crousse B, Bonnet-Delpon D, Bégué JP (2003). „Mild and Selective Oxidation of Sulfur Compounds in Trifluoroethanol: Diphenyldisulfide and Methyl phenyl Sulfoxide“. Org. Synth. 80: 184. doi:10.15227/orgsyn.080.0184.
- ↑ Xu WL, Li YZ, Zhang QS, Zhu HS (2004). „A Selective, Convenient, and Efficient Conversion of Sulfides to Sulfoxides“. Synthesis (2): 227–232. doi:10.1055/s-2004-44387.
- ↑ Mayer RJ, Ofial AR (May 2018). „Nucleophilic Reactivities of Bleach Reagents“. Organic Letters. 20 (10): 2816–2820. doi:10.1021/acs.orglett.8b00645. PMID 29741385.
- ↑ Chernyshov IY, Vener MV, Prikhodchenko PV, Medvedev AG, Lev O, Churakov AV (2017-01-04). „Peroxosolvates: Formation Criteria, H2O2 Hydrogen Bonding, and Isomorphism with the Corresponding Hydrates“. Crystal Growth & Design. 17 (1): 214–220. doi:10.1021/acs.cgd.6b01449. ISSN 1528-7483.
- ↑ Löffler G. and Petrides, P. E. Physiologische Chemie. 4 ed., p. 288, Springer, Berlin 1988, ISBN 3-540-18163-6 (in German)
- ↑ Löffler G. and Petrides, P. E. Physiologische Chemie. 4 ed., pp. 321–322, Springer, Berlin 1988, ISBN 3-540-18163-6 (in German)
- ↑ Gabaldón T (March 2010). „Peroxisome diversity and evolution“. Philosophical Transactions of the Royal Society of London. Series B, Biological Sciences. 365 (1541): 765–773. doi:10.1098/rstb.2009.0240. PMC 2817229. PMID 20124343.
- ↑ Wanders RJ, Waterham HR (2006). „Biochemistry of mammalian peroxisomes revisited“. Annual Review of Biochemistry. 75 (1): 295–332. doi:10.1146/annurev.biochem.74.082803.133329. PMID 16756494.
- ↑ Nelson D, Cox C, Lehninger AL, Cox MM (2001). Lehninger Biochemie (German). Springer. стр. 663–664. ISBN 3-540-41813-X. Архивирано од изворникот на 28 February 2017.CS1-одржување: непрепознаен јазик (link)
- ↑ Riley, Edward P. et al. (ed.) Fetal Alcoholspectrum Disorder Fasd: Management and Policy Perspectives Архивирано на 28 февруари 2017 г., Wiley-VCH, 2010, ISBN 3-527-32839-4 p. 112
- ↑ 46,0 46,1 Nelson, David; Cox, Michael; Lehninger, Albert L. and Cox, Michael M. Lehninger Biochemie, p. 932, Springer, 2001, ISBN 3-540-41813-X (in German)
- ↑ Kröger M (1989). „History“. Chemie in unserer Zeit. 23: 34–35. doi:10.1002/ciuz.19890230106.
- ↑ Schildknecht H, Holoubek K (1961). „The bombardier beetle and its chemical explosion“. Angewandte Chemie. 73: 1–7. doi:10.1002/ange.19610730102.
- ↑ Weber CG (Winter 1981). „The Bombadier Beetle Myth Exploded“. Creation/Evolution. 2 (1): 1–5. Архивирано од изворникот 29 September 2017. Посетено на 12 November 2017.
- ↑ Isaak M (30 May 2003). „Bombardier Beetles and the Argument of Design“. TalkOrigins Archive. Архивирано од изворникот 16 November 2017. Посетено на 12 November 2017.
- ↑ „Wie Pflanzen sich schützen, Helmholtz-Institute of Biochemical Plant Pathology (in German)“ (PDF) (германски). Helmholtz-Institute of Biochemical Plant Pathology. Архивирано од изворникот (PDF) на 23 July 2011. Посетено на 14 February 2022.
- ↑ Veal EA, Day AM, Morgan BA (April 2007). „Hydrogen peroxide sensing and signaling“. Molecular Cell. 26 (1): 1–14. doi:10.1016/j.molcel.2007.03.016. PMID 17434122.
- ↑ Weindruch R (1 December 2006). „Calorie Restriction and Aging“. Scientific American. Архивирано од изворникот 14 February 2022. Посетено на 14 February 2022.
- ↑ Giorgio M, Trinei M, Migliaccio E, Pelicci PG (September 2007). „Hydrogen peroxide: a metabolic by-product or a common mediator of ageing signals?“. Nature Reviews. Molecular Cell Biology. 8 (9): 722–728. doi:10.1038/nrm2240. PMID 17700625. S2CID 6407526. Архивирано од изворникот 15 February 2022. Посетено на 7 February 2020.
- ↑ Gonzalez D, Bejarano I, Barriga C, Rodriguez AB, Pariente JA (2010). „Oxidative Stress-Induced Caspases are Regulated in Human Myeloid HL-60 Cells by Calcium Signal“. Current Signal Transduction Therapy. 5 (2): 181–186. doi:10.2174/157436210791112172.
- ↑ Bejarano I, Espino J, González-Flores D, Casado JG, Redondo PC, Rosado JA, и др. (September 2009). „Role of Calcium Signals on Hydrogen Peroxide-Induced Apoptosis in Human Myeloid HL-60 Cells“. International Journal of Biomedical Science. 5 (3): 246–256. PMC 3614781. PMID 23675144.
- ↑ López-Lázaro M (July 2007). „Dual role of hydrogen peroxide in cancer: possible relevance to cancer chemoprevention and therapy“. Cancer Letters. 252 (1): 1–8. doi:10.1016/j.canlet.2006.10.029. PMID 17150302.
- ↑ Rapoport R, Hanukoglu I, Sklan D (May 1994). „A fluorimetric assay for hydrogen peroxide, suitable for NAD(P)H-dependent superoxide generating redox systems“. Analytical Biochemistry. 218 (2): 309–313. doi:10.1006/abio.1994.1183. PMID 8074285. S2CID 40487242. Архивирано од изворникот 18 March 2020. Посетено на 1 July 2019.
- ↑ Tarr MA, уред. (2003). Chemical degradation methods for wastes and pollutants environmental and industrial applications. New York: M. Dekker. стр. 165. ISBN 978-0-203-91255-3.
- ↑ Pignatello JJ, Oliveros E, MacKay A (January 2006). „Advanced Oxidation Processes for Organic Contaminant Destruction Based on the Fenton Reaction and Related Chemistry“. Critical Reviews in Environmental Science and Technology. 36 (1): 1–84. doi:10.1080/10643380500326564. S2CID 93052585.
- ↑ Pera-Titus M, Garcıa-Molina V, Baños MA, Giménez J, Esplugas S (February 2004). „Degradation of chlorophenols by means of advanced oxidation processes: a general review“. Applied Catalysis B: Environmental. 47 (4): 219–256. doi:10.1016/j.apcatb.2003.09.010.
- ↑ Goor G, Glenneberg J, Jacobi S (2007). „Hydrogen Peroxide“. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a13_443.pub2. ISBN 978-3-527-30673-2.
- ↑ Ascenzi JM, уред. (1996). Handbook of disinfectants and antiseptics. New York: M. Dekker. стр. 161. ISBN 978-0-8247-9524-5.
- ↑ Rutala WA, Weber DJ (September 2004). „Disinfection and sterilization in health care facilities: what clinicians need to know“. Clinical Infectious Diseases. 39 (5): 702–709. doi:10.1086/423182. PMID 15356786.
- ↑ Falagas ME, Thomaidis PC, Kotsantis IK, Sgouros K, Samonis G, Karageorgopoulos DE (July 2011). „Airborne hydrogen peroxide for disinfection of the hospital environment and infection control: a systematic review“. The Journal of Hospital Infection. 78 (3): 171–177. doi:10.1016/j.jhin.2010.12.006. PMID 21392848.
- ↑ Block SS, уред. (2000). „Chapter 9: Peroxygen compounds“. Disinfection, sterilization, and preservation (5. изд.). Philadelphia: Lea & Febiger. стр. 185–204. ISBN 978-0-683-30740-5.
- ↑ 67,0 67,1 „Chemical Disinfectants | Disinfection & Sterilization Guidelines | Guidelines Library | Infection Control | CDC“. www.cdc.gov (англиски). 4 April 2019. Архивирано од изворникот 1 July 2017. Посетено на 12 April 2020.
- ↑ McDonnell G, Russell AD (January 1999). „Antiseptics and disinfectants: activity, action, and resistance“. Clinical Microbiology Reviews. 12 (1): 147–179. doi:10.1128/cmr.12.1.147. PMC 88911. PMID 9880479.
- ↑ Block SS, уред. (2000). „Chapter 27: Chemical Sporicidal and Sporostatic Agents“. Disinfection, sterilization, and preservation (5. изд.). Philadelphia: Lea & Febiger. стр. 529–543. ISBN 978-0-683-30740-5.
- ↑ „Sec. 184.1366 Hydrogen peroxide“. U.S. Government Printing Office via GPO Access. 1 April 2001. Архивирано од изворникот на 3 July 2007. Посетено на 7 July 2007.
- ↑ Wernimont EJ (9–12 July 2006). System Trade Parameter Comparison of Monopropellants: Hydrogen Peroxide vs Hydrazine and Others (PDF). 42nd AIAA/ASME/SAE/ASEE Joint Propulsion Conference & Exhibit. Sacramento, California. Архивирано од изворникот (PDF) на 10 December 2014.
- ↑ Ventura M, Mullens P (19 June 1999). „The Use of Hydrogen Peroxide for Propulsion and Power“ (PDF). General Kinetics, LLC. Архивирано од изворникот (PDF) на 10 December 2014. Посетено на 10 December 2014.
- ↑ Cieśliński D (2021). „Polish civil rockets' development overview“. Архивирано од изворникот 6 February 2022. Посетено на 15 February 2022.
- ↑ „Nucleus: A Very Different Way to Launch into Space“. Nammo (англиски). Архивирано од изворникот 6 February 2022. Посетено на 2022-02-06.
- ↑ „Peroxide Accident – Walter Web Site“. Histarmar.com.ar. Архивирано од изворникот на 10 December 2014. Посетено на 2015-02-14.
- ↑ Scott R (November 1997). „Homing Instincts“. Jane's Navy Steam Generated by Catalytic Decomposition of 80–90% Hydrogen Peroxide Was Used for Driving the Turbopump Turbines of the V-2 Rockets, the X-15 Rocketplanes, the Early Centaur RL-10 Engines and is Still Used on Soyuz for That Purpose Today. International. Архивирано од изворникот на 17 July 2011. Посетено на 12 May 2007.
- ↑ „Soyuz using hydrogen peroxide propellant“. NASA. Архивирано од изворникот на 5 August 2013.
- ↑ Lane N (2003). Oxygen : the molecule that made the world (First issued in paperback, repr.. изд.). Oxford: Oxford University Press. стр. 117. ISBN 978-0-19-860783-0. Архивирано од изворникот 13 April 2021. Посетено на 12 November 2020.
- ↑ Sulieman M, Addy M, MacDonald E, Rees JS (May 2004). „The effect of hydrogen peroxide concentration on the outcome of tooth whitening: an in vitro study“. Journal of Dentistry (English). Elsevier Ltd. 32 (4): 295–299. doi:10.1016/j.jdent.2004.01.003. PMID 15053912. Архивирано од изворникот 15 February 2022. Посетено на 30 September 2021.CS1-одржување: непрепознаен јазик (link)
- ↑ Shepherd S. „Brushing Up on Gum Disease“. FDA Consumer. Архивирано од изворникот на 14 May 2007. Посетено на 7 July 2007.
- ↑ Gibbs KB (14 November 2016). „How to remove blood stains from clothes and furniture“. Today.com. Архивирано од изворникот 20 May 2021. Посетено на 5 August 2021.
- ↑ Mayntz M. „Dried Blood Stain Removal“. Lovetoknow.com. Архивирано од изворникот 17 August 2021. Посетено на 5 August 2021.
- ↑ Capizzi R, Landi F, Milani M, Amerio P (August 2004). „Skin tolerability and efficacy of combination therapy with hydrogen peroxide stabilized cream and adapalene gel in comparison with benzoyl peroxide cream and adapalene gel in common acne. A randomized, investigator-masked, controlled trial“. The British Journal of Dermatology. 151 (2): 481–484. doi:10.1111/j.1365-2133.2004.06067.x. PMID 15327558. S2CID 2611939.
- ↑ „Ways to use Hydrogen Peroxide in the Garden“. Using Hydrogen Peroxide. Архивирано од изворникот на 4 March 2016. Посетено на 3 March 2016.
- ↑ Bhattarai SP, Su N, Midmore DJ (2005). Oxygation Unlocks Yield Potentials of Crops in Oxygen-Limited Soil Environments. Advances in Agronomy. 88. стр. 313–377. doi:10.1016/S0065-2113(05)88008-3. ISBN 978-0-12-000786-8.
- ↑ „Hydrogen Peroxide for Plants and Garden“. 7 September 2019. Архивирано од изворникот 10 May 2021. Посетено на 10 May 2021.
- ↑ „Effect of hydrogen peroxide spraying on Hydrocotyle ranunculoides“. Архивирано од изворникот 24 March 2020. Посетено на 10 May 2021.
- ↑ „FDA Approves Additional Indications for 35% PEROX-AID (hydrogen peroxide) for Use in Certain Finfish“. FDA (англиски). 2019-07-26. Архивирано од изворникот 12 December 2019. Посетено на 2019-12-19.
- ↑ Greene B, Baker D, Frazier W. „Hydrogen Peroxide Accidents and Incidents: What we can learn from history“ (PDF). NASA. Архивирано (PDF) од изворникот 6 April 2019. Посетено на 6 April 2019.
- ↑ see Hans Marquardt, Lehrbuch der Toxikologie
- ↑ „Material Compatibility with Hydrogen Peroxide“. Архивирано од изворникот на 4 March 2016. Посетено на 3 March 2016.
- ↑ „Hydrogen Peroxide Mouthwash is it Safe?“. Архивирано од изворникот на 20 December 2013. Посетено на 30 October 2013.
- ↑ 93,0 93,1 93,2 „Occupational Safety and Health Guideline for Hydrogen Peroxide“. Архивирано од изворникот на 13 May 2013.
- ↑ For example, see an MSDS for a 3% peroxide solution Архивирано на 15 април 2012 г..
- ↑ H2O2 toxicity and dangers Архивирано на 5 јуни 2012 г. Agency for Toxic Substances and Disease Registry website
- ↑ CRC Handbook of Chemistry and Physics, 76th Ed, 1995–1996
- ↑ „CDC – Immediately Dangerous to Life or Health Concentrations (IDLH): Chemical Listing and Documentation of Revised IDLH Values – NIOSH Publications and Products“. 25 October 2017. Архивирано од изворникот 17 November 2012. Посетено на 20 October 2018.
- ↑ „Threshold Limit Values for Chemical Substances and Physical Agents & Biological Exposure Indices, ACGIH“ (PDF). Архивирано од изворникот (PDF) на 2 June 2013.
- ↑ „ATSDR – Redirect – MMG: Hydrogen Peroxide“. Архивирано од изворникот на 3 March 2016. Посетено на 3 March 2016.
- ↑ Wilgus TA, Bergdall VK, Dipietro LA, Oberyszyn TM (2005). „Hydrogen peroxide disrupts scarless fetal wound repair“. Wound Repair and Regeneration. 13 (5): 513–519. doi:10.1111/j.1067-1927.2005.00072.x. PMID 16176460. S2CID 1028923.
- ↑ Urban MV, Rath T, Radtke C (June 2019). „Hydrogen peroxide (H2O2): a review of its use in surgery“. Wiener Medizinische Wochenschrift. 169 (9–10): 222–225. doi:10.1007/s10354-017-0610-2. PMID 29147868. S2CID 35739209.
- ↑ „Cleveleand Clinic: What Is Hydrogen Peroxide Good For?“. December 2021. Посетено на 25 August 2022.
- ↑ see e.g. Detlev Heidemann, Endodontie, Urban&Fischer 2001
- ↑ Douglass WC (1995). Hydrogen peroxide : medical miracle. Atlanta, GA: Second Opinion Pub. ISBN 978-1-885236-07-4.
- ↑ 105,0 105,1 Hydrogen Peroxide, 3%. 3. Hazards Identification Southeast Fisheries Science Center, daughter agency of NOAA.
- ↑ 106,0 106,1 „Questionable methods of cancer management: hydrogen peroxide and other 'hyperoxygenation' therapies“. CA: A Cancer Journal for Clinicians. 43 (1): 47–56. 1993. doi:10.3322/canjclin.43.1.47. PMID 8422605. S2CID 36911297.
- ↑ 107,0 107,1 Cooper A (12 January 2005). „A Prescription for Death?“. CBS News. Архивирано од изворникот 17 July 2007. Посетено на 7 July 2007.
- ↑ 108,0 108,1 Mikkelson B (30 April 2006). „Hydrogen Peroxide“. Snopes.com. Архивирано од изворникот 15 February 2022. Посетено на 7 July 2007.
- ↑ 109,0 109,1 „Naturopath Sentenced For Injecting Teen With Hydrogen Peroxide – 7NEWS Denver“. Thedenverchannel.com. 2006-03-27. Архивирано од изворникот на 20 March 2014. Посетено на 2015-02-14.
- ↑ Halliwell B (January 2007). „Oxidative stress and cancer: have we moved forward?“. The Biochemical Journal. 401 (1): 1–11. doi:10.1042/BJ20061131. PMID 17150040. S2CID 850978. Архивирано од изворникот 15 February 2022. Посетено на 30 November 2019.
- ↑ French LK, Horowitz BZ, McKeown NJ (July 2010). „Hydrogen peroxide ingestion associated with portal venous gas and treatment with hyperbaric oxygen: a case series and review of the literature“. Clinical Toxicology. 48 (6): 533–538. doi:10.3109/15563650.2010.492526. PMID 20575671. S2CID 25148041. Архивирано од изворникот 4 January 2022. Посетено на 4 January 2022.
- ↑ „Heeresversuchsstelle Kummersdorf“. UrbEx | Forgotten & Abandoned (англиски). 2008-03-23. Архивирано од изворникот 29 June 2018. Посетено на 2018-06-01.
- ↑ „The Nazi Doctors: Medical Killing and the Psychology of Genocide“. Robert Jay Lifton. Архивирано од изворникот 27 June 2018. Посетено на 26 June 2018.
- ↑ „Explosion and fire in a hydrogen peroxide plant“. ARIA. November 2007. Архивирано од изворникот на 14 February 2022.
- ↑ „Accident No: DCA-99-MZ-001“ (PDF). U.S. National Transportation Safety Board. Архивирано (PDF) од изворникот 3 November 2015. Посетено на 30 October 2015.
- ↑ Mizokami K (28 September 2018). „The True Story of the Russian Kursk Submarine Disaster“. Архивирано од изворникот на 14 February 2022.
- ↑ Wheaton S (16 August 2010). „Bleach Spill Shuts Part of Times Square“. The New York Times. Архивирано од изворникот 1 December 2017. Посетено на 24 February 2017.
Библиографија
- DrabowiczJ, и др. (1994). Capozzi G, и др. (уред.). The Syntheses of Sulphones, Sulphoxides and Cyclic Sulphides. Chichester UK: John Wiley & Sons. стр. 112–6. ISBN 978-0-471-93970-2.
- Greenwood NN, Earnshaw A (1997). Chemistry of the Elements (2. изд.). Oxford UK: Butterworth-Heinemann. A great description of properties & chemistry of H
2O
2. - March J (1992). Advanced Organic Chemistry (4. изд.). New York: Wiley. стр. 723.
- Hess WT (1995). „Hydrogen Peroxide“. Kirk-Othmer Encyclopedia of Chemical Technology. 13 (4. изд.). New York: Wiley. стр. 961–995.
Надворешни врски[уреди | уреди извор]
| „Водород пероксид“ на Ризницата ? |
- Hydrogen Peroxide at The Periodic Table of Videos (University of Nottingham)
- Material Safety Data Sheet
- ATSDR Agency for Toxic Substances and Disease Registry FAQ
- International Chemical Safety Card 0164
- NIOSH Pocket Guide to Chemical Hazards
- Process flow sheet of Hydrogen Peroxide Production by anthrahydroquinone autoxidation
- Hydrogen Peroxide Handbook by Rocketdyne
- IR spectroscopic study J. Phys. Chem.
| ||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||
| ||||||||||||||
|

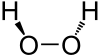



![{\displaystyle {\ce {[NH4]2S2O8 + 2 H2O -> 2 [NH4]HSO4 + H2O2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/540ac1415a894b716e562ad9cae286dae3786482)
![{\displaystyle {\ce {2 [NH4]HSO4 -> [NH4]2S2O8 + H2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/07b33cca8404ebfd6870f015c443c68bb17a3995)









![{\displaystyle {\ce {R-CH2-CH2-CO-SCoA + O2 ->[{\ce {FAD}}] R-CH=CH-CO-SCoA + H2O2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c81784a048a5c7ac9b29e369eaef884fdf03642f)

![{\displaystyle {\ce {H2O2 ->[{\ce {CAT}}] {1/2O2}+ H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/df4f002a0680eb6c0668474a565b44dd6b1f7ff9)