Хлорна киселина

| |
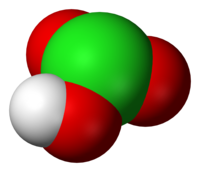
| |
Други називи хлорна(V) киселина | |
| Назнаки | |
|---|---|
| 7790-93-4 | |
| ChemSpider | 18513 |
| EC-број | 232-233-0 |
| |
| 3Д-модел (Jmol) | Слика |
| PubChem | 19654 |
| |
| UNII | Z0V9L75H3K |
| ОН-бр. | 2626 |
| Својства | |
| Хемиска формула | |
| Моларна маса | 0 g mol−1 |
| Изглед | безбоен раствор |
| Густина | 1 г/мл, раствор (прибл.) |
| >40 г/100 мл (20 °C) | |
| Киселост (pKa) | ~ −1 |
| Конјуг. база | хлорат |
| Структура | |
| Геометрија на молекулата | пирамидална |
| Опасност | |
| Безбедност при работа: | |
Главни опасности
|
оксиданс, корозивен |
| GHS-ознаки: | |
Пиктограми
|
 
|
Сигнални зборови
|
Опасност |
Изјави за опасност
|
H271, H314 |
Изјави за претпазливост
|
P210, P220, P221, P260, P264, P280, P283, P301+P330+P331, P303+P361+P353, P304+P340, P305+P351+P338, P306+P360, P310, P321, P363, P370+P378, P371+P380+P375, P405, P501 |
| NFPA 704 | |
| Слични супстанци | |
| Други анјони | бромна киселина јодна киселина |
| Други катјони | амониум хлорат натриум хлорат калиум хлорат |
| Дополнителни податоци | |
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |
| Наводи | |
Хлорна киселина, HClO3 — киселина на хлорот и формален претходник на хлоратните соли. Ова е силна киселина (pKa ≈ −2,7) и оксиданс.
Својства
[уреди | уреди извор]Оваа киселина е термодинамички нестабилна во однос на диспропорционација.
Хлорната киселина е стабилна во студен воден раствор со концентрација од 30 %. Раствор до 40 % може да се добие со внимателно испарување под намален притисок. Во повисоки концентрации растворот се разложува и оддава различни производи, како на пример:
- 8 HClO3 → 4 HClO4 + 2 H2O + 2 Cl2 + 3 O2
- 3 HClO3 → HClO4 + H2O + 2 ClO2
Опасност
[уреди | уреди извор]Оваа киселина е моќен оксиданс. Највеќето органски и запаливи материјали ќе дефларираат при допир.
Добивање
[уреди | уреди извор]Киселината се добива со реакција на сулфурна киселина со бариум хлорат, при што нерастворливиот бариум сулфат се отстранува со таложење:
- Ba(ClO3)2 + H2SO4 → 2 HClO3 + BaSO4
Друг начин е згревање на хипохлореста киселина, што дава хлорна киселина и хлороводород:
- 3 HClO → HClO3 + 2 HCl
Поврзано
[уреди | уреди извор]- Хлорат
- Хипохлореста киселина
- Хлореста киселина
- Перхлорна киселина
- Оксидирачка киселина
- Дихлор пентоксид
Наводи
[уреди | уреди извор]- Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2. изд.). Butterworth-Heinemann. ISBN 0080379419.
- R. Bruce King, уред. (1994). „Chloric acid“. Encyclopedia of Inorganic Chemistry. 2. Chichester: Wiley. стр. 658. ISBN 0-471-93620-0.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

