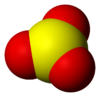
Сулфур триоксид
| |||
Претпочитано име по МСЧПХ: Sulfur trioxide | |||
| Систематско име | Sulfonylideneoxidane | ||
Други називи Sulfuric anhydride | |||
| Назнаки | |||
|---|---|---|---|
| 7446-11-9 | |||
| ChEBI | CHEBI:29384 | ||
| ChemSpider | 23080 | ||
| EC-број | 231-197-3 | ||
| 1448 | |||
| |||
| 3Д-модел (Jmol) | Слика | ||
| PubChem | 24682 22235242 (hemihydrate) 22235243 (monoammoniate) 23035042 (monohydrate) 19427588 (monoformamate) 222852 (monokis(trimethylammoniate)) | ||
| RTECS-бр. | WT4830000 | ||
| |||
| ОН-бр. | UN 1829 | ||
| Својства | |||
| Хемиска формула | |||
| Моларна маса | 0 g mol−1 | ||
| Густина | 1.92 g/cm3, liquid | ||
| Точка на топење | |||
| Точка на вриење | |||
| Reacts to give sulfuric acid | |||
| Термохемија | |||
| Ст. енталпија на формирање ΔfH |
−395.7 kJ/mol | ||
| Стандардна моларна ентропија S |
256.77 J K−1 mol−1 | ||
| Опасност | |||
| NFPA 704 | |||
| Температура на запалување | {{{value}}} | ||
| Смртоносна доза или концентрација: | |||
LC50 (средна концентрација)
|
rat, 4hr 375 mg/m3[се бара извор] | ||
| Слични супстанци | |||
| Други катјони | Селен триоксид Телур триоксид | ||
| Слични sulfur oxides | Сулфур моноксид Сулфур диоксид | ||
| Слични супстанци | Сулфурна киселина | ||
| Дополнителни податоци | |||
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |||
| Наводи | |||
Сулфур триоксид е хемиско соединение со молекулска формула SO3. Во гасовита состојба, ова соединение е значителен загадувач, и е примараен агенс во киселите дождови.[1] Тоа се подготвува во огромни размери како претходник од сулфурна киселина.
Структура и сврзување[уреди | уреди извор]
Гасовитиот SO3 е со триаголна планарна молекуларна D3h симетрија, што е предвидено од страна на VSEPR теоријата. SO3 припаѓа на D3h групата.
Во однос на оксидациската состојба, сулфурниот атом има оксидационен број од +6 и формален полнеж од +3. Луисовата структура се состои од една S=O двојна врска и две S–O единечни врски без утализација на d-орбиталите.[2]} Електричниот диполен момент од гасовитиот сулфур триоксид е нула. Тоа е последица на аголот од 120° помеѓу S-O врските.
Хемиски реакциии[уреди | уреди извор]
SO3 е анхидрид од H2SO4. Така, последователно на тоа е следната реакција:
Реакцијата се случува брзо и е егзотермна, премногу насилно за да се користи во обемно производство. На или под 340 °C, сулфурната киселина, сулфур триоксид, и водата коегзистираат во значителни рамнотежни концентрации.
Сулфур триоксид исти така реагира со сулфур дихлорид при што се добиваат значајни производи, како тионил хлорид.
- SO3 + SCl2 → SOCl2 + SO2
SO3 е силна Луисова киселина лесно формира кристален комплекс со пиридин, диоксан и триметиламин кои може да се користат како сулфонирачки агенси.[3]
Подготовка[уреди | уреди извор]
Сулфур триоксид може да се подготви во лабораторија со пиролиза на натриум бисулфат. Натриум пиросулфат е еден интермедиерен производ:[4]
- Реакција на дехидратација на 315 °C:
- 2 NaHSO4 → Na2S2O7 + H2O
- Cracking at 460 °C:
- Na2S2O7 → Na2SO4 + SO3
Овој метод не е толку корисен бидејќи дава мал принос на другите метални бисулфати, особено за калиумовата сол, зошто слободно го ослободува прво сулфур диоксид, претворајќи го во дикалиум пероксисулфат, додека еквивалентно соединение на натриум е многу нестабилно за да се формира.
Индустриски SO3 е произведен со директен процес. Сулфур диоксид, главно се добива со горење на сулфур или железо пирит (сулфидна руда на железото), претходно прочистена електростатички. Очистениот SO2 се оксидира од атмосферскиот кислород помеѓу 400 and 600 °C со помош на катализатор кој се состои од ванадиум пентаоксид (V2O5) активиран со калиум оксид K2O .Платина е доста ефикасна но е премногу скапа и отровна.
Поголемиот дел на сулфур триоксид добиен на овој начин се претвора во сулфурна киселина не со директно додавање на вода , со што се замаглува, туку со апсорпција на концентрирана сулфурна киселина и разредување со вода од произведеното масло.
Структура на цврст SO3[уреди | уреди извор]
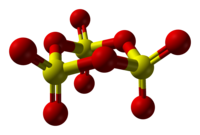
Природата на цврстиот SO3 е изненадувачки сложено подрачје поради структурни промени предизвикани од траги од вода.[5] По кондензација на гасот, апсолутно чист SO3 кондензира во тример, често наречен γ-SO3. Оваа молекулска форма е е безбојно цврста супстанца со точка на топење од 16.8 °C. Усвоената циклична структура се опишува како [S(=O)2(μ-O)]3.[6]
Наводи[уреди | уреди извор]
- ↑ Thomas Loerting, Klaus R. Liedl (2000). „Toward elimination of descrepancies between theory and experiment: The rate constant of the atmospheric conversion of SO3 to H2SO4“. Proceedings of the National Academy of Sciences of the United States of America. 97 (16): 8874–8878. doi:10.1073/pnas.97.16.8874.
- ↑ Terence P. Cunningham , David L. Cooper , Joseph Gerratt , Peter B. Karadakov and Mario Raimondi (1997). „Chemical bonding in oxofluorides of hypercoordinatesulfur“. Journal of the Chemical Society, Faraday Transactions. 93 (13): 2247–2254. doi:10.1039/A700708F.CS1-одржување: повеќе имиња: список на автори (link)
- ↑ Предлошка:Cotton&Wilkinson6th
- ↑ http://doc.utwente.nl/68103/1/Vries69thermal.pdf
- ↑ Holleman, Arnold Frederik; Wiberg, Egon (2001), Wiberg, Nils (уред.), Inorganic Chemistry, Преведено од Eagleson, Mary; Brewer, William, San Diego/Berlin: Academic Press/De Gruyter, ISBN 0-12-352651-5
- ↑ Advanced Inorganic Chemistry by Cotton and Wilkinson, 2nd ed p543
| ||||||||||||||||||||||||||||