Калциум сулфат
| |

| |
Други називи Сулфат од вар | |
| Назнаки | |
|---|---|
| 7778-18-9 10034-76-1 10101-41-4 | |
| ChEBI | CHEBI:31346 CHEBI:32583 |
| ChEMBL | ChEMBL2106140 |
| ChemSpider | 22905 |
| DrugBank | DB15533 |
| EC-број | 231-900-3 |
| 7487 | |
| |
| 3Д-модел (Jmol) | Слика |
| KEGG | C13194 D09201 |
| PubChem | 24928 |
| RTECS-бр. | WS6920000 |
| |
| UNII | E934B3V59H 3RW091J48V 4846Q921YM |
| Својства | |
| Хемиска формула | |
| Моларна маса | 0 g mol−1 |
| Изглед | white solid |
| Мирис | odorless |
| Густина | 2.96 g/cm3 (безводен) 2.32 g/cm3 (дихидрат) |
| Точка на топење | |
| 0.26 g/100ml at 25 °C (дихидрат)[1] | |
| Производ на растворливост, Ksp | 4.93 × 10−5 mol2L−2 (безводен) 3.14 × 10−5 (дихидрат) [2] |
| Растворливост во глицерол | малку растворлив (дихидрат) |
| Киселост (pKa) | 10.4 (anhydrous) 7.3 (дихидрат) |
| -49.7·10−6 cm3/mol | |
| Структура | |
| Кристална структура | ортохомбиски |
| Термохемија | |
| Ст. енталпија на формирање ΔfH |
-1433 kJ/mol[3] |
| Стандардна моларна ентропија S |
107 J·mol−1·K−1 [3] |
| Опасност | |
| NFPA 704 | |
| Температура на запалување | {{{value}}} |
| NIOSH (здравствени граници во САД): | |
PEL (дозволива)
|
TWA 15 mg/m3 (вкупно) TWA 5 mg/m3 (resp) [само за безводна форма][4] |
REL (препорачана)
|
TWA 10 mg/m3 (вкупно) TWA 5 mg/m3 (resp) [само безводен][4] |
IDLH (непосредна опасност)
|
N.D.[4] |
| Безбедносен лист | ICSC 1589 |
| Слични супстанци | |
| Други катјони | Магнезиум сулфат Стронциум сулфат Бариум сулфат |
| Дополнителни податоци | |
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |
| Наводи | |
Калциум сулфат (или калциум сулфат) — неорганско соединение со формулата CaSO4 и сродни хидрати. Во форма на γ- анхидрит (безводна форма), се користи како средство за сушење. Еден посебен хидрат е попознат како париски малтер, а друг природно се јавува како минерален гипс. Има многу намени во индустријата. Сите форми се бели цврсти материи кои се слабо растворливи во вода. [5] Калциум сулфатот предизвикува трајна тврдост во водата.
Хидратациски состојби и кристалографски структури[уреди | уреди извор]
Соединението постои во три нивоа на хидратација што одговараат на различни кристалографски структури и на минерали:
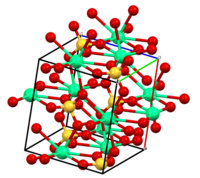
- CaSO4 (анхидрит): безводна состојба. Структурата е поврзана со циркониум ортосиликат (циркон): Ca2+ е 8-координатен, О е 3-координати
- CaSO4·2H2O ((гипс и селенит (минерал)): дихидрат..[6]
- CaSO4·12H2O (басанит): хемихидрат, познат и како гипс од Париз. Понекогаш се разликуваат специфични хемихидрати: α-хемихидрат и β-хемихидрат.[7]
Употреба[уреди | уреди извор]
Главната употреба на калциум сулфат е производство на малтер и штуко. Овие апликации го користат фактот дека калциум сулфатот кој е прашкаст и калциниран формира калапи со хидратација и се стврднува како кристален калциум сулфат дихидрат. Исто така е погоден што калциум сулфатот е слабо растворлив во вода и не се раствора лесно во контакт со вода по неговото зацврстување.
Реакции на хидратација и дехидрација[уреди | уреди извор]
Со разумно загревање, гипсот се претвора во делумно дехидриран минерал наречен басанит или гипс од Париз. Овој материјал ја има формулата CaSO 4 ·( n H 2 O), каде што 0,5 ≤ n ≤ 0,8. [7] Температурите помеѓу 100 и 150 °C (212–302 °F) се потребни за исфрлање на водата во нејзината структура. Деталите за температурата и времето зависат од влажноста на околината. Температурите до 170 °C (338 °F) се користат во индустриско калцинирање, но на овие температури почнува да се формира γ-анхидрит. Топлинската енергија што се доставува до гипсот во ова време (топлината на хидратација) има тенденција да оди во исфрлање на водата (како водена пареа) наместо да ја зголемува температурата на минералот, која полека се зголемува додека водата не исчезне, а потоа се зголемува побрзо. Равенката за делумна дехидрација е:
- CaSO 4 · 2 H 2 O → CaSO 4 ·12 H 2 O +1 12 H 2 O↑
Ендотермичното својство на оваа реакција е релевантно за изведбата на гипскартон, давајќи отпорност на пожар на станбени и други објекти. Во пожар, структурата ќе остане релативно ладна бидејќи водата се губи од гипсот, со што се спречува (или значително забавува) оштетување на рамката (преку согорување на дрвени членови или губење на цврстина на челик при високи температури) и последователен структурен колапс. Но, на повисоки температури, калциум сулфатот ќе ослободи кислород и ќе дејствува како оксидирачки агенс. Ова својство се користи во алуминотермијата. За разлика од повеќето минерали, кои кога се рехидрираат едноставно формираат течни или полутечни пасти, или остануваат прашкаст, калцинираниот гипс има необично својство: кога се меша со вода на нормални (амбиентални) температури, брзо се враќа хемиски во претпочитаната форма на дихидрат. додека физички се „поставува“ за да формира цврста и релативно силна кристална решетка од гипс:
- CaSO 4 ·12 H 2 O +1 12 H 2 O → CaSO 4 · 2 H 2 O
Оваа реакција е егзотермна и е одговорна за леснотијата со која гипсот може да се лее во различни форми, вклучувајќи страни (за гипскартон), стапчиња (за креда) и калапи (за имобилизација на скршени коски или за лиење метал). Измешан со полимери, се користи како цемент за поправка на коските. Мали количества калциниран гипс се додаваат на земјата за да се создадат силни структури директно од лиената земја, алтернатива на кирпичот (кој ја губи својата сила кога е влажен). Условите на дехидрација може да се променат за да се прилагоди порозноста на хемихидратот, што резултира со таканаречените α- и β-хемихидрати (кои се повеќе или помалку хемиски идентични).
На загревање до 180 °C (356 °F), формата речиси без вода, наречена γ-анхидрит (CaSO4 · nH2O каде што се произведува n = 0 до 0,05). γ-анхидритот полека реагира со водата за да се врати во состојба на дихидрат, својство што се користи во некои комерцијални сушени средства. На греење над 250 °C, се формира целосно безводна форма наречена β-анхидрит или „природен“ анхидрит. Природниот анхидрит не реагира со вода, дури и во текот на геолошките временски размери, освен ако не е многу ситно измелен.
Променливиот состав на хемихидратот и γ-анхидритот, и нивната лесна меѓуконверзија, се должи на нивните речиси идентични кристални структури кои содржат „канали“ кои можат да сместат променлива количина на вода или други мали молекули како што е метанолот.
Прехранбената индустрија[уреди | уреди извор]
Калциум сулфат хидрати се користат како коагулант во производи како што е тофу. [8]
За Управата за храна и лекови, тоа е дозволено во сирење и сродни производи од сирење; житно брашно; пекарски производи; замрзнати десерти; вештачки засладувачи за желе и конзерва; зачини зеленчук и некои бонбони. [9]
Тој е познат во серијата Е броеви како E516, а ФАО на ОН го признава како средство за зацврстување, средство за третман на брашно, секвестрант и средство за квасец. [9]
Стоматологија[уреди | уреди извор]
Калциум сулфатот има долга историја на употреба во стоматологијата. [10] Се користи во регенерација на коските како материјал за графт и врзувач на графтот (или продолжувач) и како бариера во регенерација на водена коскено ткиво. Калциум сулфатот е биокомпатибилен материјал и целосно се ресорбира по имплантацијата. [11] Калциум сулфатот создава средина богата со калциум во областа на имплантација. [12]
Други употреби[уреди | уреди извор]

Кога се продава во безводна состојба како средство за сушење со средство кое покажува боја под името Дриерит, се појавува како сино (безводно) или розево (хидрирано) поради импрегнација со кобалт (II) хлорид, кој функционира како индикатор за влага.
До 1970-тите, комерцијални количини на сулфурна киселина се произведувале во Вајтхавен (Кумбрија, Обединето Кралство) од безводен калциум сулфат. Кога се меша со шкрилци или лапор, и се пече, сулфатот ослободува гас сулфур диоксид, претходник во производството на сулфурна киселина, реакцијата исто така произведува калциум силикат, минерална фаза есенцијална во производството на цементен клинкер. [13]
- 2 CaSO 4 + 2 SiO 2 → 2 CaSiO 3 + 2 SO 2 + O 2 [14]
Фабриката правела сулфурна киселина со „Анхидрит Процес“, во кој самиот цементен клинкер бил нуспроизвод. Во овој процес, анхидритот (калциум сулфат) го заменува варовникот во цементната суровина и во услови на редукција, наместо јаглерод диоксид се еволуира сулфур диоксид. Сулфур диоксидот се претвора во сулфурна киселина со процесот на контакт со користење на катализатор на ванадиум пентооксид . [15]
CaSO 4 + 2 C → CaS + 2CO 2
3 CaSO 4 + CaS + 2 SiO 2 → 2 Ca 2 SiO 4 ( белит ) + 4 SO 2
3 CaSO 4 + CaS → 4 CaO + 4 SO 2
Ca 2 SiO 4 + CaO → Ca 3 OSiO 4 (алит)
2 SO 2 + O 2 → 2 SO 3 (во присуство на катализатор ванадиум пентооксид)
SO 3 + H2O → H 2 SO 4 [16]
Поради неговата зголемена употреба на пазарот, фабриката во Вајтхавен продолжила да се шири на начин што не го споделуваат другите погони за анхидрит процес. Рудникот за анхидрит бил отворен на 1/11/1955 година, а фабриката за киселина започнала на 14/11/1955 година. Извесно време во раните 1970-ти, таа станала најголемата фабрика за сулфурна киселина во Обединетото Кралство, правејќи околу 13% од националното производство и била убедливо најголемата фабрика за процес на анхидрит некогаш изградена. [17]
Производство и појава[уреди | уреди извор]
Главните извори на калциум сулфат се природен гипс и анхидрит, кои се појавуваат на многу локации во светот како евапорит. Тие може да се извлечат со вадење на отворен камен или со длабоко ископување. Светското производство на природен гипс е околу 127 милиони тони годишно. [18]
Покрај природните извори, калциум сулфатот се произведува како нуспроизвод во голем број процеси:
- При десулфуризација на димни гасови, издувните гасови од електраните на фосилни горива и други процеси (на пр. производство на цемент) се чистат за да се намали нивната содржина на сулфур оксид, со инјектирање фино мелен варовник: [19]
- SO
2 + 0.5 O
2 + CaCO
3 → CaSO
4 + CO
2
Сродните методи за заробување на сулфур користат вар, а некои произведуваат нечист калциум сулфит, кој при складирање оксидира до калциум сулфат.
- Во производството на фосфорна киселина од фосфатна карпа, калциум фосфатот се третира со сулфурна киселина и калциум сулфат преципитати. Производот, наречен фосфогипс, често е контаминиран со нечистотии, што ја прави неговата употреба неекономична.
- Во производството на водород флуорид, калциум флуоридот се третира со сулфурна киселина, со што се таложи калциум сулфат.
- При рафинирање на цинк, растворите на цинк сулфат се третираат со хидрирана вар за да се ко-таложат тешки метали како бариум.
- Калциум сулфатот, исто така, може да се обнови и повторно да се користи од остатоците од гипс картон на градилиштата.
Овие процеси на таложење имаат тенденција да концентрираат радиоактивни елементи во производот на калциум сулфат. Ова прашање е особено со нуспроизводот на фосфатот, бидејќи фосфатните руди природно содржат ураниум и неговите производи на распаѓање како што се радиум-226, олово-210 и полониум-210. Екстракцијата на ураниум од руди на фосфор може да биде економична само по себе во зависност од цените на пазарот на ураниум или одвојувањето на ураниумот може да биде наложено со законодавството за животна средина и неговата продажба се користи за враќање на дел од трошоците на процесот. [20] [21] [22]
Калциум сулфатот е исто така честа компонента на валканите наслаги во индустриските разменувачи на топлина, бидејќи неговата растворливост се намалува со зголемување на температурата.
Ретроградна растворливост[уреди | уреди извор]
Распуштањето на различните кристални фази на калциум сулфат во вода е егзотермично и ослободува топлина (намалување на Енталпијата: ΔH <0). Како непосредна последица, за да продолжи, реакцијата на растворање треба да ја евакуира оваа топлина што може да се смета како производ на реакцијата. Ако системот се излади, рамнотежата на растворање ќе еволуира надесно според принципот на Ле Шателје и Браун и калциум сулфатот полесно ќе се раствори. Така, растворливоста на калциум сулфатот се зголемува со намалување на температурата и обратно. Ако температурата на системот е зголемена, топлината на реакцијата не може да се распадне и рамнотежата ќе се повлече налево според Ле Шателје и Браун. Растворливоста на калциум сулфатот се намалува со зголемување на температурата. Ова контраинтуитивно однесување на растворливост се нарекува ретроградна растворливост. Поретко е отколку кај повеќето соли чија реакција на растворање е ендотермична (т.е. реакцијата троши топлина: зголемување на енталпијата : ΔH > 0) и чија растворливост се зголемува со температурата. Друго соединение на калциум, калциум хидроксид (Ca(OH) 2, портландит ) исто така покажува ретроградна растворливост од истата термодинамичка причина: бидејќи неговата реакција на растворање е исто така егзотермна и ослободува топлина. Значи, за да се раствори максималната количина на калциум сулфат или калциум хидроксид во вода, потребно е растворот да се излади блиску до неговата точка на замрзнување наместо да се зголеми неговата температура.

Ретроградната растворливост на калциум сулфат е исто така одговорна за неговото таложење во најжешката зона на системите за греење и за неговиот придонес во формирањето на бигор во котлите заедно со талогот на калциум карбонат чија растворливост, исто така, се намалува кога CO 2 се ослободува од топла вода или може избега надвор од системот.
На Марс[уреди | уреди извор]
Наодите од 2011 година на роверот <i id="mwATY">Opportunity</i> на планетата Марс покажуваат форма на калциум сулфат на површината. Сликите сугерираат дека минералот е гипс. [23]
Наводи[уреди | уреди извор]
- ↑ Lebedev, A. L.; Kosorukov, V. L. (2017). „Gypsum Solubility in Water at 25°C“ (PDF). Geochemistry International. 55 (2): 171–177. doi:10.1134/S0016702917010062. S2CID 132916752.
- ↑ D.R. Linde (ed.) "CRC Handbook of Chemistry and Physics", 83rd Edition, CRC Press, 2002
- ↑ 3,0 3,1 Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. стр. A21. ISBN 978-0-618-94690-7.
- ↑ 4,0 4,1 4,2 „Џебен водич за опасните хемиски материи #0095“. Национален институт за безбедност и здравје при работа (NIOSH). (англиски)
- ↑ Franz Wirsching "Calcium Sulfate" in Ullmann's Encyclopedia of Industrial Chemistry, 2012 Wiley-VCH, Weinheim. doi:10.1002/14356007.a04_555
- ↑ Cole, W.F.; Lancucki, C.J. (1974). „A refinement of the crystal structure of gypsum CaSO4·2H2O“. Acta Crystallographica Section B. 30 (4): 921. doi:10.1107/S0567740874004055.
- ↑ 7,0 7,1 Taylor H.F.W. (1990) Cement Chemistry.
- ↑ „About tofu coagulant“. www.soymilkmaker.com. Sanlinx Inc. 31 August 2015. Архивирано од изворникот на 2015-03-14. Посетено на 2023-02-27.
- ↑ 9,0 9,1 „Compound Summary for CID 24497 - Calcium Sulfate“. PubChem.
- ↑ Titus, Harry W.; McNally, Edmund; Hilberg, Frank C. (1933-01-01). „Effect of Calcium Carbonate and Calcium Sulphate on Bone Development“. Poultry Science (англиски). 12 (1): 5–8. doi:10.3382/ps.0120005. ISSN 0032-5791.
- ↑ Thomas, Mark V.; Puleo, David A.; Al-Sabbagh, Mohanad (2005). „Calcium sulfate: a review“. Journal of Long-Term Effects of Medical Implants. 15 (6): 599–607. doi:10.1615/jlongtermeffmedimplants.v15.i6.30. ISSN 1050-6934. PMID 16393128.
- ↑ „Biphasic Calcium Sulfate - Overview“. Augma Biomaterials. 2020-03-25. Посетено на 2020-07-16.
- ↑ Whitehaven Coast Archeological Survey
- ↑ COMMONWEALTH OF AUSTRALIA.
- ↑ Whitehaven anhydrate process
- ↑ Whitehaven anhydrate process
- ↑ website cement kilns whitehaven[мртва врска]
- ↑ Gypsum, USGS, 2008
- ↑ Speight, James G. (2000). „Fuels, Synthetic, Gaseous Fuels“. Kirk‐Othmer Encyclopedia of Chemical Technology. doi:10.1002/0471238961.0701190519160509.a01. ISBN 9780471484943.
- ↑ Wang, R. D.; Field, L. A.; Gillet d'Auriac, F. S. „Recovery of uranium from phosphate rocks“. OSTI 6654998.
- ↑ „Uranium from Phosphates | Phosphorite Uranium - World Nuclear Association“.
- ↑ „Brazil plans uranium-phosphate extraction plant in Santa Quitéria : Uranium & Fuel - World Nuclear News“.
- ↑ „NASA Mars Opportunity rover finds mineral vein deposited by water“. NASA Jet Propulsion Laboratory. December 7, 2011. Посетено на April 23, 2013.
Надворешни врски[уреди | уреди извор]
| ||||||||||||
| ||||||||||||||||||||||||||||
|

