Гас

Гас или плин[1] — една од четирите фундаментални состојби на материјата (другите се цврста, течна и плазма). Чистиот гас може да биде составен од поединечни атоми (на пр. благороден гас како неон), елементарни молекули направени од еден тип на (на пр. кислород), или соединение молекули направени од различни атоми (на пр. јаглерод диоксид). Гас мешавината би содржела голем број на чисти гасови кои се многу слични на воздухот. Она што го разликува гасот од течноста и цврстите материи е огромната поделба на одделните честички на гас. Оваа поделба обично го прави гасот безбоен е невидлива за човечкото око. Интеракцијата на честичките на гасот во присуство на електрични и гравитациски полиња се смета за занемарлива, како што е наведено од страна на постојаната брзина на векторите претставени на сликата. Еден тип на попознат гас е пареата.
Гасовитата состојба на материјата се наоѓа помеѓу течна и плазма состојба,[2] последната кој ја овозможува горната граница за температурата во гасови. Одблеснува долниот крај на скалата за температура лежат изродувачки квантни гасови[3] со која се добива зголемување на внимание.[4]
Се смета дека фламанскиот лекар и хемичар Јан Баптиста фан Хелмонт (1580-1644) е првиот кој го употребил изразот „гас“.[5]
Елементарни(основни) гасови[уреди | уреди извор]
На само хемиски елементи кои се стабилни мулти атом еднојадрени молекули на нормална температура и притисок (STP), се водород (H2), азот (N2) и кислород (O2); плус две халгогени, флуор (F2) и хлор (Cl2). Овие гасови, кога се групираат заедно со едноатомен благородни гасови; кои се хелиум (He), неон (Ne), аргон (Ar), криптон (Kr), ксенон (Xe) и радон (Rn) ; се нарекуваат "елементарни гасови". Алтернативно, тие се понекогаш познати како "молекуларни гасови" за да се разликуваат од молекули кои се исто така хемиски соединенија.
Потекло на поимот[уреди | уреди извор]
Зборот гас е неологизам првпат употребен во раниот 17 век од страна на фламански хемичар J.B. van Helmont.[6] Зборот на Ван Хелмонт се чини дека бил само фонетска транскрипција на грчкиот збор χάος хаос – g во холандскиот се изговара како х во "лох" – во случај кој Ван Хелмонт кој ја следи воспоставената алхемиска употреба потврдена прва во делата на Парацелзиус. Според терминологијата на Парацелузус, хаос значи нешто како "ултра-ретка вода".[7]
Алтернативна приказна [8] е тој збор на Ван Хелмонт оштетен gahst (или geist), што значи дух или дух (душа). Ова е поради тоа што одредени гасови биле предложени со натприродно потекло, како и нивна способност да предизвикаат смрт, да го изгаснат огнот, и да се случи "мини, дното на бунари, црковни и други осамени места ".
Физички одлики[уреди | уреди извор]

Бидејќи повеќето гасови тешко се набљудуваат директно, тие се опишани преку употреба на четири физички својства или макроскопски одлики: притисок, волумен, број на честички (хемичарите ги групираат според молови) и температура. Овие четири одлики беа постојано забележани од страна на Роберт Бојл, Жак Чарлс, Џон Далтон, Џозеф Геј-Лисак и Амадео Авогадро за различни гасови во различни поставувања. Нивните детални студии на крајот доведоа до математички однос меѓу овие својства изразени од страна на закон за идеален гас (види поедноставен модел подолу).
Гас честичките се широко одделени една од друга, а со тоа имаат и послаба меѓумолекулски обврзници од течности и материи. Овие меѓумолекулски сили релултираат од електростатички интеракции помеѓу гас честички. Како наполнети области од различни гас честички repel, додека спротивно наполнети региони од различни гас честички се привлекуваат една со друга; гасовите кои содржат трајно одговорни полнежи јони се познати како плазми. Гасовити соединенија со поларна ковалентна обврзници кои содржат трајно постојано неурамнотежено полнење и искуство со релативно силни меѓумолекулски сили, иако мрежата на молекулата останува со неутрален полнеж. Постојат минливи, случајно предизвикани обвиненија низ неполарни ковалентни врски на молекули и електростатички интеракции предизвикани од нив и се наведени Ван дер Валсови сили. Интеракцијата на овие меѓумолекулски сили варира во рамките на една супстанција која одредува многу од физичките својства карактеристични за секој гас.[9][10] Споредбата на точки на вриење за соединенија гормирани од страна на јонски и ковалентни врски води до овој заклучок.[11] Честички чад лебдат во сликата која обезбедува увид на однесувањето на низок гас притисок. Во споредба со другите состојби на материјата, гасовите имаа ниска густина и вискозност. Притисокот и температурата влијаат на честички во рамките на определен обем. Оваа варијација во поделбата на честички и брзината се нарекува компресибилност. Оваа поделба на честичките и големината влијаат на оптичките својства на гасови што може да се најде во следнава список на индекси на рефракција. Според тоа, гас честичките се рашируваат или дифузираат со цел хомогено да се распоредат целосно во било кој сад.
Макроскопски[уреди | уреди извор]
При набљудување на гас, типично е да се одреди референтна рамка или скала за должина. Поголем размер на должина одговара на макроскопски или гасот од глобална гледна точка. Овој регион (наведен како волумен) мора да биде доволно голем за да собере доволно примероци на гас честички. Како резултат на статистичка анализа на овој примерок за големина може да произведува "просечно" однесување (на пр. Брзина, температура и притисок) на сите гас честички во регионот. Спротивно на тоа, помал обем на должина одговаеа на микроскопски или од глобална гледна точка. Макроскопски, одликите на гас се мери според услови на гас честичките во однос на самите себе (брзина, притисок или темпераатура) или во однос на нивното опкружување (волумен). На пример, Роберт Бојл студирал пневматска хемија на мали делови во текот на својата кариера. Еден од неговите експерименти е поврзан со макроскопски својства на притисок и волумен на гас. Неговиот експеримент е користи Ј-цевка манометар која изгледа како епрувета во облик на буквата Ј. Бојл затворен интертен гас во најблискиот крај на тест епруветата со колона од жива, со што бројот на честички и температурата е константна. Тој забележал дека кога притисокот е зголемен во гас, со додавање на повеќе жива во колона, волуменот на заробениот гас се намалува во обем (ова е познато како обратна врска). Исто така, кога Бојл го помножил притисокот со волуменот на секоја испитуван случај производот бил константен. Овој однос го содржи секој гас што го набљудувал Бојл што води до законот (PV=k), именуван во чест на неговата работа во оваа област. Постојат многу математички алатки достапни за анализа на својства на гас. Како резултат на тоа што гасовите се разгледуваат во отежнати услови, овие алатки се малку посложени, од Ојлер равенки за inviscid проток на Navier–Stokes equations[12] кој е одговорен за вискозни ефекти. Овие равенки се прилагодени на условите во прашање на гасоводниот систем. Лабораториската опрема на Бојл дозволи користење на алгебра за да се добијат неговите аналитички резултати. Неговите резултати се можни, бидејќи тој ги изучил гасовите во ситуации со релативно низок притисок, каде што тие се однесуваат на "идеален" начин. Овие идеални односи, се однесуваат на безбедноста при пресметки за различни услови при летање на материјалите кои се во употреба. Денес се користи опрема со висока технологија која е создадена за да ни помогне при безбедно истражување на повеќе егзотични оперативни средини каде што гасовите не се однесуваат на "идеален" начин. Оваа напредна математика, вклучувајќи ја статистиката и мултиваријабилниот калкулус, овозможува решени за ваквите сложени динамички ситуации како reentry простор на возило. Еден пример е анализа на спејс шатл со повторен влез претставен за да се обезбедат својства на материјалот под овие услови на вчитување кои се соодветни. Во овој режим, гасот веќе не се однесува идеално.
Притисок[уреди | уреди извор]
Симболот се користи за да се претстави притисокот во равенките "p" или "P" со SI-единици на паскали.
Во описот на еден сад со гас, терминот притисок (или апсолутен притисок) се однесува на просечната сила по единица површина на садот. Вклучувајќи го овој волумен, полесно е да се визуелизира гас честички кои се движат по прави линии, додека ти се судрат со садот (види го дијаграмот на врвот на статијата). Силата од страна на честичките во садот со овој судир прави промена динамиката на честичката.[13] За време на судирот се менува брзината само на нормална компонента. Честичка која се движи паралелно до ѕидот не ја менува својата динамика. Затоа, просечната сила на површина треба да биде просечна промена линеарна динамика од сите овие судири на гас честички.
Притисок е збир на сите нормални компоненти на сила притискана од честички кои влијаат на ѕидовите на садот поделени на површината на ѕидот.
Температура[уреди | уреди извор]
Симболот се користи за да ја претстави температурата во равенки е T со SI-единици на келвини.
Брзината на гас честички е пропорционална со неговата апсолутна температура. Обемот на балонот во видеото се намалува кога заробени честички на гас постепено се додаваат на многу студен азот. Температурата на било кој физички систем е поврзана со движењето на честички (молекули и атоми) кои го сочинуваат гас системот.[14] Во статистичката механика, температурата е мерка за средна кинетичка енегрија складирана во честичка. Методите за чување на оваа енергија се диктирани од страна на степени на слобода на самата честичка (начини на енергија). Кинетичката енергија додаде (ендотермен процес) на гас честички по пат на судири произведува линеарно, со вртење и движење со вибрации. Спротивно на тоа, молекула во цврста состојба може да ги зголеми своите вибрирачки режими со додавање на топлина, како структура на решетка, кристално спречува линеарни и вртежни движења. Овие загреани гас молекули имаат поголем опсег на брзина која постојано се менува поради постојани судири со други честички. Опсег на брзината може да се опише со Максвел-Болцман дистрибуција. Употребата на оваа дистрибуција подразбира идеални гасови во близина на термодинамичка рамнотежа на системот на честички кои се засегнати.
Специфичен волумен[уреди | уреди извор]
Симболот се користи за да се претстави специфичен волумен во равенки со "v" со SI-единици метри кубни по килограм.
Симболот се користи за да се претстави волумен во равенки со "V" со SI-единици метри кубни.
При вршење на термодинамичка анализа, тоа е типично кога се зборува за интензивни и обемни својства. Својствата кои зависат од количината на гас (или од маса или волумен) се нарекуваат широки својства, додека својствата кои не зависат од количината на гас се наречени интензивни својства. Специфичен волумен е пример за интензивен простор, бидејќи тоа е односот на обемот кој е окупиран од страна на единица маса за гас кој е идентичен во текот на целиот систем во рамнотежа.[15] 1000 атоми на гас окупираат ист простор како и други 1000 атоми на било која температура и притисок. Овој концепт е полесно да се визуелизира за цврсти материи, како што е железото, кои се iнекомпресибилни во споредба со гасови. Откако ќе се наполни било кој сад со гас, волуменот зафаќа зафаќа широк простор.
Густина[уреди | уреди извор]
Симболот се користи за да се претстави густина во равенка е ρ (ро) со SI-единици на килограми на метар кубен. Овој термин е реципрочен на специфичен волумен.
Откако гас молекулите може слободно да се движат во сад, нивната маса се одликува со густина. Густина е износот на маса по единица волумен на супстанција или инверзија на специфичен волумен. За гасови, густината може да варира во рекор на еден широк опсег поради честичките кои слободно можат да се движат поблиску заедно, ограничени од страна на притисок или волумен. Оваа варијција на густина се нарекува компресибилност. Како притисокот и температурата, густината е менлива состојба на гас и промената на густината во текот на секој процес се регулира со законите на термодинамиката. За статичен гас, густината е иста во текот на целиот сад. Затоа густината е скаларна величина. Тоа може да се прикаже со кинетичка теорија дека густината е обратно пропорционална на големината на садот во кој е ограничена на фиксна маса на гас. Во овој случај на фиксна маса, густината се намалува со зголемување на волуменот.
Микроскопски[уреди | уреди извор]
Ако се набљудува гас под моќен микроскоп, ќе се види колекција на честички (молекули, атоми, јони, електрони итн.), без никаков дефинитивен облик или волумен кои се повеќе или помалку случајни движења. Овие неутрални гас честички ја менуваат својата насока, само кога се судираат со друга честичка или со страните на садот. Во еден идеален гас, овие судири се совршено еластични. Оваа честичка или микроскопски преглед на гас е опишан од страна на кинетичка молекуларна теорија. Претпоставките за оваа теорија може да се најдат во делот на постулатите на кинетичката теорија.
Кинетичка теорија[уреди | уреди извор]
Кинетичка теорија дава увид во макроскопски својства на гасови со оглед на нивниот молекуларен состав и движење. Почнувајќи со дефиниции на интензитет и кинетичка енергија,[16] може да се користи за зачувување на импулсот и геометриски односи на коцка за да се поврзат својствата на макроскопскиот систем на температура и притисок до микроскопско својство на кинетичката енергија на молекулата. Теоријата предвидува просек вредности на овие две својства.
Теоријата исто така објаснува како системот за гас реагира на промени. На пример, како гас се загрева од апсолутна нула, кога тоа е (во теорија) совршено, сепак, неговата внатрешна енергија (температура) се зголемува. Како гаста се загрева, брзината на честичките се забрзува а температурата се зголемува. Ова резултира со поголем број на судири, садот по единица време се должи на повисоки брзини на честички поврзани со покачени температури. Притисокот се зголемува пропорционално со бројот на судири во единица време.
Брауново движење[уреди | уреди извор]

Брауново дрижење е математички модел кој се користи за да се опише случајно движење на честичките суспендирани во течност. Анимацијата на гас честички, со користење на честички со розова и зелена боја, илустрира како ова однесување резултира со ширење на ширење надвор од гасови (ентропија). Овие настани се опишани од страна на теоријата на честички.
Бидејќи тоа е на границата на (или повеќе) со сегашната технологија да ги почитуваат поединечните честички гас (атоми или молекули), само теоретските пресметки даваат предлози за тоа како тие се движат, но нивното движење е различно од брауновото движење, бидејќи брауновото движење вклучува непречено повлекување поради триење на сила на многу гас молекули, испрекинато со насилни судири на молекула поединец (или повеќе) гас (и) со честички. На честички (обично се состојат од милиони или милијарди атоми) со што се движи во остар пат, но не толку остар како што би се очекувало ако се испутува поединечна гас молекула.
Меѓумолекулски сили[уреди | уреди извор]

- Главни статии: ван дер Валсова сила
Како што беше дискутирано порано, моментални атракции (или repulsions) помеѓу честички имаат ефект врз гас динамиката. Во физичка хемија, името дадено на овие сили е меѓумолекулски ван дер Валсови сили. Овие сили играа клучна улога во одредувањето на физичките својства на гас како што е вискозност и проток (види секција физички одлики). Игнорирањето на тие сили во одредени услови (види кинетичка молекуларна теорија) им овозможува вистински гас треба да се третира идеален гас. Оваа претпоставка овозможува користење на закони за идеален гас кои во голема мера ги поедноставува пресметките.
Правилната употреба на овие гас врски бара кинетичка молекуларна теорија (KMT). Кога гас честички имаат магнетно обвинение или Меѓумолекулски сили тие постепено влијаат едни на други, истовремено и растојанието меѓу нив се намалува (модел на водородна врска илустрира еден пример). Во отсуство на било кое кривично обвинение, во одреден момент, кога растојанието помеѓу гас честички е значително намалена и тие не можат повеќе да избегнат судири меѓу себе со нормална температура на гас. Уште еден случај за зголемување на судири меѓу гас честички ќе вклучува фиксниот обем на гасот, кој при загревање ќе содржи многу брзи честички. Ова значи дека овие идеални равенки обезбедуваат солидни резултати, освен за ектремно висок притисок (компримирани) или висока температура (јонизирани) услови. Забележете дека сите овие услови кои се исклучоци дозволуваат пренос на енергија да се одржи во рамките на системот на гас. Отсуството на овие интерни трансфери е она што е наведено во идеални услови со кои размената на енергија се случува само во границите на ситемот. Вистинските гасови доживуваат некои од овие судири и меѓумолекулски сили. Кога овие судири се статистички незначителни (некомпресабилни), резултатите од овие идеални равенки се значајни. Ако гас честички се компресирани во непосредна близина, се однесуваат повеќе како течност (види течна динамика).
Поедноставени модели[уреди | уреди извор]
На равенката на состојба (за гасови) се користи математички модел за да се опише грубо или да се предвиди состојбата на својствата на гасот. Во моментов, не постои единствена равенка на состојба што точно ги предвидува својствата на сите гасови во сите услови. Затоа, голем борј на многу попрецизни равенки на државата се развиени за гасови со специфична температура и притисок кој се движи. На "гас модели" најмногу се дискутира за "совршен гас", "идеален гас" и "вистински гас". Секој од овие модели има свој сет на претпоставки за да се олесни анализата на даден термодинамички систем.[17] Секој следен модел го прошитрува температура спектарот на покривање на што се применува истото.
Идеален и совршен гас модели[уреди | уреди извор]
На равенката на состојба за идеален или совршен гас е закон за идеален гас и гласи: Каде што P е притисок, V е волумен, n е износот на гас (во единица mol), R е универзална гас константа, 8.314 J/(mol K), а T е температура. Напишано на овој начин, тоа понекогаш се нарекува "хемиска верзија", бидејќи го нагласува бројот на молекули n. Исто така може да се запише и како:
каде е специфична постојан гас за одреден гас, во единица J/(kg K), и ρ = m/V е густина. Оваа нотација е верзија на "gas dynamicist's" верзија, која е попрактична за моделирање на гас текови кои вклучуваат забрзување без хемиски реакции.
Идеалниот закон за гас не направи претпоставка за специфична топлина на гас. Во најопшт случај, специфична топлина е функција од температурата и притисокот. Ако зависноста на притисокот е занемарена (а можеби и на температурата) во одредена апликација, понекогаш и на гас може да се каже дека е совршен гас, иако точните претпоставки може да се разликуваат во зависност од авторот и/или областа на науката.
За идеален гас, идеален закон за гас се применува без ограничувања за специфична топлина. Идеален гас е поедноставен "вистински гас" со претпоставка дека факторот на компресибилност Z е поставен на 1, што значи дека оваој пневматски сооднос останува константен. А факторот за компресибилност од нив исто така, бара од четирите водачи на променливи да го счедат закон за идеален гас.
Ова приближување е повеќе погодно за примена во областа на инженерството, иако поедноставни модели моѓе да се користат за да се произведе "топка-парк" опсег за тоа каде лежи реалното решение. Еден пример каде што "приближно идеален гас" ќе биде погоден за внатре во комората за согорување на млазен мотор.[18] Исто така, може да биде корисно задржување на основните хемиски реакции и поделби за пресметка на емисиите.
Вистински гас[уреди | уреди извор]

Секоја една од поставките навадени подолу додава на комплексноста на решение за проблемот. Како што се зголемува густината на гас со зголемување на притисокот, меѓумолекулски сили играат повеќе значајни улоги во однесувањето на гас, што резултира со идеален закон за гас кој не е повеќе обезбедување на "разумни" резултати. На горната граница на опсегот на температура на мотор (на пример, комора за согорување делови – 1300 K), сложени честички гориво апсорбираат внатрешна енергија со помош на ротации и вибрации кои предизвикуваат нивните специфични загревања да се разликуваат од оние на двоатомски молекули и благородните гасови. На повеќе од двојно температура, електронки побудување и дисоцијација на честичките од гасот почнува да се појавува и предизвикува притисокот да се приспособи на поголем број на честички (транзиција од гас наплазма).[19] На крајот, сите термодинамички процеси се претпоставува дека ги опишува униформираните гасоци, чија брзија варира во зависност од фиксна дистрибуција. Со користење на нерамнотежна ситуација која имлицира дека онласта на протокот мора да се одликува на некој начин да им овозможи решение. Еден од првите обиди да ги прошират границите на законот за идеален гас вклучи покривање на различни термодинамички процеси со прилагодување на равенката која следи pVn = константно а потоа менување на n преку различни вредности како што се специфичен однос топлина, γ.
Ефекти на вистинскиот гас вклучувајќи ги оние прилагодувања на сметка на поголем опсег на однесување на гасот:
- Ефекти на компресибилност (Z дозволено е да се движат од 1.0)
- Променлив топлински капацитет (специфични квалификации кои варираат со температура)
- Ван дер Валсови сили (во врска со компресибилност, може да замени други равенки на состојба)
- Нерамнотежни термодинамички ефекти
- Проблеми со молекуларна дисоцијација и основни реакции со променлив состав.
За повеќето апликации, како на детална анализа не е претерано. Примери каде "ефекти на вистински гас" ќе имаат значително влијание би било на Space Shuttle re-entry каде што се присутни екстремно високи температури и притисоци или гасови кои се произведени за време на геолошките настани како сликата на ерупцијата на 1990 година на Mount Redoubt.
Историска синтеза[уреди | уреди извор]
Законот на Бојл[уреди | уреди извор]

Законот на Бојл беше можеби првиот израз на равенката на состојбата. Во 1662 Роберт Бојл изврши серија на експерименти користејќи стаклена туба во Ј-форма, која беше затворена на едниот крај. Меркур е додаден на цевката, задржувајќи фиксна количина на воздух во краток, запечатен крај на цевката. Потоа обемот на гас беше внимателно измерен и дополнително беше додадена жива во цевката. Притисокот на гасот може да се утврди од страна на разликата помеѓу нивото на живата во краткиот крај на цевката и долгиот, отворен крај. Сликата од опремата на Бојл покажува некои од егзотичните алатки кои ги гористел Бојл при неговото истражување на гасови.
Преку овие експерименти, Бојл истакна дека притисокот од гас се одржа во константа температура и варира обратнопропорционално со обемот на гас.[20] На пример, ако обемот е преполовен, притисокот е двојно поголем; и ако обемот е двојно, притисокот е преполовен. Со оглед на обратната врска меѓу притисокот и волуменот, производ на притисок (P) и волумен (V) е константа (k) за дадена маса на ограничен гас сè додека температурата е константна. Изјави како формула, со што е:
Бидејќи пред и по волумени и притисоци на фиксен износ гас, каде што пред и после температурите се еднакви на константата k, тие можат да бидат поврзани со равенката:
Законот на Чарлс[уреди | уреди извор]
Во 1787, францускиот физичар и балон пионер, Жак Чарлс, покажа дека кислород, азот, водород, јаглерод диоксид и воздух се шират до иста мера во однос на истиот интервал од 80 келвини. Тој истакна дека, за идеален гас при константен притисок, обемот е правопропорционален на температурата:
Законот на Геј-Лисак[уреди | уреди извор]
Во 1802 година, Јозеф Луис Геј-Лисак објави резултати на слични, иако посеопфатни експерименти.[21] Геј-Лисак кредитиран од претходната работа на Чари од страна на именување на законот во негова чест. Самиот Геј-Лисак е заслужен за опишување закон за притисок, кој беше пронајден во 1809 година. Притисокот од страните на сад од страна на идеален гас е пропорционален на неговата температура.
Авогадров закон[уреди | уреди извор]
Во 1811 година, Амадео Авогадро потврди дека еднакви волумени на чисти гасови содржат еднаков број на честички. Неговата теорија не била оптшто прифатена до 1858 година, кога друг италијански хемичар Stanislao Cannizzaro беше во можност да се објасни неидеални исклучоци. За својат работа со гасови од еден век претходно, бројот што го носи неговото име Авогадрова константа претставува број на атоми кои се наоѓаат на 12 грама елементарен јаглерод -12 (6.022×1023 mol−1). Оваа специфична бројка на гас честички, при стандардни услови и притисок (закон за идеален гас) зафаќа 22.40 литри, што е наведен како моларен волумен.
Авогадровиот закон наведува дека обемот окупиран од страна на идеален гас е пропорционален на бројот на молови (или молекули) во садот. Ова доведува до моларен волумен на гас, кој во STP е 22.4 dm3 (or litres). Односот е даде со:
каде што n e еднаков на бројот на гас молови (бројот на молекули поделено Авогадров број).
Закон на Далтон[уреди | уреди извор]

Во 1801 година, Џон Далтон објави Закон за парцијални притисоци од неговата работа со закон за врска на идеален гас: Притисокот од мешавина на реактивни гасови не е еднаков на збирот на притисоците на сите составни гасови. Математички, ова може да биде претставено за n видови како што се:
Притисоквкупно = Притисок1 + Притисок2 + ... + Притисокn
Сликата на списанието на Далтон опишува симболи кои се користат како кратенки за снимање на патот што го следат. Меѓу неговите клучни забелешки по мешање нереактивни "еластични течности" (гасови) се следниве:[22]
- За разлика од течности, потешките гасови не се таложат на дното при мешање
- Идентитетот гас честичка не игра никаква улога при одредување на конечен притисок (се однесуваат како нивната големина да е незначителна).
Специјални теми[уреди | уреди извор]
Компресибилност[уреди | уреди извор]

Термодинамиката користи фактор (Z) за да смени равенка за идеален гас во сметка со компресибилни ефекти на вистински гасови. Овој фактор претставува односот на вистински до идеален специфичен волумен. Toј понекогаш е "fudge-factor" или исправка за проширување на корисен спектар на законот за идеален гас при употреба во дизајн. Обично оваа вредност Z е многу блиску до единство. Сликата за фактор на копмперсија покажува колку Z варира во текот на еден спектар на многу ниски температури.
Бројот Рејнолдс[уреди | уреди извор]
Во течната механика, бројот Рејнолдс е односот од инерцијалните сили (vsρ) и густината (μ/L). Таа е една од најважните бездимензионални броеви употребувани во течна динамика, најчесто заедно со други бездимензионални броеви, за да се обезбеди критериум на утврдување на динамиката за сличност. Како таква, бројот Рејнолдс обезбедува врска меѓу резултатите од моделирање (дизајн) и сите други вистински услови. Исто така може да се користи за обележување на протокот.
Вискозност[уреди | уреди извор]

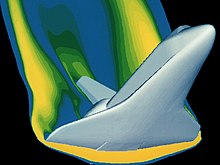
Вискозност, физичко својство, е мерка за тоа колку добро соседните молекули се држат еден до друг. Цвста материја може да издржи сила на сечење поради силата на вакви меѓумолекулски сили. Течност постојано ќе се деформиња кога ќе дојде до слуично оптоварување од друг предмет. Додека гасот има ниска вредност на вискозност од течност, тоа сè уште е забележително својство. Ако гасовите немаа вискозност, тогаш тие не ќе се држеа до површината на страна и ќе формираа граница слој. Една студија на delta wing во Schlieren слика открива дека честичките од гасот се држат еден до друго (види секција слој на граница).
Турбуленција[уреди | уреди извор]

Во течната динамика, турбуленција или турбулентен проток е режим на проток кој се одликува со хаотични, стохастички промени. Ова ги вкличува нискиот интензитет на дифузија, висок интернзитет на струење на воздухот, брза промена на притисокот и брзината во просторот и времето. Погледот од сателит на времето окулу островите на Робинзон Крусо илустрира само еден пример.
Граничен слој[уреди | уреди извор]
Честички, всушност, се "држат" на површината на објектот движејќи се низ него. Овој слој на честички се нарекува граничен слој. На површината на објектот, тоа во суштина е статички и се должи на триење на површината. Објект, со својот граничен слој е всушност нов облик на објектот што остатокот од молекулите што се "гледа" како објектот се приближува. Овој граничен слој може да се оддели од површината, суштински создајќи нова површина и целосно менувајќи ја патеката на проток. Класичен пример на ова е аеродинамичко одолговлекување. Сликата делта крило јасно го покажува граничниот слој на задебелување на гасот кој се влева од десно кон лево по должината на водечките рабови.
Принцип на максимална ентропија[уреди | уреди извор]
Како што вкупниот број степени на слобода ја достигне бесконечноста, системот ќе се најде во макросостојба која одговара на највисоките множества. Со цел да се илустрира овој принцип, да се почитува температурата на кожа од замрзната метална шипка. Користење на топлинска слика на температурата на кожата, имајќи ја предвид температурата на дистрибуција од површината. Ова првично набљудување на температурата претставува "микросостојба." Во иднина, второ набљудување на температурата на кожата ќе ја произведе втората микросостојба. Со продолжување на овој процес на набљудување, тоа е можно ако се произведе една серија на микросостојби кои ќе ја илустрираат топлинската историја на површината на барот. Карактеризација на оваа историска серија на микросостојби е можно со изборот на макросостојба која успешно ги класифиција во една група.
Термодинамичка рамнотежа[уреди | уреди извор]
Кога преносот на енергија престанува од системот, оваа состојба се нарекува термодинамичка рамнотежа. Обично оваа состојба подразбира системот и околината да се на иста температура, така што топлината веќе не се пренесува помеѓу нив. Тоа исто така значи дека надворешните сили се измалансирани (волуменот се менува) и сите хемиски реакции во рамките на системот се конечни. Настаните може да варираат во зависност од системот. Сад со мраз кој е ставен да се топи на собна температура ќе му бидат потребни часови, додека со полупроводници и пренос на топлина што се случува во транзиција на уредот за да се исклучи состојбата може да биде од редот на неколку наносекунди.
Гасот како мотив во популарната култура[уреди | уреди извор]
- „Гас за заспивање“ (англиски: Sleeping Gas) — песна на англиската рок-група The Teardrop Explodes од 1980 година.[23]
- „Гас за смеење“ (англиски: Laughing Gas, Laffing Gas) — американски филм од 1914 година, во режија на Чарли Чаплин.[24]
Поврзано[уреди | уреди извор]
Белешки[уреди | уреди извор]
- ↑ плин — Дигитален речник на македонскиот јазик
- ↑ This early 20th century discussion infers what is regarded as the plasma state. See page 137 of American Chemical Society, Faraday Society, Chemical Society (Great Britain) The Journal of physical chemistry, Volume 11 Cornell (1907).
- ↑ The work by T. Zelevinski provides another link to latest research about Strontium in this new field of study. See Tanya Zelevinsky (2009). „84Sr—just right for forming a Bose-Einstein condensate“. Physics. 2: 94. Bibcode:2009PhyOJ...2...94Z. doi:10.1103/physics.2.94.
- ↑ for links material on the Bose–Einstein condensate see Quantum Gas Microscope Offers Glimpse Of Quirky Ultracold Atoms. ScienceDaily. 4 November 2009.
- ↑ Бојан Шоптрајанов, Хемија за втора година на реформираното гимназиско образование (петто изменето и дополнето издание). Скопје: Просветно дело, 2009, стр. XXXI.
- ↑ J. B. van Helmont, Ortus medicinae. … (Amsterdam, (Netherlands): Louis Elzevir, 1652 (first edition: 1648)). The word "gas" first appears on page 58, where he mentions: "… Gas (meum scil. inventum) …" (… gas (namely, my discovery) …). On page 59, he states: "… in nominis egestate, halitum illum, Gas vocavi, non longe a Chao …" (… in need of a name, I called this vapor "gas", not far from "chaos" …)
- ↑ Harper, Douglas. „gas“. Online Etymology Dictionary.
- ↑ Draper, John William (1861). A textbook on chemistry. New York: Harper and Sons. стр. 178.
- ↑ The authors make the connection between molecular forces of metals and their corresponding physical properties. By extension, this concept would apply to gases as well, though not universally. Cornell (1907) pp. 164–5.
- ↑ One noticeable exception to this physical property connection is conductivity which varies depending on the state of matter (ionic compounds in water) as described by Michael Faraday in the 1833 when he noted that ice does not conduct a current. See page 45 of John Tyndall's Faraday as a Discoverer (1868).
- ↑ John S. Hutchinson (2008). Concept Development Studies in Chemistry. стр. 67.
- ↑ Anderson, p.501
- ↑ J. Clerk Maxwell (1904). Theory of Heat. Mineola: Dover Publications. стр. 319–20. ISBN 0-486-41735-2.
- ↑ See pages 137–8 of Society, Cornell (1907).
- ↑ Kenneth Wark (1977). Thermodynamics (3. изд.). McGraw-Hill. стр. 12. ISBN 0-07-068280-1.
- ↑ For assumptions of Kinetic Theory see McPherson, pp.60–61
- ↑ Anderson, pp. 289–291
- ↑ John, p.205
- ↑ John, pp. 247–56
- ↑ McPherson, pp.52–55
- ↑ McPherson, pp.55–60
- ↑ John P. Millington (1906). John Dalton. стр. 72, 77–78.
- ↑ Discogs, The Teardrop Explodes – Kilimanjaro (пристапено на 12 март 2021)
- ↑ IMDb, Laughing Gas (1914) (пристапено на 7.2.2016)
Наводи[уреди | уреди извор]
- Anderson, John D. (1984). Fundamentals of Aerodynamics. McGraw-Hill Higher Education. ISBN 0-07-001656-9.
- John, James (1984). Gas Dynamics. Allyn and Bacon. ISBN 0-205-08014-6.
- McPherson, William and Henderson, William (1917). An Elementary study of chemistry.CS1-одржување: повеќе имиња: список на автори (link)
| „Гас“ на Ризницата ? |
| ||||||||||||||||||||||||||||||||||||
|









