Митохондриски заболувања
| Митохондриски заболувања | |
|---|---|
| Синоними | Митохондриски болести; митохондриска цитопатија; митохондиопатија |
 | |
| Микрограф покажувајќи парталави црвени влакна, откритие забележано кај различни видови на митохондриски заболувања. Мускулна биопсија. Гомориево трихромско боење. | |
| Специјалност | Медицинска генетика |
Митохондриски заболувања или митохондриски болести ― група на нарушувања предизвикани од митохондриската нефункционалност. Митохондриите се органели кои создаваат енергија за клетката и се наоѓаат во секоја клетка на човечкото тело освен црвените крвни зрнца. Тие ја претвораат енергијата на молекулите од храната во аденозин трифосфат што ги напојува повеќето клеточни функции.
Митохондрските заболувања добиваат уникатни особини и поради начинот на кој болестите често се наследувани и поради тоа што митохондриите се толку критични за функцијата на клетките. Подкласа на овие болести кои имаат невромускулни симптоми се познати како митохондриски миопатии.
Видови[уреди | уреди извор]
Митохондриските заболувања може да се манифестираат на многу различни начини[1] дали кај деца[2] или кај возрасни.[3] Примери на митохондриските болести се:
- Митохондриска миопатија[2][3]
- Наследен од мајката, дијабетес мелитус и глувост[4]
- Додека дијабетесот мелитус и глувоста може да бидат најдено заедно поради други причини, на рана возраст оваа комбинација може да се должи на митохондриска болест, како што може да биде појавена кај Кернс-Сајровиот синдром и Пирсоновиот синдром[2]
- Леберова наследна оптичка невропатија[3]
- Леберовата наследна оптичка невропатија е нарушување на очите кое се одликува со напредно губење на средишниот вид поради дегенерација на оптичките живци и мрежницата (очигледно влијае помеѓу 1 од 30.000 и 1 од 50.000 луѓе[5]); губењето на видот обично започнува во младата зрелост[2]
- Лејов синдром, потакутна некротизирачка енцефаломиелопатија[6]
- Невропатија, атаксија, ретинитис пигментоза и птоза
- напредни симптоми како што е опишано во кратенката
- деменција
- Мионеврогена гастроинтестинална енцефалопатија
- псевдо опструкција на гастроинтестиналниот тракт
- невропатија
- Синдром на миоклонска епилепсија со парталави црвени влакна
- напредна миоклонска епилепсија
- „Парталави црвени влакна“ се купчиња од заболени митохондрии кои се насобираат во подсарколемалниот регион на мускулното влакно и се појавуваат кога мускулите се обоени со изменето Гомориево трихромно боење
- низок раст
- губење на слух
- млечна ацидоза
- нетолеранција на вежбање
- Синдром на митохондриска енцефалопатија, млечна ацидоза и епизоди слични на мозочен удар
- Синдром на исцрпување на митохондриската ДНК
Состојбите како што е Фридрајховата атаксија може да влијаат на митохондриите, но не се поврзани со митохондриските белковини.
Претставување[уреди | уреди извор]
Поврзани услови[уреди | уреди извор]
Стекнати состојби во кои е вклучена митохондриската нефункционалност се:
- дијабетес
- Хантингтонова болест
- рак
- Алцхајмерова болест[7]
- Паркинсонова болест
- биполарно растројство,[8][9][10] шизофренија, стареење,[11] беспокојни нарушувања[12]
- срцеви заболувања
- саркопенија
- синдром на хроничен замор[9]
- амиотрофична латерална склероза[13]
Телото, и секоја мутација, е модулирано од други варијанти на геномот; мутацијата која кај една личност може да предизвика заболување на црниот дроб може кај друга личност да предизвика мозочно нарушување. Тежината на специфичниот дефект исто така може да биде голема или мала. Некои дефекти вклучуваат нетолеранција на вежбање. Дефектите често посериозно влијаат на работата на митохондриите и повеќе ткива, што доведува до повеќесистемски заболувања.[14]
Исто така, објавено е дека клетките на ракот толерантни на лекови имаат зголемен број и големина на митохондрии, што наведува зголемување на митохондриската биогенеза.[15] Интересно, една неодамнешна студија во списанието Nature Nanotechnology, објавила дека клетките на ракот можат да ги заземаат митохондриите од имуните клетки преку физички наноцевки за тунелирање.[16]
Како по правило, митохондриските болести се полоши кога неисправните митохондрии се присутни во мускулите, големиот мозок или живците,[17] бидејќи овие клетки користат повеќе енергија од повеќето други клетки во телото.
Иако митохондриските болести варираат во голема мера во прикажување од личност до личност, дефинирани се неколку главни клинички категории на овие состојби, врз основа на најчестите фенотипски особини, симптоми и знаци поврзани со одредени мутации кои имаат тежнеење да ги предизвикаат.
Исклучително прашање и област на истражување е дали намалувањето на аденозин трифосфатот или реактивните видови кислород се всушност одговорни за забележаните фенотипски последици.[се бара извор]
Понекогаш е пријавено дека се поврзани со церебеларна атрофија или хипоплазија.[18]
Причини[уреди | уреди извор]
Митохондриските нарушувања може да бидат предизвикани од мутации (стекнати или наследни), во митохондриската ДНК или во јадрените гени кои ги кодираат митохондриските компоненти. Тие, исто така, може да бидат резултат на стекната митохондриска нефункционалност поради негативните ефекти на лековите, инфекциите или други причини од животната средина.[19] Оксалатот може да влезе во клетките каде што е познато дека предизвикува митохондриска нефункционалност.[20]
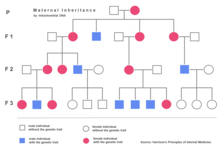
Јадрената ДНК има две копии по клетка (освен сперматозоидите и јајце-клетките), едната копија е наследена од таткото, а другата од мајката. Митохондриската ДНК, сепак, е наследувана само од мајката (со некои исклучоци) и секоја митохондрија обично содржи помеѓу 2 и 10 копии на митохондриска ДНК. За време на клеточната делба, митохондриите се сегрегираат случајно помеѓу двете нови клетки. Тие митохондрии прават повеќе копии, нормално достигнувајќи 500 митохондрии по клетка. Бидејќи митохондриската ДНК се копира кога митохондриите се размножуваат, тие можат да собираат случајни мутации, феномен наречен хетероплазмија. Ако само неколку од копии на митохондриската ДНК наследени од мајката се неисправни, митохондриската поделба може да предизвика повеќето од неисправните копии да завршат само во една од новите митохондрии (за подробни шеми на наследување, видете човечка митохондриска генетика). Митохондриската болест може да стане клинички очигледна штом бројот на зафатени митохондрии ќе достигне одредено ниво; овој феномен е нарекуван „прагово изразување“.
Митохондриите поседуваат многу исти патишта за поправка на ДНК како јадрата - но не сите;[21] затоа, мутациите се случуваат почесто во митохондрискта ДНК отколку во јадрената ДНК (видете статијата Стапка на мутации). Ова значи дека нарушувањата на митохондриската ДНК може да се појават спонтано и релативно често. Дефектите во ензимите кои ја контролираат репликацијата на митохондриската ДНК (од кои сите се кодирани од гените во јадрената ДНК), исто така, може да предизвикаат мутации на митохондриската ДНК.
Повеќето митохондриски функции и биогенеза се контролирани од јадрената ДНК. Човечката митохондриска ДНК кодира 13 белковини од дишевниот ланец, додека повеќето од проценетите 1.500 белковини и компоненти насочени кон митохондриите се јадрено шифрирани. Дефектите во јадрено кодираните митохондрискии гени се поврзани со стотици клинички фенотипови на болести, вклучувајќи анемија, деменција, хипертензија, лимфом, ретинопатија, напади и невро-развојни нарушувања.[22]
Студијата на истражувачите од Универзитетот Јејл (објавена во 12 февруари 2004 година, издание на New England Journal of Medicine) ја истражувала улогата на митохондриите во отпорноста кон инсулин кај потомците на пациентите со дијабетес тип 2.[23] Други студии покажале дека механизмот може да вклучува прекин на постапката на митохондриска сигнализација во телесните клетки ( интрамиоцелуларни липиди). Студијата спроведена во биомедицинскиот истражувачки центар Пенингтон во Батон Руж, Луизијана[24] покажала дека тоа, пак, делумно ги оневозможува гените кои произведуваат митохондрии.
Механизми[уреди | уреди извор]
Ефективната вкупна енергетска единица за достапната телесна енергија е нарекувана дневен капацитет за создавање гликоген,[25][26][27] и е користена за споредување на митохондрискиот излиз на засегнати или хронично осиромашени лица со гликоген со здрави поединци. Оваа вредност бавно е менувама кај даден поединец, бидејќи потребни се помеѓу 18 и 24 месеци за да биде завршен целиот циклус.[26]
Капацитетот за создавање гликоген е целосно зависен и определен од нивоата на работа на митохондриите во сите клетки на човечкото тело;[28] сепак, врската помеѓу енергијата создадена од митохондриите и капацитетот на гликоген е многу лабава и е посредувана од многу биохемиски патишта.[25] Енергетскиот излез на целосна здрава митохондриска функција може да се предвиди точно со сложен теоретски аргумент, но овој аргумент не е јасен, бидејќи најголемиот дел од енергијата е трошен од мозокот и не е лесно да биде измерена.
Дијагноза[уреди | уреди извор]
Митохондриските заболувања обично се откривани со анализа на примероци од мускулите, каде што присуството на овие органели е поголемо. Најчестите тестови за откривање на овие болести се:
- Саутерновиот метод за откривање на големи бришења или удвојувања
- Полимеразна верижна реакција и тестирање на специфична мутација[29]
- Секвенционирање
Третмани[уреди | уреди извор]
Иако истражувањето е во тек, можностите за третман во моментов се ограничени; витамините често се препишувани, иако доказите за нивната ефикасност се ограничени.[30] Пирогроздовата киселина била предложена во 2007 година како можност за третман.[31] N-ацетилцистеин менува многу модели на митохондриска нефункционалност.[32] Во случај на нарушувања на расположението, конкретно биполарно растројство, се претпоставува дека N-ацетилцистеин, ацетил-L-карнитин, S-аденозилметионин, коензим Q10, алфа-липоична киселина, креатин монохидрат и мелатонин може да бидат потенцијални можности за третман.[33]
Генска терапија пред зачнувањето[уреди | уреди извор]
Терапијата за замена на митохондријата, каде што јадрената ДНК е пренесувана во друга здрава јајце-клетка оставајќи ја зад себе неисправната митохондриска ДНК, е процедура за третман на ин витро оплодувањето.[34] Користејќи слична техника на пројадрен пренос, истражувачите од Универзитетот во Њукасл, предводени од Даглас Турнбул, успешно пресадиле здрава ДНК во човечки јајца од жени со митохондриска болест во јајце-клетките на жени даритело кои не биле засегнати.[35][36] Во такви случаи, се поставувани етички прашања во врска со биолошкото мајчинство, бидејќи детето добива гени и генски регулаторни молекули од две различни жени. Користењето генетско инженерство во обидите да бидат добиени бебиња без митохондриски болести е контроверзно во некои кругови и покренува важни етички прашања.[37][38] Машко бебе било родено во Мексико во 2016 година од мајка со Лејов синдром со помош на терапијата за замена на митохондријата.[39]
Во септември 2012 година во Обединетото Кралство било започнато јавно советување за да бидат истражени вклучените етички прашања.[40] Човечкиот генетско инженерство било користен во мал обем за да им биле овозможи на неплодните жени со генетски дефекти во нивните митохондрии, да имаат деца.[41] Во јуни 2013 година, владата на Обединетото Кралство се согласила да развие законска регулатива што ќе ја легализира процедурата на „ин витро оплодувањето од три лица“ како третман за поправање или елиминирање на митохондриските болести кои се пренесуваат од мајка на дете. Постапката може да биде понудена од 29 октомври 2015 година откако ќе бидат воспоставени регулативите.[42][43][44] Зародочното митохондриското пресадување и протофекција се предложени како можен третман за наследна митохондриска болест и алотопско изразување на митохондриските белковини како радикален третман за оптоварување со мутации на митохондриска ДНК.
Во јуни 2018 година, Комитетот за референци за прашања на заедницата на Сенатот на Австралија препорача чекор кон легализирање на терапијата за замена на митохондриите. Истражувањата и клиничките примени на терапијата за замена на митохондриите биле надгледувани со закони донесени од сојузните и сојузнодржавните влади. Сојузнодржавните закони, во најголем дел, биле во согласност со повисокиот сојузен закон. Во сите сојузни држави, законодавството ја забранувала употребата на техники на терапијата за замена на митохондриите во медицината, а освен за Западна Австралија, после истражувањето на ограничен опсег на терапијата за замена на митохондриите, било дозволено до 14-тиот ден од развојот на зародокот, под услов да биде одобрена дозвола. Во 2010 година, почесниот пратеник Марк Батлер, тогаш сојузен министер за душевно здравје и стареење, назначил независен комитет за да ги разгледа двата релевантни закони: Законот за забрана на човечко клонирање за размножување од 2002 година и Законот за истражување на човечки заридоци од 2002 година. Извештајот на Комитетот, објавен во јули 2011 година, препорачал постојното законодавство да остане непроменето
Во моментов, во тек се клинички испитувања врз луѓе на GenSight Biologics (ClinicalTrials.gov # NCT02064569) и на Универзитетот во Мајами (ClinicalTrials.gov # NCT02161380) за да биде испитана безбедноста и ефикасноста на митохондриската генска терапија кај Леберовата наследна оптичка невропатија.
Епидемиологија[уреди | уреди извор]
Околу 1 од 4.000 деца во Соединетите Држави, ќе развијат митохондриска болест на возраст од 10 години. До 4.000 деца годишно во Соединетите Држави, се раѓаат со еден вид митохондриска болест.[45] Бидејќи митохондрските нарушувања содржат многу варијации и подмножества, некои одредени митохондриски нарушувања се многу ретки.
Просечниот број на раѓања годишно кај жените изложени на ризик за пренесување на болеста на митохондриската ДНК, е проценуван на приближно 150 во Обединетото Кралство и 800 во Соединетите Држави.[46]
Историја[уреди | уреди извор]
Првата патогена мутација во митохондриската ДНК била идентификувана во 1988 година; од тоа време до 2016 година, биле идентификувани околу 275 други мутации кои предизвикуваат болест.[47]
Истакнати случаи[уреди | уреди извор]
Истакнати луѓе со митохондриска болест се:
- Мети Степанек, поет, застапник за мир и мотивациски говорник кој имал дисавтономна митохондријална миопатија и кој починал на 13-годишна возраст[48]
- Роко Балдели, тренер и поранешен центар во Главната бејзбол лига, кој морал да се повлече од активното играње на 29-годишна возраст поради митохондриска каналопатија.
- Чарли Гард, британско момче кое имало синдром на осиромашување на митохондриската ДНК; одлуките за неговата грижа биле донесени на различни правни судови.
- Чарлс Дарвин, натуралист од деветнаесеттиот век, кој боледувал од болест со инвалидитет, шпекулирано е дека имал синдром на митохондриска енцефалопатија, млечна ацидоза и епизоди слични на мозочен удар.[49]
Наводи[уреди | уреди извор]
- ↑ „Mitochondrial Diseases“. medlineplus.gov. Посетено на 25 февруари 2024.
- ↑ 2,0 2,1 2,2 2,3 „Mitochondrial disease in children“. Journal of Internal Medicine. 287 (6): 609–633. 2020. doi:10.1111/joim.13054. PMID 32176382.
- ↑ 3,0 3,1 3,2 „Mitochondrial diseases in adults“. Journal of Internal Medicine. 287 (6): 592–608. 2020. doi:10.1111/joim.13064. PMID 32463135.
- ↑ Tsang SH, Aycinena AR, Sharma T (2018). „Mitochondrial disorder: maternally inherited diabetes and deafness“. Atlas of Inherited Retinal Diseases. Advances in Experimental Medicine and Biology. 1085. стр. 163–165. doi:10.1007/978-3-319-95046-4_31. ISBN 978-3-319-95045-7. PMID 30578504.
- ↑ „Current and future landscape in genetic therapies for Leber hereditary optic neuropathy“. Cells. 12 (15): 2013. 2023. doi:10.3390/cells12152013. PMC 10416882 Проверете ја вредноста
|pmc=(help). PMID 37566092 Проверете ја вредноста|pmid=(help). - ↑ Rahman S (2023). „Leigh syndrome“. Mitochondrial Diseases. Handbook of Clinical Neurology. 194. стр. 43–63. doi:10.1016/B978-0-12-821751-1.00015-4. ISBN 9780128217511. PMID 36813320 Проверете ја вредноста
|pmid=(help). - ↑ Abyadeh, Morteza; Gupta, Vivek; Chitranshi, Nitin; Gupta, Veer; Wu, Yunqi; Saks, Danit; WanderWall, Roshana; Fitzhenry, Matthew J; Basavarajappa, Devaraj (2021). „Mitochondrial dysfunction in Alzheimer's disease - a proteomics perspective“. Expert Review of Proteomics. 18 (4): 295–304. doi:10.1080/14789450.2021.1918550. PMID 33874826 Проверете ја вредноста
|pmid=(help). - ↑ Stork, C; Renshaw, P F (2005). „Mitochondrial dysfunction in bipolar disorder: Evidence from magnetic resonance spectroscopy research“. Molecular Psychiatry. 10 (10): 900–19. doi:10.1038/sj.mp.4001711. PMID 16027739.
- ↑ 9,0 9,1 Pieczenik, Steve R; Neustadt, John (2007). „Mitochondrial dysfunction and molecular pathways of disease“. Experimental and Molecular Pathology. 83 (1): 84–92. doi:10.1016/j.yexmp.2006.09.008. PMID 17239370.
- ↑ Nierenberg, Andrew A; Kansky, Christine; Brennan, Brian P; Shelton, Richard C; Perlis, Roy; Iosifescu, Dan V (2012). „Mitochondrial modulators for bipolar disorder: A pathophysiologically informed paradigm for new drug development“. Australian & New Zealand Journal of Psychiatry. 47 (1): 26–42. doi:10.1177/0004867412449303. PMID 22711881.
- ↑ Valiente-Pallejà, A; Tortajada, J; Bulduk, BK (2022). „Comprehensive summary of mitochondrial DNA alterations in the postmortem human brain: A systematic review“. eBioMedicine. 76 (103815): 103815. doi:10.1016/j.ebiom.2022.103815. PMC 8790490 Проверете ја вредноста
|pmc=(help). PMID 35085849 Проверете ја вредноста|pmid=(help). - ↑ Misiewicz, Zuzanna; Iurato, Stella; Kulesskaya, Natalia; Salminen, Laura; Rodrigues, Luis; Maccarrone, Giuseppina; Martins, Jade; Czamara, Darina; Laine, Mikaela A. (26 септември 2019). „Multi-omics analysis identifies mitochondrial pathways associated with anxiety-related behavior“. PLOS Genetics. 15 (9): e1008358. doi:10.1371/journal.pgen.1008358. PMC 6762065. PMID 31557158.
- ↑ Muyderman, H; Chen, T (април 2014). „Mitochondrial dysfunction in amyotrophic lateral sclerosis – a valid pharmacological target?“. British Journal of Pharmacology. 171 (8): 2191–2205. doi:10.1111/bph.12476. PMC 3976630. PMID 24148000.
- ↑ „Mitochondria: in sickness and in health“. Cell. 148 (6): 1145–59. 2012. doi:10.1016/j.cell.2012.02.035. PMC 5381524. PMID 22424226.
- ↑ „Targeting tumor phenotypic plasticity and metabolic remodeling in adaptive cross-drug tolerance“. Science Signaling. 12 (595). август 2019. doi:10.1126/scisignal.aas8779. PMC 7261372. PMID 31431543.CS1-одржување: display-автори (link)
- ↑ „Intercellular nanotubes mediate mitochondrial trafficking between cancer and immune cells“. Nat. Nanotechnol. 17 (1): 98–106. 2021. doi:10.1038/s41565-021-01000-4. PMC 10071558 Проверете ја вредноста
|pmc=(help). PMID 34795441 Проверете ја вредноста|pmid=(help). - ↑ Finsterer, Josef (2007). „Hematological Manifestations of Primary Mitochondrial Disorders“. Acta Haematologica. 118 (2): 88–98. doi:10.1159/000105676. PMID 17637511.
- ↑ Lax, Nichola Zoe; Hepplewhite, Philippa Denis; Reeve, Amy Katherine; Nesbitt, Victoria; McFarland, Robert; Jaros, Evelyn; Taylor, Robert William; Turnbull, Douglass Matthew (2012). „Cerebellar Ataxia in Patients with Mitochondrial DNA Disease“. Journal of Neuropathology & Experimental Neurology. 71 (2): 148–61. doi:10.1097/NEN.0b013e318244477d. PMC 3272439. PMID 22249460.
- ↑ „Mitochondrial diseases“. MeSH. Посетено на 25 февруари 2024.
- ↑ Patel, Mikita; Yarlagadda, Vidhush; Adedoyin, Oreoluwa; Saini, Vikram; Assimos, Dean G.; Holmes, Ross P.; Mitchell, Tanecia (May 2018). „Oxalate induces mitochondrial dysfunction and disrupts redox homeostasis in a human monocyte derived cell line“. Redox Biology. 15: 207–215. doi:10.1016/j.redox.2017.12.003. PMC 5975227. PMID 29272854.
- ↑ „The maintenance of mitochondrial DNA integrity--critical analysis and update“. Cold Spring Harbor Perspectives in Biology. 5 (5): a012641. мај 2013. doi:10.1101/cshperspect.a012641. PMC 3632056. PMID 23637283.
- ↑ „Mapping gene associations in human mitochondria using clinical disease phenotypes“. PLOS Comput Biol. 5 (4): e1000374. 2009. Bibcode:2009PLSCB...5E0374S. doi:10.1371/journal.pcbi.1000374. PMC 2668170. PMID 19390613.
- ↑ Petersen, Kitt Falk; Dufour, Sylvie; Befroy, Douglas; Garcia, Rina; Shulman, Gerald I. (12 февруари 2004). „Impaired Mitochondrial Activity in the Insulin-Resistant Offspring of Patients with Type 2 Diabetes“. New England Journal of Medicine. 350 (7): 664–671. doi:10.1056/NEJMoa031314. PMC 2995502. PMID 14960743.
- ↑ Sparks, Lauren M.; Xie, Hui; Koza, Robert A.; Mynatt, Randall; Hulver, Matthew W.; Bray, George A.; Smith, Steven R. (јули 2005). „A High-Fat Diet Coordinately Downregulates Genes Required for Mitochondrial Oxidative Phosphorylation in Skeletal Muscle“. Diabetes. 54 (7): 1926–1933. doi:10.2337/diabetes.54.7.1926. PMID 15983191. Предлошка:Gale ProQuest 216493144.
- ↑ 25,0 25,1 Mitchell, Peter. „David Keilin's respiratory chain concept and its chemiosmotic consequences“ (PDF). Nobel institute.
- ↑ 26,0 26,1 Michelakis, Evangelos (јануари 2007). „A Mitochondria-K+ Channel Axis Is Suppressed in Cancer and Its Normalization Promotes Apoptosis and Inhibits Cancer Growth“. University of Alberta. University of Alberta, 2007. 11 (1): 37–51. doi:10.1016/j.ccr.2006.10.020. PMID 17222789.
- ↑ Lorini & Ciman, M, & M (1962). „Hypoglycaemic action of Diisopropylammonium salts in experimental diabetes“. Institute of Biochemistry, University of Padua, September 1962. Biochemical Pharmacology. 11 (9): 823–827. doi:10.1016/0006-2952(62)90177-6. PMID 14466716.
- ↑ „Clinical pharmacology and toxicology of dichloroacetate“. Environ. Health Perspect. 106 (Suppl 4): 989–94. 1998. doi:10.1289/ehp.98106s4989. PMC 1533324. PMID 9703483.
- ↑ Bulduk, Bengisu Kevser; Kiliç, Hasan Basri; Bekircan-Kurt, Can Ebru; Haliloğlu, Göknur; Erdem Özdamar, Sevim; Topaloğlu, Haluk; Kocaefe, Y. Çetin (март 2020). „A Novel Amplification-Refractory Mutation System-PCR Strategy to Screen MT-TL1 Pathogenic Variants in Patient Repositories“. Genetic Testing and Molecular Biomarkers. 24 (3): 165–170. doi:10.1089/gtmb.2019.0079. PMID 32167396.
- ↑ „Nutritional cofactor treatment in mitochondrial disorders“. J Am Diet Assoc. 103 (8): 1029–38. 2003. doi:10.1016/S0002-8223(03)00476-0. PMID 12891154.
- ↑ „Therapeutic potential of pyruvate therapy for mitochondrial diseases“. Mitochondrion. 7 (6): 399–401. 2007. doi:10.1016/j.mito.2007.07.002. PMID 17881297.
- ↑ Frantz MC, Wipf P (јуни 2010). „Mitochondria as a target in treatment“. Environ Mol Mutagen. 51 (5): 462–75. Bibcode:2010EnvMM..51..462F. doi:10.1002/em.20554. PMC 2920596. PMID 20175113.
- ↑ „Mitochondrial modulators for bipolar disorder: A pathophysiologically informed paradigm for new drug development“. Australian & New Zealand Journal of Psychiatry. 47 (1): 26–42. 2012. doi:10.1177/0004867412449303. PMID 22711881.
- ↑ „Mitochondrial gene replacement in primate offspring and embryonic stem cells“. Nature. 461 (7262): 367–372. септември 2009. Bibcode:2009Natur.461..367T. doi:10.1038/nature08368. PMC 2774772. PMID 19710649.
- ↑ Boseley, Sarah (2010-04-14). „Scientists reveal gene-swapping technique to thwart inherited diseases“. Guardian. London.
- ↑ Craven, Lyndsey; Tuppen, Helen A.; Greggains, Gareth D.; Harbottle, Stephen J.; Murphy, Julie L.; Cree, Lynsey M.; Murdoch, Alison P.; Chinnery, Patrick F.; Taylor, Robert W. (2010). „Pronuclear transfer in human embryos to prevent transmission of mitochondrial DNA disease“. Nature. 465 (7294): 82–85. Bibcode:2010Natur.465...82C. doi:10.1038/nature08958. PMC 2875160. PMID 20393463.

- ↑ „UK urged to permit IVF procedure to prevent fatal genetic diseases“. The Guardian. London. 2015-04-30.
- ↑ „Three parent baby law is 'irresponsible' says Church of England ahead of vote“. The Telegraph. London. 2015-04-30.
- ↑ Hamzelou, Jessica (2016-09-27). „Exclusive: World's first baby born with new "3 parent" technique“. New Scientist (англиски). Посетено на 25 февруари 2024.
- ↑ Sample, Ian (2012-09-17). „Regulator to consult public over plans for new fertility treatments“. The Guardian. London. Посетено на 25 февруари 2024.
- ↑ „Genetically altered babies born“. BBC News. 2001-05-04. Посетено на 25 февруари 2024.
- ↑ The Human Fertilisation and Embryology (Mitochondrial Donation) Regulations 2015 No. 572
- ↑ „UK government backs three-person IVF“. BBC News. 27 јуни 2013.
- ↑ Knapton, Sarah (1 март 2014) 'Three-parent babies' could be born in Britain next year The Daily Telegraph Science News, Посетено на 25 февруари 2024
- ↑ The Mitochondrial and Metabolic Disease Center
- ↑ Gorman, Gráinne S.; Grady, John P.; Ng, Yi; Schaefer, Andrew M.; McNally, Richard J.; Chinnery, Patrick F.; Yu-Wai-Man, Patrick; Herbert, Mary; Taylor, Robert W. (26 февруари 2015). „Mitochondrial Donation — How Many Women Could Benefit?“. New England Journal of Medicine. 372 (9): 885–887. doi:10.1056/NEJMc1500960. PMC 4481295. PMID 25629662.
- ↑ Claiborne, A.; English, R.; Kahn, J. (2016). „Etiology, Clinical Manifestation, and Diagnosis“. Во Claiborne, Anne; English, Rebecca; Kahn, Jeffrey (уред.). Mitochondrial Replacement Techniques. стр. 37. doi:10.17226/21871. ISBN 978-0-309-38870-2. PMID 27054230.
- ↑ „Young poet, peace advocate Mattie dies | the Spokesman-Review“.
- ↑ Hayman, John (мај 2013). „Charles Darwin's Mitochondria“. Genetics. 194 (1): 21–25. doi:10.1534/genetics.113.151241. PMC 3632469. PMID 23633139.
Надворешни врски[уреди | уреди извор]
| „Митохондриски заболувања“ на Ризницата ? |
- Митохондриски заболувања на Curlie (англиски)
- Меѓународни митохондриски пациенти
| Класификација |
|---|
|
