Бришење (генетика)

Во генетиката, бришење (исто така наречено бришење ген, недостаток или мутација на бришење) (знак: Δ) е мутација (генетска аберација) во која дел од хромозомот или низа од ДНК се изоставени за време на репликацијата на ДНК. Може да биде избришан кој било број на нуклеотиди, од една база до цел дел од хромозомот.[1] Некои хромозоми имаат кревки точки каде се случуваат прекини, што резултира со бришење на дел од хромозомот. Паузите можат да бидат предизвикани од топлина, вируси, зрачење или хемиски реакции. Кога хромозомот се распаѓа, ако дел од него е избришан или изгубен, делот од хромозомот што недостасува е нарекувано бришење или недостаток.[2]
За да биде појавена синапсија помеѓу хромозом со голем интеркаларен недостаток и нормален целосен хомолог, неспарениот регион на нормалниот хомолог мора да излезе од линеарната структура во јамка за бришење или надоместок.
Најмалите мутации на бришење на една база се случуваат со превртување на една база во шаблонската ДНК, проследено со пролизгување на шаблонот на влакното на ДНК, во рамките на активното место на ДНК-полимеразата.[3][4][5]
Бришењето може да биде предизвикано од грешки во хромозомското вкрстување за време на мејозата, што предизвикува неколку сериозни генетски болести. Бришењето што не се јавува во множители на три бази може да предизвика поместување на рамката со менување на рамката за читање на 3-нуклеотидните белковини на генетската низа. Бришењата се присутни кај еукариотските организми, вклучувајќи ги и луѓето, а не кај прокариотските организми, како што се бактериите.
Причини[уреди | уреди извор]
Причините се следниве:
- Загуби од транслокација
- Хромозомски вкрстувања во хромозомска инверзија
- Нерамномерно преминување
- Прекршување без повторно приклучување
Видови[уреди | уреди извор]
Видовите бришења се следниве:
- Терминално бришење - бришење што се случува кон крајот на хромозомот.
- Интеркаларно/интерстицијално бришење – бришење што се јавува од внатрешноста на хромозомот.
- Микробришење – релативно мала количина на бришење (до 5Mb што може да вклучува десетина гени).
Микробришењето обично се наоѓа кај деца со физички абнормалности. Голема количина на бришење би резултирала со непосреден абортус (спонтан абортус).
Номенклатура[уреди | уреди извор]

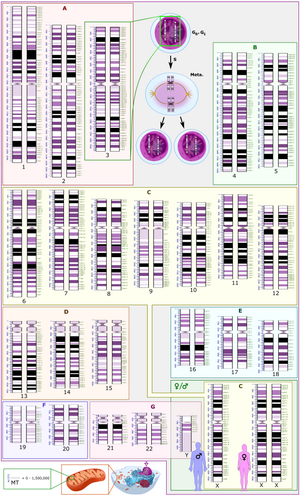
Меѓународниот систем за човечка цитогеномска номенклатура е меѓународен стандард за номенклатура на човечкиот хромозом, кој вклучува имиња на редови, симболи и скратени поими кои се користени во описот на човечкиот хромозом и хромозомските абнормалности. Кратенките вклучуваат минусен знак (−) за бришење на хромозомот и „del“ за бришење на делови од хромозом.[7]
Ефекти[уреди | уреди извор]
Малите бришења се со помала веројатност да бидат фатални; големите бришења обично се фатални - секогаш постојат варијации врз основа на кои гените се губени. Некои бришења со средна големина доведуваат до препознатливи човечки нарушувања, на пр. Вилијамсов синдром.
Бришењето на одреден број парови кои не се рамномерно деливи со три ќе доведе до мутација на поместување на рамката, предизвикувајќи сите кодони што се случуваат по бришењето да бидат погрешно прочитани за време на преводот, создавајќи сериозно изменета и потенцијално нефункционална белковина. Спротивно на тоа, бришењето кое е рамномерно деливо со три е нарекувано бришење „во рамка“.[8]
Бришењето се одговорни за низа генетски нарушувања, вклучувајќи некои случаи на машка неплодност, две третини од случаите на Дишенова мускулна дистрофија,[1] и две третини од случаите на цистична фиброза (оние предизвикани од ΔF508).[9] Бришењето на дел од краткиот крак на хромозомот 5 резултира со синдромот на мачкин плач.[1] Бришењето во генот за кодирање на преживувањето на моторниот неврон предизвикува 'рбетна мускулна атрофија, најчеста генетска причина за смрт на доенчиња.
Микробришењата се поврзани со многу различни состојби, вклучително и Ангелмановиот синдром, Прадер-Вилиевиот синдром и Диџорџовиот синдром.[10] Некои синдроми, вклучително и Ангелмановиот синдром и Прадер-Вилиевиот синдром, се поврзани и со микробришења и со геномско втиснување, што значи дека истото микробришење може да предизвика два различни синдроми во зависност од тоа од кој родител доаѓа бришењето.[11]
Неодамнешната работа наведува дека некои бришења на високо зачувани низи може да бидат одговорни за еволутивните разлики присутни меѓу тесно сродните видови. Ваквите бришења кај луѓето, наречени човечки зачувани бришења, може да бидат одговорни за анатомските и однесувачките разлики помеѓу луѓето, шимпанзата и другите врсти цицачи како човеколиките мајмуни или мајмуните.[12]
Неодамнешната сеопфатна класификација на ниво на пациент и квантификација на настаните на двигателите во групите TCGA, открила дека во просек има 12 двигателски настани по тумор, од кои 2,1 се бришења на туморски сузбивачи.[13]
Откривање[уреди | уреди извор]
Воведувањето на молекуларни техники во врска со класичните цитогенетски методи во последниве години значително го подобрила дијагностичкиот потенцијал за хромозомски абнормалности. Конкретно, споредбената геномска хибридизација со микронизи заснована на употреба на клонови на бактериски вештачки хромозоми, ветува чувствителна стратегија за откривање на промени во бројот на копии на ДНК на ниво на геном. Резолуцијата на откривањето може да биде висока до 30.000 „редови“ и големината на откриеното бришење на хромозомите може да биде мала од 5-20 kb во должина.[14] Други сметачки методи биле избирани за да бидат откриени грешки при бришење во секвенционирањето на ДНК, како што е профилирањето на крајната низа.[15][16]
Бришење на митохондриската ДНК[уреди | уреди извор]
Во квасецот Saccharomyces cerevisiae, јадрените гени Rad51p, Rad52p и Rad59p кодираат белковини кои се неопходни за рекомбинациско поправка и се користени во поправка на прекини на двојни влакна во митохондриската ДНК.[17] Губењето на овие белковини ја намалува стапката на спонтано бришење на ДНК во митохондриите.[17] Ова откритие дава знак дека поправката на прекините на ДНК со двојни влакна со хомологна рекомбинација е чекор во образувањето на бришења на митохондриската ДНК.
Поврзано[уреди | уреди извор]
- Вметнување-бришење
- Хромозомски аберации
- Нулти алел
- Список на генетски нарушувања
- Медицинска генетика
- Синдром на микробришење
- Синдром на хромозомско бришење
- Вметнување (генетика)
- Бришење на 10q26
Наводи[уреди | уреди извор]
- ↑ 1,0 1,1 1,2 Lewis, R. (2004). Human Genetics: Concepts and Applications (6. изд.). McGraw Hill. ISBN 978-0072951745.
- ↑ Klug, William S. (2015). Concepts of genetics. Michael R. Cummings, Charlotte A. Spencer, Michael Angelo Palladino (11. изд.). Boston. ISBN 978-0-321-94891-5. OCLC 880404074.
- ↑ Banavali, Nilesh K. (2013). „Partial Base Flipping is Sufficient for Strand Slippage near DNA Duplex Termini“. Journal of the American Chemical Society. 135 (22): 8274–8282. doi:10.1021/ja401573j. PMID 23692220.
- ↑ Banavali, Nilesh K. (2013). „Analyzing the Relationship between Single Base Flipping and Strand Slippage near DNA Duplex Termini“. The Journal of Physical Chemistry B. 117 (46): 14320–14328. doi:10.1021/jp408957c. PMID 24206351.
- ↑ Manjari, Swati R.; Pata, Janice D.; Banavali, Nilesh K. (2014). „Cytosine Unstacking and Strand Slippage at an Insertion–Deletion Mutation Sequence in an Overhang-Containing DNA Duplex“. Biochemistry. 53 (23): 3807–3816. doi:10.1021/bi500189g. PMC 4063443. PMID 24854722.
- ↑ Warrender JD, Moorman AV, Lord P (2019). „A fully computational and reasonable representation for karyotypes“. Bioinformatics. 35 (24): 5264–5270. doi:10.1093/bioinformatics/btz440. PMC 6954653. PMID 31228194.CS1-одржување: повеќе имиња: список на автори (link)
- "This is an Open Access article distributed under the terms of the Creative Commons Attribution License (http://creativecommons.org/licenses/by/4.0/)" - ↑ „ISCN Symbols and Abbreviated Terms“. Coriell Institute for Medical Research. Посетено на 25 февруари 2024.
- ↑ LSDB — Controlled vocabulary terms Архивирано на 6 октомври 2011 г. at The GEN2PHEN Knowledge Centre. Posted Fri, 08/01/2010.
- ↑ Mitchell, Richard Sheppard; Kumar, Vinay; Robbins, Stanley L.; Abbas, Abul K.; Fausto, Nelson (2007). Robbins basic pathology. Saunders/Elsevier. ISBN 978-1-4160-2973-1.
- ↑ Srour, Myriam; Shevell, Michael (2015-01-01), Rosenberg, Roger N.; Pascual, Juan M. (уред.), „Chapter 14 - Global Developmental Delay and Intellectual Disability“, Rosenberg's Molecular and Genetic Basis of Neurological and Psychiatric Disease (Fifth Edition) (англиски), Boston: Academic Press: 151–161, ISBN 978-0-12-410529-4, Посетено на 25 февруари 2024
- ↑ Kalsner, Louisa; Chamberlain, Stormy J. (22 април 2015). „Prader-Willi, Angelman, and 15q11-q13 duplication syndromes“. Pediatric Clinics of North America. 62 (3): 587–606. doi:10.1016/j.pcl.2015.03.004. ISSN 0031-3955. PMC 4449422. PMID 26022164.
- ↑ „Human-specific loss of regulatory DNA and the evolution of human-specific traits“. Nature. 471 (7337): 216–9. март 2011. Bibcode:2011Natur.471..216M. doi:10.1038/nature09774. PMC 3071156. PMID 21390129.
- ↑ Vyatkin, Alexey D.; Otnyukov, Danila V.; Leonov, Sergey V.; Belikov, Aleksey V. (14 јануари 2022). „Comprehensive patient-level classification and quantification of driver events in TCGA PanCanAtlas cohorts“. PLOS Genetics. 18 (1): e1009996. doi:10.1371/journal.pgen.1009996. PMC 8759692 Проверете ја вредноста
|pmc=(help). PMID 35030162 Проверете ја вредноста|pmid=(help). - ↑ Ren, H (May 2005). „BAC-based PCR fragment microarray: high-resolution detection of chromosomal deletion and duplication breakpoints“. Human Mutation. 25 (5): 476–482. doi:10.1002/humu.20164. PMID 15832308.
- ↑ Shmilovici, A.; Ben-Gal, I. (2007). „Using a VOM Model for Reconstructing Potential Coding Regions in EST Sequences“ (PDF). Journal of Computational Statistics. 22 (1): 49–69. doi:10.1007/s00180-007-0021-8. Архивирано од изворникот (PDF) на 2020-05-31. Посетено на 2014-01-10.
- ↑ Volik, S.; Zhao, S.; Chin, K.; Brebner, J. H.; Herndon, D. R.; Tao, Q.; Kowbel, D.; Huang, G.; Lapuk, A. (4 јуни 2003). „End-sequence profiling: Sequence-based analysis of aberrant genomes“. Proceedings of the National Academy of Sciences. 100 (13): 7696–7701. Bibcode:2003PNAS..100.7696V. doi:10.1073/pnas.1232418100. PMC 164650. PMID 12788976.
- ↑ 17,0 17,1 Ivanetich, K. M.; Lucas, S.; Marsh, J. A.; Ziman, M. R.; Katz, I. D.; Bradshaw, J. J. (1978). „Organic compounds. Their interaction with and degradation of hepatic microsomal drug-metabolizing enzymes in vitro“. Drug Metabolism and Disposition: The Biological Fate of Chemicals. 6 (3): 218–225. PMID 26540.
| „Бришење (генетика)“ на Ризницата ? |
