Сулфид
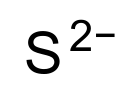
| |
| Систематско име | сулфид(2−)[1] (адитив) |
| Назнаки | |
|---|---|
| 18496-25-8 | |
| ChEBI | CHEBI:15138 |
| ChemSpider | 27079 |
| 3Д-модел (Jmol) | Слика |
| PubChem | 29109 |
| |
| UNII | G15I91XETI |
| Својства | |
| Хемиска формула | |
| Моларна маса | 0 g mol−1 |
| Конјуг. киселина | бисулфид |
| Слични супстанци | |
| Други анјони | оксид селенид телурид |
| Дополнителни податоци | |
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |
| Наводи | |
Сулфид — неоргански анјон на сулфурот со хемиска формула S2− или хемиско соединение кое содржи еден или повеќе јони S2−. Растворите на сулфидните соли се корозивни. Сулфидите се големи семејства на соединенија на неоргански органски соединенија, како на пр. олово сулфидот и диметил сулфидот. Сулфурводородот (H2S) и бисулфидот (SH−) се конјугирани киселини на сулфидот.
Хемиски својства
[уреди | уреди извор]Сулфидниот јон (S2−) не постои во водни алкални раствори раствори на Na2S,[2][3] туку сулфидот се претвора во хидросулфид:
- S2− + H2O → SH− + OH−
При обработка со киселина, сулфидните соли се претвораат во сулфурводород:
- S2− + H+ → SH−
- SH− + H+ → H2S
Оксидацијата на сулфидот е сложен процес. Зависно од условитетаа може да даде елементен сулфур, полисулфиди, политионати, сулфит или сулфат. Металните сулфиди реагираат со халогени, образувајќи сулфур и метални соли.
- 8 MgS + 8 I2 → S8 + 8 MgI2
Метални деривати
[уреди | уреди извор]Водените раствори на преоднометални катјони реагираат со сулфидни извори (H2S, NaHS, Na2S), со што се таложат цврсти сулфиди. Ваквите неоргански сулфиди се слабо растворливи во вода, а многу од нив се сродни на минералите со истиот состав. Еден познат пример е силножолтиот вид CdS или „кадмиумско жолто“. Црните дамки што се појавуваат на сребрени предмети се Ag2S. Таквите видови понекогаш се нарекуваат соли. Сврзувањето на преднометални сулфиди е впрочем мошне ковалентно, што доведува до нивните полуспроводнички својства, кое пак е поврзано со заситените бои. Неколку од нив наоѓаат практична примена како пигменти, во сончеви ќелии и како катализатори. Габата црна кропилка (Aspergillus niger) игра улога во растворливоста на тешкометалните сулфиди.[4]
Геологија
[уреди | уреди извор]- Главната статија за оваа категорија е Сулфидни минерали.
Голем број на важни метални руди се сулфиди.[5] Позначајни примери се: аргентитот (сребро сулфид), цинабаритот (жива сулфид), галенитот (олово сулфид), молибденитот (молибден сулфид), пентландитот (никел сулфид), реалгарот (арсен сулфид), стибнитот (антимон), сфалеритот (цинк сулфид), пиритот (железо дисулфид) и халкопиритот (железо-бакар сулфид).
Корозија предизвикана од сулфиди
[уреди | уреди извор]Растворените слободни сулфиди (H2S, HS− и S2−) предизвикуваат многу агресивна корозија кај бројни метали како челикот, не’рѓосувачкиот челик и бакарот. Сулфидите присутни во воден раствор се одговорни за напрежното напукнување на челикот, наречено и сулфидно напрежно напукнување. Посебни мерки против корозија се посветуваат во индустриските погони кои обработуваат сулфиди: дробилки на сулфидни руди, длабоки нафтени извори, цевководите за сулфуреста нафта и фабриките на натронска хартија.
Корозијата поттикната од микроби или биогени сулфиди е предизвикана од сулфаторедуцирачки бактерии кои произведуваат сулфид што се испушта во воздухот и потоа оксидира во сулфурна киселина под дејство на сулфурооксидирачките бактерии. Биогената сулфурна киселина реагира со фекалии, ги напукнува канализациските цевки до степен на структурно пропаѓање. Овие оштетувања се голем проблем во јавната канализација низ целиот свет.
Оксидацијата на сулфидот може да создаде тиосулфат (S2O2−
3), кој е преоден вид одговорен за тешки проблеми со дупчеста корозија на челикот и не’рѓосувачкиот челик, а сердината исто така се закиселува со производството на сулфурна киселина кога оксидацијата е понапредната.
Органска хемија
[уреди | уреди извор]Во органската хемија, поимот „сулфид“ се однесува на спојот C–S–C, иако поимот тиоетер е поеднозначен. На пример, тиоетерот диметил сулфид е CH3–S–CH3. Полифенилен сулфидот (вид. подолу) ја има емпириската формула C6H4S. Понекогаш под сулфиди се подразбираат молекулите кои ја содржат фунционалната група –SH. На пример, метил сулфид може да значи CH3–SH. Претпочитаниот описник за овие соединенија со SH е тиол или меркаптан, т.е. метантиол или метил меркаптан.
Дисулфиди
[уреди | уреди извор]Поимот „дисулфид“ предизвикуа забуна бидејќи има различни значења. Молибден дисулфидот (MoS2) се состои од раздвоени сулфидни средишта здружен со молибденот во формалната оксидациска состојба +4 (т.е. Mo4+ и два S2−). Од друга страна, железо дисулфидот (пирит, FeS2) се состои од S2−
2, или двоанјонот −S–S− здрижен со двовалентно железо во формалната оксидациска состојба +2 (црно железо: Fe2+). Диметил дисулфидот ја има хемиската врска CH3–S–S–CH3, а пак јаглерод дисулфидот нема врска S–S, туку S=C=S (линеарномолекулен аналог на CO2). Во сулфурната хемија и биохемијата, дисулфид најчесто ѝ се дава на сулфурниот аналог на пероксидната врска –O–O–. Дисулфидната врска (–S–S–) игра важна улога во конформацијата на белковините и во каталитичкото дејство на ензимите.
Примери
[уреди | уреди извор]| Формула | Точка на топење (°C) | Точка на вриење (°C) | CAS-бр. | |
|---|---|---|---|---|
| H2S | Сулфурводородот е многу токсичен и корозивен гас со мирис на расипано јајце. | −85,7 | −60,20 | 7783-06-4 |
| CdS | Кадмиум сулфидот може да се користи кај светлосетилниците. | 1750 | 1306-23-6 | |
| Калциум полисулфидот („сулфурна вар“) е традиционален фунгицид (габосузбивач) во градинарството. | ||||
| CS2 | Јаглерод дисулфидот е претходник на органосулфурни соединенија. | −111,6 | 46 | 75-15-0 |
| PbS | Олово сулфидот се користи кај инфрацрвените сетилници. | 1114 | 1314-87-0 | |
| MoS2 | Молибден дисулфидот, минералниот молибденит, служи како катализатор за отстранување на сулфур од фосилни горива; се користи и како подмачкувач во услови на висока температура и притисок. | 1317-33-5 | ||
| Cl–CH2CH2–S–CH2CH2–Cl | Иперитот е органосулфурно соединение (тиоетер) користен како хемиско оружје во Првата светска војна. | 13–14 | 217 | 505-60-2 |
| Ag2S | Сребро сулфидот е составница на сребреното темнило. | 21548-73-2 | ||
| Na2S | Натриум сулфидот како хидрат се користи во производството на натронска хартија и како претходник на органосулфурни соединенија. | 920 | 1180 | 1313-82-2 |
| ZnS | Цинк сулфидот се користи за леќи и други оптички уреди во инфрацрвениот дел на спектарот. Кога е допиран со сребро се користи кај алфа-забележувачи, а цинк сулфидот со траги од бакар наоѓа примена кај фотолуминесцентните ленти за осветлување во вонредни ситуации и за светлечки сказалки на часовници. | 1185 | 1314-98-3 | |
| C6H4S | Полифенилен сулфидот а полимер наречен „сулфар“. Неговите повторувачки единици се меѓусебно сврзуваат со сулфидни (тиоетерски) споеви. | 26125-40-6 25212-74-2 | ||
| SeS2 | Селен дисулфидот е противгабичен лек кој се користи во препарати против првут. | <100 | 7488-56-4 | |
| FeS2 | Пиритот, наречен и „злато на будалите“, е чест минерал. | 600 | 1317-66-4 |
Добивање
[уреди | уреди извор]Сулфидните соединенија можат да се добијат на неколку различни начини:[6]
- Непосредно здружување на елементи:
- Пример: Fe(ц) + S(ц) → FeS(ц)
- Редукција на сулфат:
- Пример: MgSO4(ц) + 4C(ц) → MgS(ц) + 4CO(г)
- Таложење на нерастворлив сулфид:
- Пример: M2+ + H2S(г) → MS(ц) + 2H+(вр)
Безбедност
[уреди | уреди извор]Многу метални сулфиди се толку нерастворливи во вода што веројатно не се токсични. Некои од нив испуштаат токсичен сулфурводород кога ќе се изложат на силна минерална киселина, вкучувајќи ги желудочните киселини.
Органските сулфиди се многу запаливи. Кога гори, сулфидот го ослободува гасот сулфур диоксид (SO2).
Сулфурводородот, некои од неговите соли и речиси сите органски сулфиди имаат силна скапана миризба; нив ги ослободува биомасата кога гние.
Поврзано
[уреди | уреди извор]- Органски сулфид (тиоетер)
- Сулфидни минерали
Наводи
[уреди | уреди извор]- ↑ „sulfide(2−) (CHEBI:15138)“. Chemical Entities of Biological Interest (ChEBI). UK: European Bioinformatics Institute.
- ↑ May, P.M.; Batka, D.; Hefter, G.; Könignberger, E.; Rowland, D. (2018). „Goodbye to S2-“. Chem. Comm. 54 (16): 1980–1983. doi:10.1039/c8cc00187a. PMID 29404555.
- ↑ Meyer, B; Ward, K; Koshlap, K; Peter, L (1983). „Second dissociation constant of hydrogen sulfide“. Inorganic Chemistry. 22 (16): 2345. doi:10.1021/ic00158a027.
- ↑ Harbhajan Singh (17 ноември 2006). Mycoremediation: Fungal Bioremediation. стр. 509. ISBN 9780470050583.
- ↑ Vaughan, D. J.; Craig, J. R. “Mineral chemistry of metal sulfides" Cambridge University Press, Cambridge: 1978. ISBN 0-521-21489-0.
- ↑ Atkins; Shriver (2010). Inorganic Chemistry (5. изд.). New York: W. H. Freeman & Co. стр. 413.
Надворешни врски
[уреди | уреди извор] Сулфид на Ризницата ?
Сулфид на Ризницата ?- Органски и неоргански сулфиди — Енциклопедија Британика (англиски)
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||
|
