Алуминиум
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Спектрални линии на алуминиумот | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Општи својства | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Име и симбол | алуминиум (Al) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Изглед | металична сребрено-сива | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Алуминиумот во периодниот систем | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомски број | 13 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Стандардна атомска тежина (±) (Ar) | 26,9815385(7)[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Категорија | слаб метал, понекогаш се смета за металоид | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Група и блок | група 13, p-блок | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Периода | III периода | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Електронска конфигурација | [Ne] 3s2 3p1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
по обвивка | 2, 8, 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Физички својства | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Фаза | цврста | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Точка на топење | 933,47 K (660,32 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Точка на вриење | 2.743 K (2.470 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Густина близу с.т. | 2,70 г/см3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| кога е течен, при т.т. | 2,375 г/см3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Топлина на топење | 10,71 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Топлина на испарување | 284 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Моларен топлински капацитет | 24,20 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
парен притисок
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомски својства | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Оксидациони степени | 3, 2,[2] 1[3], −1, −2 (амфотерен оксид) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Електронегативност | Полингова скала: 1,61 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Енергии на јонизација | I: 577,5 kJ/mol II: 1.816,7 kJ/mol II: 2.744,8 kJ/mol (повеќе) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Атомски полупречник | емпириски: 143 пм | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ковалентен полупречник | 121±4 пм | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ван дер Валсов полупречник | 184 пм | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Разни податоци | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Кристална структура | страноцентрирана коцкеста (сцк) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Брзина на звукот тенка прачка | (валуван) 5.000 м/с (при с.т.) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Топлинско ширење | 23,1 µм/(m·K) (при 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Топлинска спроводливост | 237 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Електрична отпорност | 28,2 nΩ·m (при 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Магнетно подредување | парамагнетен[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Модул на растегливост | 70 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Модул на смолкнување | 26 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Модул на збивливост | 76 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Поасонов сооднос | 0,35 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Мосова тврдост | 2,75 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Викерсова тврдост | 160–350 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Бринелова тврдост | 160–550 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS-број | 7429-90-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Историја | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Предвидел | Антоан Лавоазје[5] (1787) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Првпат издвоен | Ханс Кристијан Ерстед[6] (1825) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Именуван од | Хамфри Дејви[5] (1807) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Најстабилни изотопи | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Алуминиум (симб. Al) — хемиски елемент со атомски број 13. Тоj е сребренобел, мек, немагнетен и нодуларен метал во боровата група. По маса, алуминиумот сочинува околу 8% од Земјината кора; тоа е третиот најзастапен елемент по кислородот и силициумот и најзастапен метал во кората, иако е поретко во мантијата подолу. Главната руда од алуминиум е боксит. Алуминиумскиот метал е толку хемиски реактивен што природните примероци се ретки и се ограничени на екстремно редуцирачки средини. Наместо тоа, се наоѓа во комбинација во повеќе од 270 различни минерали.[7]
Алуминиумот е извонреден поради неговата ниска густина и неговата способност да се спротивстави на корозијата преку феноменот на пасивација. Алуминиумот и неговите легури се од витално значење за воздушната индустрија [8] и се важни за транспортните и градежните индустрии, за градење фасади и прозорски рамки. [9] Оксидите и сулфатите се најкорисни соединенија од алуминиум. [8]
И покрај неговата распространетост во животната средина, ниту еден познат облик на живот не користи алуминиумски соли метаболно, но алуминиумот добро е поднесен од страна на растенијата и животните. [10] Поради изобилството на овие соли, потенцијалот за биолошка улога за нив е од постојан интерес, а студиите продолжуваат.
Физички карактеристики[уреди | уреди извор]
Јадра и изотопи[уреди | уреди извор]
Од изотопите од алуминиум, само 27 Al е стабилен. Ова е во согласност со алуминиум кој има непарен атомски број. [б 1] Тој е единствениот алуминиумски изотоп што постоел на Земјата во неговиот сегашен облик од создавањето на планетата. Скоро целиот елемент на Земјата е присутен како овој изотоп, што го прави алуминиумот мононуклиден елемент и значи дека неговата стандардна атомска тежина практично се изедначува со онаа на изотопот. Стандардната атомска тежина на алуминиумот е ниска во споредба со многу други метали, [б 2] која има последици за својствата на елементот.
Сите други изотопи на алуминиумот се радиоактивни. Најстабилен од овие е 26 АЛ (полуживот 720.000 години) и затоа не можел да преживее од формирањето на планетата. Сепак, 26 Al е произведен од аргон во атмосферата со спалувањето предизвикано од протони на космички зраци. Односот од 26 Al до 10 Be се користи за радиодикација на геолошки процеси во текот на 10 5 до 10 6 годишни временски размери, особено транспорт, таложење, складирање на седименти, погребни времиња и ерозија.[12] Повеќето научници за метеоритите веруваат дека енергијата ослободена од распаѓањето на 26 Al е одговорна за топење и диференцијација на некои астероиди по нивното формирање пред 4,55 милијарда години. [13]
Останатите изотопи од алуминиум, со масени броеви кои се движат од 21 до 43, сите имаат полуживот под еден час. Три метастабилни состојби се познати, сите со полуживот под една минута. [11]
Електронска школка[уреди | уреди извор]
Алуминиумскиот атом има 13 електрони, наредени во електронска конфигурација на [ Ne ] 3s 2 3p 1, [14] со три електрони над стабилна конфигурација на благороден гас. Соодветно на тоа, првите три комбинирани енергии на јонизација на алуминиум се далеку пониски од четвртата енергија од јонизација. [15] Алуминиумот релативно лесно може да ги предаде своите три најоддалечените електрони во многу хемиски реакции (види подолу ). Електронегативноста на алуминиумот е 1.61 (Паулинска скала). [16]
Слободниот алуминиумски атом има полупречник од 143 пикометри.[17] Со трите најдлабоки електрони отстранети, полупречникот се намалува на 39 пикометри за 4-координиран атом или 53,5 пикометри за 6-координиран атом. [17] На стандардна температура и притисок, алуминиумските атоми (кога не се засегнати од атомите на други елементи) формираат површински центриран кубичен кристален систем, поврзан со метално сврзување обезбедено од најоддалечените електрони на атомите; оттаму алуминиумот (во овие услови) е метал. Овој кристален систем го делат некои други метали, како олово и бакар ; големината на единицата ќелија од алуминиум е споредлива со онаа на тие други метали. [18]
Масовно[уреди | уреди извор]

Алуминиумскиот метал, кога е во квантитет, е многу сјаен и наликува на сребро, бидејќи повластено апсорбира далеку ултравиолетово зрачење додека ја рефлектира цела видлива светлина, така што не дава никаква боја на рефлектирана светлина, за разлика од рефлектантни спектри на бакар и злато. Друга важна карактеристика на алуминиумот е неговата ниска густина, 2,70 g / cm 3.[19] [б 3] Алуминиумот е релативно мек, издржлив, лесен, пластичен и податлив со изглед кој се движи од сребрена до досадна сива, во зависност од грубоста на површината. Не магнетен е и не може лесно да се запали. Свеж филм од алуминиум служи како добар рефлектор (приближно 92%) од видливата светлина и одличен рефлектор (од прилика 98%) на средно и далеку инфрацрвено зрачење. Јачината на издржливоста на чистиот алуминиум е 7-11 MPa, додека алуминиумските легури имаат јачина на сила која се движи од 200 MPa до 600 MPa. [20] Алуминиумот има околу една третина густина и цврстина на челик. Лесно е обработен, молдиран, извлечен и екструдиран.
Алуминиумските атоми се наредени во површински центриран кубичен кристален систем. Алуминиумот има енергетска-складирана грешка од околу 200 mJ / m 2.[21]
Алуминиумот е добар термички и електричен проводник, кој има 59% спроводливост на бакар, топлински и електрични, додека има само 30% од густината на бакар. Алуминиум е способен за суперспроводливост, со суперспроводлива критична температура од 1,2 Kelvin и критично магнетно поле од околу 100 Гаус (10 milliteslas ).[22] Алуминиумот е најчест материјал за изработка на суперспроводливи кубити.[23]
Хемија[уреди | уреди извор]
Алуминиумската отпорност на корозија може да биде одлична поради тенок површински слој од алуминиум оксид кој се формира кога голиот метал е изложен на воздух, ефикасно спречувајќи понатамошна оксидација,[24] во процес наречен пасивација. Најсилните алуминиумски легури се помалку отпорни на корозија поради галванични реакции со легиран бакар.[25] Оваа отпорност на корозија е значително намалена со водени соли, особено во присуство на различни метали.
Во високо кисели раствори алуминиумот реагира со вода за да формира водород, а во многу алкални за да формираат алуминати - заштитен пасивација под овие услови е занемарлива. Првенствено поради тоа што е кородиран од страна на растворени хлориди, како што е обичниот натриум хлорид, апаратите за домаќинство никогаш не се направени од алуминиум. [26]
Сепак, поради својата општа отпорност на корозија, алуминиумот е еден од ретките метали што ја задржува сребрената рефлексија во фино прашкаст облик, што го прави важна компонента на бои со сребрена боја. Алуминиумското огледало има најголема рефлексија на секој метал во 200-400 nm ( UV ) и 3.000-10.000 nm (далеку IR ) региони; во 400-700 nm видлив опсег, малку е надминат од калај и сребро и во 700-3000 nm (во близина на IR) од сребро, злато и бакар.[27]
Алуминиумот се оксидира со вода на температура под 280°C за да се произведе водород, алуминиум хидроксид и топлина:
- 2 Al + 6 H 2 O → 2 Al (OH) 3 + 3 H 2
Оваа конверзија е од интерес за производство на водород. Сепак, комерцијалната примена на овој факт има предизвици во заобиколувањето на пасивирачкиот оксиден слој, кој ја инхибира реакцијата и во складирање на енергијата потребна за регенерација на алуминиумскиот метал. [28]
Неоргански соединенија[уреди | уреди извор]
Огромното мнозинство на соединенија, вклучувајќи ги сите минерали што содржат алуминиум и сите комерцијално значајни алуминиумски соединенија, имаат алуминиум во оксидационата состојба 3+. Бројот на координати на таквите соединенија варира, но генерално Al 3+ е шест-координата или тетракоординат. Речиси сите соединенија од алуминиум (III) се безбојни. [29]
Сите четири трихалиди се добро познати. За разлика од структурите на трите потешки трихалиди, алуминиум флуорид (AlF 3 ) има шест-координатен Al. Октаедричната координативна средина за AlF 3 е поврзана со компактноста на флуоридниот јон, од кои шест можат да се вклопат околу малиот Al 3+ центар. AlF 3 сублима (со крек) на 1,291 °C (2,356 °F). Со потешки халиди, координативните броеви се пониски. Останатите трихалиди се димерични или полимерни со тетрахерални Ал центри. Овие материјали се подготвуваат со третирање на алуминиумски метал со халоген, иако постојат други методи. Ацидификацијата на оксидите или хидроксидите овозможува настанување на хидрати. Во воден раствор, халогените често формираат мешавини, кои обично содржат шест-координатни алуминиумски центри коишто ги прикажуваат и халидните и акви лиганди. Кога алуминиум и флуорид се заедно во воден раствор, тие лесно формираат комплексни јони како што е [AlF(H2O)5]2+ </br> [AlF(H2O)5]2+ </br> [AlF(H2O)5]2+ </br>, AlF3(H2O)3 </br> AlF3(H2O)3 </br> AlF3(H2O)3 </br> AlF3(H2O)3, и [AlF6]3− </br> [AlF6]3− </br>. Во случај на хлорид, полиалуминиумските кластери се формираат како што е [Al 13 O 4 (OH) 24 (H 2 O) 12 ] 7+.
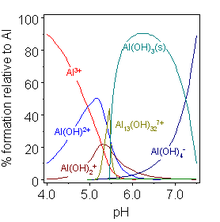
Алуминиумот формира еден стабилен оксид со хемиска формула Al2O3. Тој може да се најде во природата во минералниот корунд.[30] Алуминиум оксид, исто така, честопати се нарекува Алумина.[31] Сафир и рубин се нечисти корунди загадени со траги од други метали. Двата оксидни хидроксиди, AlO (OH), се [./https://en.wikipedia.org/wiki/Boehmite boehmite] и [./https://en.wikipedia.org/wiki/Diaspore diaspore]. Постојат три трихидроксиди: bayerite, gibbsite и nordstrandite, кои се разликуваат во нивната кристална структура (полиморфни ). Повеќето се произведуваат од руди со различни влажни процеси со користење на киселина и база. Греењето на хидроксидите доведува до формирање на корунди. Овие материјали се од централно значење за производство на алуминиум и се исклучително корисни.
Алуминиум карбид (Al4C3) се прави со загревање на мешавина од елементи над 1000°C (1,832 °F). Бледо жолтите кристали се состојат од тетрахерални алуминиумски центри.Тие реагираат со вода или разредена киселина за да се добие метан. Ацетилидот, Al2(C2)3, се прави со пренесување на ацетилен преку загреан алуминиум.
Алуминиум нитрид (AlN) е единствениот нитрид познат по алуминиум. За разлика од оксидите, тој содржи тетрахерални алуминиумски центри. Може да се направи од елементите на 800 °C (1,472 °F). Тој е материјал кој е стабилен на воздух со висока топлинска спроводливост. Алуминиум фосфид (AlP) е направен на сличен начин; се хидролизира за да се добие фосфин :
- Alp + 3 H 2 O → Al (OH) 3 + pH 3
Иако големо мнозинство на алуминиумски соединенија имаат Al 3+ центри, соединенијата со пониски оксидациски состојби се познати и некогаш од значење како претходници на видот Al3+.
Алуминиум (I)[уреди | уреди извор]
AlF, AlCl и AlBr постојат во гасната фаза кога трихалидот се загрева со алуминиум. Составот AlI е нестабилен на собна температура, конвертирајќи се во тријодид: [32]
Стабилен дериват на алуминиум моноиодид е цикличниот адукт формиран со триетиламин, Al4I4(NEt3)4. Исто така, од теоретски интерес, но само на минливо постоење се Al2O и Al2S. Al2O е направен со загревање на нормалниот оксид, Al2O3, со силициум на 1,800 °C (3,272 °F) во вакуум.[33]
Алуминиум (II)[уреди | уреди извор]
Многу едноставни Al (II) соединенија се повикуваат или се забележуваат во реакциите на алуминиум метал со оксиданси. На пример, алуминиум моноксид, AlO, е откриен во гасна фаза по експлозија [34] и во ѕвездени апсорпциони спектри. [35] Потемелно се испитуваат соединенијата со формулата R4Al2 кои содржат Al-Al врска и каде што R е голем органски лиганд.[36]
Органоалуминиеви соединенија и сродни хидриди[уреди | уреди извор]
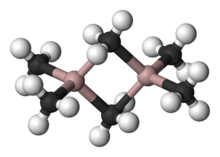
Постојат различни соединенија со емпириска формула AlR 3 и AlR1,5Cl1,5.[37] Овие видови обично се тетраедарни алуминиум центри формирани од димеризацијата со некои R или Cl премостување помеѓу двете Al-атоми, на пример, " триметилалуминиум " ја има формулата Al2(CH3)6 (види слика). Со големи органски групи, триорганоалуминиевите соединенија постојат како трикоординирани мономери, како што се триизобутилалуминиум.Таквите соединенија се користат во индустриската хемија, и покрај фактот што тие често се високопирофорни. Неколку аналози постојат помеѓу органоалуминиеум и органоморони соединенија, освен големи органски групи.
Индустриски важниот алуминиум хидрид е литиум алуминиум хидрид (LiAlH 4 ), кој се користи како редуктор во органската хемија. Може да се произведува од литиум хидрид и алуминиум трихлорид :
- 4 LiH + AlCl3 → LiAlH4 + 3 LiCl
Неколку корисни деривати на LiAlH 4 се познати, на пр. Натриум бис (2-метоксиетокси) дихидридоалуминиат. Наједноставниот хидрид, алуминиум хидрид или ален, останува лабораториска љубопитност. Тоа е полимер со формулата (ALH 3) n, за разлика од соодветниот бор хидрид што е димер со формулата (BH3)2.
Природна појава[уреди | уреди извор]
Во вселената[уреди | уреди извор]
Алуминиумското изобилство на честички во Сончевиот Систем е 3,15 милионитинки. [38] [б 4] Тој е дванаесеттиот елемент најзастапен од сите елементи и трет најзастапен меѓу елементите кои имаат непарни атомски броеви, по водород и азот. [38] Единствениот стабилен изотоп на алуминиум, 27Al, е 18-тото најзастапно јадро во Вселената. Тој е создаден речиси целосно по соединување на јаглерод во масивни ѕвезди кои подоцна ќе станат супернова од тип II: ова соединување создава 26Mg, што, по фаќањето слободни протони и неутрони станува алуминиум. Некои помали количини од 27Al се создаваат во водородни горени школки на еволуираните ѕвезди, каде што 26 Mg може да фаќа слободни протони. [39] Во суштина, целиот алуминиум кој сега постои е 27Al; 26Аl бил присутен во раниот Сончев систем, но во моментов е исчезнат. Сепак, количините на траги од 26 Al што постојат се најчестиот емитер на гама зраци во меѓуѕвездениот гас.[39]
На земјата[уреди | уреди извор]

Генерално, Земјата е околу 1,59% алуминиум по маса (седма во изобилие по маса). [40] Алуминиумот се јавува во поголем процент на Земјата отколку во Универзумот, бидејќи алуминиумот лесно формира оксиди и се врзува за карпи и алуминиумпт останува во Земјината кора, додека помалку реактивните метали тонат до јадрото. [39] Во Земјината кора, алуминиумот е најзастапен (8.3% по маса) метален елемент и третиот најзастапен од сите елементи (по кислород и силициум). [41] Голем број силикати во Земјината кора содржат алуминиум. [42] Спротивно на тоа, мантијата на Земјата е само 2.38% алуминиум по маса. [43]
Поради својот силен афинитет за кислород, алуминиумот речиси никогаш не е пронајден во елементарната состојба; наместо тоа се наоѓа во оксиди или силикати. Feldspars, најчестата група на минерали во Земјината кора, се алумосиликати. Алуминиум, исто така, се јавува во минералите берил, криолит, гранат, шпинел и тиркизна боја.[44] Нечистотиите во Al2O3, како што се хром и железо, ги даваат скапоцените камења рубин и сафир. [45] Мајчин алуминиум метал може да се најде само како мала фаза во ниско ниво на кислородни fugacity средини, како на ентериери на одредени вулкани. [46] Индустрискиот алуминиум е пријавен кај студени седишта во североисточната континентална падина на Јужнокинеското Море. Можно е овие депозити да резултираат од бактериско намалување на тетрахидроксоалуминатот Al(OH)4 -.[47]
Иако алуминиумот е чест и раширен елемент, не сите алуминиумски минерали се економски издржливи извори на метал. Речиси сите метални алуминиум се произведуваат од руди боксит (AlOx(OH)3-2 x ). Бокситот се јавува како производ на атмосферски влијанија од ниско железо и силициум во тропски климатски услови. [48] Во 2017 година, повеќето боксити биле минирани во Австралија, Кина, Гвинеја и Индија. [49]
Историја[уреди | уреди извор]

Историјата на алуминиумот е обликувана со употребата на алум. Првиот напишан запис за алум, направен од грчкиот историчар Херодот, датира од 5 век пр.н.е. [50] Древните го користеле алумот за бојадисување и за одбрана на градот. [50] По Крстоносните војни, алумот бил неопходен напредок во европската индустрија на ткаенини, [51] бил предмет на меѓународна трговија; [52] бил увезен во Европа од источниот Медитеран до средината на XV век. [53]
Природата на алумот останува непозната. Околу 1530 година, швајцарскиот лекар Парацелсус сугерирал дека алумот бил сол на земја од алум. [54] Во 1595 година, германскиот лекар и хемичар Андреас Лививија експериментално го потврдил тоа; [55] Во 1722 година, германскиот хемичар Фридрих Хофман го објавил своето верување дека основата на алумот била посебна земја. [56] Во 1754 година, германскиот хемичар Андреас Сигисмунд Маргграф синтетизирал алумина со варена глина во сулфурна киселина и потоа додавајќи поташа.[56]
Обидите за производство на алуминиумски метал датираат од 1760 година. [57] Првиот успешен обид, бил завршен во 1824 од страна на данскиот физичар и хемичар Ханс Кристиан Орстед. Тој реагирал безводен алуминиум хлорид со калиум амалгам, давајќи грутка метал што изгледа слично на калај. [58] [59] Тој ги презентирал неговите резултати и демонстрирал примерок од новиот метал во 1825 година. [60] [61] Во 1827 година, германскиот хемичар Фридрих Велер ги повторил експериментите на Орстед, но не идентификувал никаков алуминиум. [62] (Причината за оваа недоследност била откриена само во 1921 година.) [63] Во 1827 година тој спровел сличен експеримент со мешање на безводен алуминиум хлорид со калиум и произвел прашок од алуминиум. [59] Во 1845 година, тој успеал да произведе мали парчиња метал и опишал некои физички својства на овој метал. [63] По многу години потоа, Велер бил заслужен за откривање на алуминиум. [64] Бидејќи методот на Велер не можел да даде големи количини на алуминиум, металот остана редок; неговата цена ја надмина онаа на златото. [62]

Францускиот хемичар Анри Етиен, Сент-Клер Девил, објавил индустриски метод за производство на алуминиум во 1854 година во Париската академија на науките.[65] Алуминиум трихлорид можел да биде намален со натриум, што било попогодно и поевтино од калиум, што го користел Велер. [66] Во 1856 година, Девил, заедно со придружниците, го основал првото индустриско производство на алуминиум во светот. [65] Од 1855 до 1859 година, цената на алуминиумот се намалил за големина од 500 до 40 долари за килограм. [67] Дури и тогаш, алуминиумот сè уште не бил од голема чистота и произведениот алуминиум се разликувал по својства по примерок. [68]
Првиот индустриски метод за производство од големи размери бил независно развиен во 1886 година од страна на францускиот инженер Пол Херро и американскиот инженер Чарлс Мартин Хол ; сега е познат како процес на Hall-Héroult. [69] Процесот Hall-Héroult ја претвора алумината во метал. Австрискиот хемичар Карл Џозеф Бајер го открил начинот на прочистување на бокситот за да се добие алумина, сега познат како Бајер процес, во 1889 година. [70] Современото производство на метали од алуминиум се базира на процесите на Баер и Хал-Херол. [71]
Цените на алуминиумот паднаа, а алуминиумот стана широко користен за накит, секојдневни предмети, рамки за очила, оптички инструменти, прибор за на маса и фолија во 1890-тите и почетокот на 20 век. Способноста на алуминиумот да формира тешки, но сепак лесни легури со други метали, придонел металот што многу да се користи во тоа време. [72] За време на Првата светска војна, големите влади барале големи пратки од алуминиум за лесни и јаки авионски рамки. [73]
До средината на 20 век, алуминиумот станал дел од секојдневниот живот и е суштинска компонента на домашни апарати. [74] Во средината на 20-от век, алуминиумот се појавил како градежен материјал, со апликации за градежништво како во основната конструкција, така и во ентериерот, [75] и се повеќе се употребувал во воениот инженеринг, за авиони и за моторни возила со копнен оклоп. [76] првиот вештачки сателит на Земјата, кој бил пуштен во 1957 година, се состоел од две одделни алуминиумски полутопки кои биле здружени заедно и сите последователни вселенски возила се направени од алуминиум. [71] Алуминиумската конзерва била измислена во 1956 година и била употребувана како сад за пијалаци во 1958 година. [77]

Во текот на 20 век, производството на алуминиум брзо се зголемило: додека светското производство на алуминиум во 1900 било 6.800 тони, годишното производство прво надминало 100.000 метрички тони во 1916 година; 1.000.000 тони во 1941 година; 10.000.000 тони во 1971 година. [78] Во 1970-тите, зголемената побарувачка за алуминиум ја направило размена на стоки; алуминиумот влегол во Лондонската берза на метали, најстарата индустриска метална берза во светот, во 1978 година. [71] Производството продолжило да расте: годишното производство на алуминиум надминало 50.000.000 метрички тони во 2013 година. [78]
Вистинската цена наа алуминиумот се намалила од 14.000 долари за метрички тон во 1900 година на 2.340 долари во 1948 година (во 1998 година САД долари). [78] Трошоците за екстракција и обработка биле намалени во однос на технолошкиот напредок и размерот на економиите. Меѓутоа, потребата за искористување на послабите депозити со понизок степен на квалитет и користењето на зголемените трошоци за влез (пред сè, енергија), ја зголемиле нето-цената на алуминиумот; [79] вистинската цена почнала да расте во 1970-тите со зголемувањето на трошоците за енергија. [80] Производството се преселило од индустријализираните земји во земји каде што производството било поевтино. [81] Трошоците за производство во доцните години на 20-от век се промениле поради напредокот во технологијата, пониските цени на енергијата, девизниот курс на американскиот долар и цените на алуминиумот. [82] Збирното учество на земјите на БРИК се зголемило во првата деценија од 21 век од 32,6% на 56,5% во примарното производство и 21,4% на 47,8% во примарната потрошувачка. [83] Кина акумулира особено голем дел од светската продукција благодарение на изобилството на ресурси, евтина енергија и владини стимули; [84] исто така, го зголемила својот удел во потрошувачката од 2% во 1972 година на 40% во 2010 година. [85] Во Соединетите Американски Држави, Западна Европа и Јапонија, повеќето алуминиум се консумирал во транспортот, инженерството, градежништвото и пакувањето. [86]
Алуминиумот во популарната култура[уреди | уреди извор]
- „Алуминиум“ (англиски: Aluminum) — песна на американската рок-група Вајт страјпс (The White Stripes) од 2001 година.[87]
Белешки[уреди | уреди извор]
- ↑ No elements with odd atomic numbers have more than two stable isotopes; even-numbered elements have multiple stable isotopes, with tin (element 50) having the highest number of isotopes of all elements, ten.[11] See Even and odd atomic nuclei for more details.
- ↑ Most other metals have greater standard atomic weights: for instance, that of iron is 55.8; copper 63.5; lead 207.2.
- ↑ Aluminium's low density (compared to the other metals) arises from the fact that its nuclei are much lighter, while difference in the unit cell size does not compensate for this difference.
- ↑ Abundances in the source are listed relative to silicon rather than in per-particle notation. The sum of all elements per 106 parts of silicon is 2.6682×1010 parts; aluminium comprises 8.410×104 parts.
Наводи[уреди | уреди извор]
- ↑ Standard Atomic Weights 2013. Commission on Isotopic Abundances and Atomic Weights
- ↑ алуминиум моноксид
- ↑ алуминиум јодид
- ↑ Lide, D. R. (2000). „Magnetic susceptibility of the elements and inorganic compounds“ (PDF). CRC Handbook of Chemistry and Physics (81st. изд.). CRC Press. ISBN 0849304814.
- ↑ 5,0 5,1 „Aluminum“. Los Alamos National Laboratory. Посетено на 3 March 2013.
- ↑ „13 Aluminium“. Elements.vanderkrogt.net. Посетено на 2008-09-12.
- ↑ Shakhashiri, B.Z. (17 March 2008). „Chemical of the Week: Aluminum“ (PDF). SciFun.org. University of Wisconsin. Архивирано од изворникот (PDF) на 9 May 2012. Посетено на 4 March 2012.
- ↑ 8,0 8,1 Singh, Bikram Jit (2014). RSM: A Key to Optimize Machining: Multi-Response Optimization of CNC Turning with Al-7020 Alloy (англиски). Anchor Academic Publishing (aap_verlag). ISBN 978-3-95489-209-9.
- ↑ Hihara, Lloyd H.; Adler, Ralph P.I.; Latanision, Ronald M. (2013). Environmental Degradation of Advanced and Traditional Engineering Materials (англиски). CRC Press. ISBN 978-1-4398-1927-2.
- ↑ Frank, W.B. (2009). „Aluminum“. Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH. doi:10.1002/14356007.a01_459.pub2. ISBN 978-3-527-30673-2.
- ↑ 11,0 11,1 IAEA – Nuclear Data Section (2017). „Livechart – Table of Nuclides – Nuclear structure and decay data“. www-nds.iaea.org. International Atomic Energy Agency. Посетено на 31 March 2017.
- ↑ Dickin, A.P. (2005). „In situ Cosmogenic Isotopes“. Radiogenic Isotope Geology. Cambridge University Press. ISBN 978-0-521-53017-0. Архивирано од изворникот на 6 декември 2008. Посетено на 16 јули 2008.
- ↑ Dodd, R.T. (1986). Thunderstones and Shooting Stars. Harvard University Press. стр. 89–90. ISBN 978-0-674-89137-1.
- ↑ Dean 1999, стр. 4.2.
- ↑ Dean 1999, стр. 4.6.
- ↑ Dean 1999, стр. 4.29.
- ↑ 17,0 17,1 Dean 1999, стр. 4.30.
- ↑ Enghag, Per (2008). Encyclopedia of the Elements: Technical Data – History – Processing – Applications. John Wiley & Sons. стр. 139, 819, 949. ISBN 978-3-527-61234-5.
- ↑ Lide 2004, стр. 4-3.
- ↑ Polmear, I.J. (1995). Light Alloys: Metallurgy of the Light Metals (3. изд.). Butterworth-Heinemann. ISBN 978-0-340-63207-9.
- ↑ Dieter, G.E. (1988). Mechanical Metallurgy. McGraw-Hill. ISBN 978-0-07-016893-0.
- ↑ Cochran, J.F.; Mapother, D.E. (1958). „Superconducting Transition in Aluminum“. Physical Review. 111 (1): 132–142. Bibcode:1958PhRv..111..132C. doi:10.1103/PhysRev.111.132.
- ↑ Devoret, M.H.; Schoelkopf, R.J. (2013). „Superconducting Circuits for Quantum Information: An Outlook“. Science. 339 (6124): 1169–1174. Bibcode:2013Sci...339.1169D. doi:10.1126/science.1231930. PMID 23471399.
- ↑ Vargel, Christian (2004) [French edition published 1999]. Corrosion of Aluminium. Elsevier. ISBN 978-0-08-044495-6. Архивирано од изворникот 21 May 2016.
- ↑ Polmear, I.J. (1995). Light Alloys: Metallurgy of the Light Metals (3. изд.). Butterworth-Heinemann. ISBN 978-0-340-63207-9.
- ↑ Beal, Roy E. (1999). Engine Coolant Testing : Fourth Volume. ASTM International. стр. 90. ISBN 978-0-8031-2610-7. Архивирано од изворникот 24 April 2016.
- ↑ Macleod, H.A. (2001). Thin-film optical filters. CRC Press. стр. 158159. ISBN 978-0-7503-0688-1.
- ↑ „Reaction of Aluminum with Water to Produce Hydrogen“ (PDF). U.S. Department of Energy. 1 January 2008. Архивирано од изворникот (PDF) на 14 September 2012.
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2. изд.). Butterworth-Heinemann. стр. 217. ISBN 0080379419.
- ↑ Roscoe, Henry Enfield; Schorlemmer, Carl (1913). A treatise on chemistry (англиски). Macmillan.
- ↑ Eastaugh, Nicholas; Walsh, Valentine; Chaplin, Tracey; Siddall, Ruth (2008). Pigment Compendium (англиски). Routledge. ISBN 978-1-136-37393-0.
- ↑ Dohmeier, C.; Loos, D.; Schnöckel, H. (1996). „Aluminum(I) and Gallium(I) Compounds: Syntheses, Structures, and Reactions“. Angewandte Chemie International Edition. 35 (2): 129–149. doi:10.1002/anie.199601291.
- ↑ Dohmeier, C.; Loos, D.; Schnöckel, H. (1996). „Aluminum(I) and Gallium(I) Compounds: Syntheses, Structures, and Reactions“. Angewandte Chemie International Edition. 35 (2): 129–149. doi:10.1002/anie.199601291.
- ↑ Tyte, D.C. (1964). „Red (B2Π–A2σ) Band System of Aluminium Monoxide“. Nature (journal). 202 (4930): 383–384. Bibcode:1964Natur.202..383T. doi:10.1038/202383a0.
- ↑ Merrill, P.W.; Deutsch, A.J.; Keenan, P.C. (1962). „Absorption Spectra of M-Type Mira Variables“. The Astrophysical Journal. 136: 21. Bibcode:1962ApJ...136...21M. doi:10.1086/147348.
- ↑ Uhl, W. (2004). „Organoelement Compounds Possessing AlAl, GaGa, InIn, and TlTl Single Bonds“. Organoelement Compounds Possessing Al–Al, Ga–Ga, In–In, and Tl–Tl Single Bonds. Advances in Organometallic Chemistry. 51. стр. 53–108. doi:10.1016/S0065-3055(03)51002-4. ISBN 978-0-12-031151-4.
- ↑ Elschenbroich, C. (2006). Organometallics. Wiley-VCH. ISBN 978-3-527-29390-2.
- ↑ 38,0 38,1 Lodders, K. (2003). „Solar System abundances and condensation temperatures of the elements“ (PDF). The Astrophysical Journal. 591 (2): 1220–1247. Bibcode:2003ApJ...591.1220L. doi:10.1086/375492. ISSN 0004-637X.
- ↑ 39,0 39,1 39,2 Clayton, Donald (2007). Handbook of Isotopes in the Cosmos: Hydrogen to Gallium. Cambridge University Press. стр. 129–137. ISBN 978-0-521-53083-5.
- ↑ Вилијам Ф. Мекдоналд Составот на Земјата. quake.mit.edu, архивирана од Интернет-архивата Wayback Machine.
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2. изд.). Butterworth-Heinemann. ISBN 0080379419.
- ↑ Wade, K.; Banister, A.J. (2016). The Chemistry of Aluminium, Gallium, Indium and Thallium: Comprehensive Inorganic Chemistry. Elsevier. стр. 1049. ISBN 978-1-4831-5322-3.
- ↑ Palme, H.; O'Neill, Hugh St. C. (2005). „Cosmochemical Estimates of Mantle Composition“ (PDF). Во Carlson, Richard W. (уред.). The Mantle and Core. Elseiver. стр. 14.
- ↑ Downs, A.J. (1993). Chemistry of Aluminium, Gallium, Indium and Thallium (англиски). Springer Science & Business Media. ISBN 978-0-7514-0103-5.
- ↑ Kotz, John C.; Treichel, Paul M.; Townsend, John (2012). Chemistry and Chemical Reactivity. Cengage Learning. стр. 300. ISBN 978-1-133-42007-1.
- ↑ Barthelmy, D. „Aluminum Mineral Data“. Mineralogy Database. Архивирано од изворникот 4 July 2008. Посетено на 9 July 2008.
- ↑ Chen, Z.; Huang, Chi-Yue; Zhao, Meixun; Yan, Wen; Chien, Chih-Wei; Chen, Muhong; Yang, Huaping; Machiyama, Hideaki; Lin, Saulwood (2011). „Characteristics and possible origin of native aluminum in cold seep sediments from the northeastern South China Sea“. Journal of Asian Earth Sciences. 40 (1): 363–370. Bibcode:2011JAESc..40..363C. doi:10.1016/j.jseaes.2010.06.006.
- ↑ Guilbert, J.F.; Park, C.F. (1986). The Geology of Ore Deposits. W.H. Freeman. стр. 774–795. ISBN 978-0-7167-1456-9.
- ↑ United States Geological Survey (2018). „Bauxite and alumina“ (PDF). Mineral Commodities Summaries. Посетено на 17 June 2018.
- ↑ 50,0 50,1 Drozdov 2007, стр. 12.
- ↑ Clapham, John Harold; Power, Eileen Edna (1941). The Cambridge Economic History of Europe: From the Decline of the Roman Empire. CUP Archive. стр. 207. ISBN 978-0-521-08710-0.
- ↑ Drozdov 2007, стр. 16.
- ↑ Setton, Kenneth M. (1976). The papacy and the Levant: 1204-1571. 1 The thirteenth and fourteenth centuries. American Philosophical Society. ISBN 978-0-87169-127-9. OCLC 165383496.
- ↑ Drozdov 2007, стр. 25.
- ↑ Weeks, Mary Elvira (1968). Discovery of the elements. 1 (7. изд.). Journal of chemical education. стр. 187.
- ↑ 56,0 56,1 Richards 1896, стр. 2.
- ↑ Richards 1896, стр. 3.
- ↑ Royal Danish Academy of Sciences and Letters (1827). Det Kongelige Danske Videnskabernes Selskabs philosophiske og historiske afhandlinger [The philosophical and historical dissertations of the Royal Danish Science Society] (дански). Popp. стр. xxv–xxvi.
- ↑ 59,0 59,1 Wöhler, Friedrich (1827). „Ueber das Aluminium“. Annalen der Physik und Chemie. 2. 11: 146–161.
- ↑ Drozdov 2007, стр. 36.
- ↑ Fontani, Marco; Costa, Mariagrazia; Orna, Mary Virginia (2014). The Lost Elements: The Periodic Table's Shadow Side. Oxford University Press. стр. 30. ISBN 978-0-19-938334-4.
- ↑ 62,0 62,1 Venetski, S. (1969). „'Silver' from clay“. Metallurgist. 13 (7): 451–453. doi:10.1007/BF00741130.
- ↑ 63,0 63,1 Drozdov 2007, стр. 38.
- ↑ Holmes, Harry N. (1936). „Fifty Years of Industrial Aluminum“. The Scientific Monthly. 42 (3): 236–239.
- ↑ 65,0 65,1 Drozdov 2007, стр. 39.
- ↑ Sainte-Claire Deville, H.E. (1859). De l'aluminium, ses propriétés, sa fabrication. Paris: Mallet-Bachelier. Архивирано од изворникот 30 April 2016.
- ↑ Polmear, Ian (2005). Light Alloys: From Traditional Alloys to Nanocrystals. Butterworth-Heinemann. стр. 15. ISBN 978-0-08-049610-8.
- ↑ Drozdov 2007, стр. 46.
- ↑ Drozdov 2007, стр. 55–61.
- ↑ Drozdov 2007, стр. 74.
- ↑ 71,0 71,1 71,2 „Aluminium history“. All about aluminium. Посетено на 7 November 2017.
- ↑ Drozdov 2007, стр. 64–69.
- ↑ Ingulstad, Mats (2012). „'We Want Aluminum, No Excuses': Business-Government Relations in the American Aluminum Industry, 1917–1957“. Во Ingulstad, Mats; Frøland, Hans Otto (уред.). From Warfare to Welfare: Business-Government Relations in the Aluminium Industry. Tapir Academic Press. стр. 33–68. ISBN 978-82-321-0049-1.
- ↑ Drozdov 2007, стр. 69–70.
- ↑ Drozdov 2007, стр. 165–166.
- ↑ Drozdov 2007, стр. 85.
- ↑ Drozdov 2007, стр. 135.
- ↑ 78,0 78,1 78,2 (Report). Отсутно или празно
|title=(help) - ↑ Nappi 2013, стр. 9.
- ↑ Nappi 2013, стр. 9–10.
- ↑ Nappi 2013, стр. 10.
- ↑ Nappi 2013, стр. 14–15.
- ↑ Nappi 2013, стр. 17.
- ↑ Nappi 2013, стр. 20.
- ↑ Nappi 2013, стр. 22.
- ↑ Nappi 2013, стр. 23.
- ↑ Discogs, The White Stripes – White Blood Cells (пристапено на 9.10.2021)
| Периоден систем на елементите | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| I | H | He | |||||||||||||||||||||||||||||||
| II | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| III | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| IV | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| V | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| VI | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| VII | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
|
| |||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||
|


