Закиселување на океаните




Закиселувањето на океаните — тековно намалување на pH вредноста на океаните на Земјата, предизвикано од навлегувањето на јаглерод диоксид (CO
2) од атмосферата.[2] Главната причина за закиселување на океаните се човечките активности, имено согорувањето на фосилните горива. Како што се зголемува количината на јаглерод диоксид во атмосферата, се зголемува и количината на јаглерод диоксид што се апсорбира од океанот. Ова доведува до серија хемиски реакции во морската вода и има негативно прелевање на океанот и живите видови кои живеат под вода.[3] Кога јаглерод диоксидот се раствора во морската вода, образува јаглеродна киселина (H2CO3).
Закиселувањето на океаните влијае на многу видови, особено на организмите како остриги и корали. Тоа е еден од неколкуте ефекти на климатските промени врз океаните. Морската вода е малку основна (што значи pH > 7), а закиселувањето на океаните вклучува поместување кон pH-неутрални услови наместо транзиција кон кисели услови (pH <7).[4] Загриженоста со закиселувањето на океаните е тоа што може да доведе до намалено производство на школки и други водни животни со школки од калциум карбонат, како и некои други физиолошки предизвици за морските организми. Организмите обложени со калциум карбонат не можат да се репродуцираат под високо заситени ацидотични води. Дел од него реагира со водата и образува јаглеродна киселина. Некои од добиените молекули на јаглеродна киселина се дисоцираат во бикарбонатен јон и водороден јон, со што се зголемува киселоста на океаните (концентрација на H<sup id="mwPw">+</sup> јони).
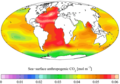
Помеѓу 1751 и 1996 година, се проценува дека pH вредноста на површината на океанот се намалила од приближно 8,25 на 8,14,[5] што претставува зголемување од речиси 30% во концентрацијата на јони H+ во светските океани (забележливо е дека рН скалата е логаритамска, така што промена од една во pH единица е еквивалентна на десеткратна промена во концентрацијата на H+ јони).[6][7] Според Националната океанска и атмосферска управа, pH вредноста на океаните денес е 8,1.[3] Постои варијација во pH вредноста на морската површина на глобално ниво со постудени и повисоки океани кои имаат способност да растворат повеќе CO2 и затоа дополнително да ја зголемат нивната киселост, како и пониски нивоа на заситеност со бикарбонати, за возврат намалувајќи ја способноста на морските организми да произведуваат тврди школки.[8] Фактори како што се океанските струи, големите континентални реки кои ја разредуваат соленоста на морската вода, топењето на мразот и таложењето на азот и сулфур од согорувањето на фосилните горива и земјоделството, исто така влијаат на киселоста на океаните.[9]
Се смета дека зголемената киселост има низа потенцијално штетни последици за морските организми како што се депресивни метаболички стапки и имунолошки реакции кај некои организми и предизвикување белење на коралите.[10] Закиселувањето на океаните влијае на екосистемите на морските средини кои обезбедуваат храна, средства за живот и други екосистемски услуги за голем дел од човечката популација. Околу 1 милијарда луѓе се целосно или делумно зависни од екосистемските услуги што ги обезбедуваат коралните гребени во однос на риболов, туризам и управување со крајбрежјето.[11] Со зголемување на присуството на слободни водородни јони, дополнителната јаглеродна киселина што се образува во океаните на крајот резултира со претворање на карбонатните јони во бикарбонатни јони. Алкалноста на океаните не се менува со процесот или може да се зголеми во долги временски периоди поради растворање на карбонат.[12] Ова нето намалување на бројот на достапни карбонатни јони може да им отежне на морските калцифицирачки организми, како што се коралите и некои планктони, да образуваат биоген калциум карбонат, а таквите структури стануваат ранливи на растворање.[13] Поради тоа, тековното закиселување на океаните може да ги загрози идните синџири на исхрана поврзани со океаните.[14][15]
Главното решение за закиселување на океаните лежи во намалувањето на нивото на CO2 во атмосферата. Како членови на Интеракадемскиот панел, 105 научни академии дале изјава за закиселување на океаните во која препорачуваат до 2050 година, глобалните емисии на CO2 да се намалат за најмалку 50% во споредба со нивото од 1990 година.[16] Целта 14 за одржлив развој на Обединетите нации („Живот под вода“) има цел да ги „минимизира и да ги реши влијанијата од закиселувањето на океаните“.[17]
Закиселувањето на океаните се случило претходно во историјата на Земјата,[18] и резултирачкиот еколошки колапс во океаните имал долготрајни ефекти врз глобалниот јаглероден циклус и климата.[19][20]
Причини и јаглероден циклус
[уреди | уреди извор]
Човечките активности како што се согорувањето на фосилните горива и промените во користењето на земјиштето довеле до нов проток на CO2 во атмосферата. Околу 45% останало во атмосферата; поголемиот дел од остатокот е преземен од океаните,[21] со дел од копнените растенија.[22]


Јаглеродниот циклус ги опишува флуксот на јаглерод диоксид (CO2) помеѓу океаните, копнената биосфера, литосферата, и атмосферата. Јаглеродниот циклус вклучува и органски соединенија како целулоза и неоргански јаглеродни соединенија како што се јаглерод диоксид, карбонат јон и бикарбонат јон. Неорганските соединенија се особено релевантни кога се зборува за закиселување на океаните бидејќи тие вклучуваат многу форми на растворен CO2 присутни во океаните на Земјата.[25]
Кога CO2 се раствора, реагира со вода за да образува рамнотежа на јонски и нејонски хемиски видови: растворен слободен јаглерод диоксид (CO2(aq)), јаглеродна киселина (H2CO3), бикарбонат (HCO−
3) и карбонат (CO2−
3). Односот на овие видови зависи од фактори како што се температурата на морската вода, притисокот и соленоста. Овие различни форми на растворен неоргански јаглерод се пренесуваат од површината на океанот до неговата внатрешност со помош на океанската пумпа за растворливост.
Отпорот на површина од океанот на апсорпција на атмосферски CO2 е познат како Ревелов фактор.
Закиселувањето на океаните е споредено со антропогените климатски промени и се нарекува „злобниот близнак на глобалното затоплување“ [26][27][28][29][30] и „другиот проблем со CO2“.[27][29][31] Зголемените температури на океаните и загубата на кислород дејствуваат истовремено со закиселувањето на океаните и го сочинуваат „смртоносното трио“ на притисоци од климатските промени врз морската средина.[32] Се смета дека и слатководните тела се закиселуваат, иако ова е покомплексен и помалку очигледен феномен.[33][34]
Се проценува дека 30-40% од јаглерод диоксидот од човековата активност ослободен во атмосферата се раствора во океани, реки и езера.[23][35]
Механизам на закиселување
[уреди | уреди извор]Распуштање на CO2 во морската вода го зголемува водородниот јон (H+) концентрација во океанот, а со тоа и ја намалува pH вредноста на океанот, како што следува:[36]
Приближно една третина од јаглерод диоксидот ослободен во атмосферата со човечка активност се раствора во океаните, реките и езерата, што резултира со зголемени нивоа на закиселување.[37] Нивото на киселоста на површината на океаните се зголемила за 30% од почетокот на индустриската револуција.
Од почетокот на индустриската револуција, океанот апсорбира околу една третина од CO2 [38] и се проценува дека pH вредноста на површината на океанот се намалила за нешто повеќе од 0,1 единица на логаритамската скала на pH, што претставува околу 29% зголемување на H+. Се очекува да се намали за дополнителни 0,3 до 0,5 pH единици [39] (дополнително удвојување до тројно зголемување на денешните концентрации на постиндустриска киселина) до 2100 година бидејќи океаните апсорбираат повеќе антропоген CO2, влијанијата се најтешки за коралните гребени и Јужниот Океан.[2] Се предвидува дека овие промени ќе се забрзаат како поантропоген CO2 се ослободува во атмосферата и се зема од океаните. Степенот на промена на океанската хемија, вклучително и pH на океаните, ќе зависи од патеките за ублажување и емисиите [40] преземени од општеството.[41]
Иако најголемите промени се очекуваат во иднина, извештај од научниците на NOAA покажале дека големи количини на вода незаситена во арагонит веќе се зголемуваат во близина на областа на континенталниот праг на Тихиот Океан во Северна Америка.[1] Континенталните полици играат важна улога во морските екосистеми, бидејќи повеќето морски организми живеат таму, и иако студијата се занимавала само со областа од Ванкувер до Северна Калифорнија, авторите сугерираат дека другите области на гребенот може да искусат слични ефекти.[1]
| Време | pH вредност | Релативна промена на pH до прединдустриски |
Извор | H + промена на концентрацијата во однос на прединдустрискиот |
|---|---|---|---|---|
| Прединдустриски (18 век) | 8.179 | анализирано поле [42] [ неуспешна верификација ] | ||
| Неодамнешно минато (1990-ти) | 8.104 | −0,075 | поле [42] | + 18,9% |
| Сегашни нивоа | ~ 8.069 | −0,11 | поле [7][43][44] | + 28,8% |
| 2050 (2× CO2 = 560 ppm) | 7.949 | −0,230 | модел [13] [ неуспешна верификација ] | + 69,8% |
| 2100 (IS92a) | 7.824 | −0,355 | модел [13] [ неуспешна верификација ] | + 126,5% |

Во плитки крајбрежни региони, голем број фактори се вкрстуваат за да влијаат на промената на pH вредноста покрај атмосферскиот CO2.[45][46] Тие вклучуваат биолошки процеси, како што се фотосинтезата и дишењето,[47] и издигнувањето на водата на брегот може да се измени со овие процеси.[48][49][50] Исто така, метаболизмот на екосистемот во слатководните извори што стигнуваат до крајбрежните води може да доведе до големи промени на pH таму,[45] со стапки на биолошки индуцирана промена на pH зависни од локалната температура на водата.
Набљудувани стапки
[уреди | уреди извор]| “ | Ако продолжиме да емитираме CO 2 со иста брзина, до 2100 година киселоста на океаните ќе се зголеми за околу 150 проценти, стапка која не е забележана најмалку 400.000 години. |
” |
—Програма за истражување на океаните за закиселување на Обединетото Кралство, 2015[51] | ||
Една од првите детални збирки на податоци за испитување како рН варирала во текот на 8 години на одредена северна умерена крајбрежна локација открила дека закиселувањето има силни врски со динамиката на in situ видови и дека варијацијата во pH вредноста на океаните може да предизвика варовничките видови да имаат полошо од неваровничките видови во години со ниска pH вредност и предвидува последици за бенталните екосистеми во близина на брегот.[52][53]
Сегашните стапки на закиселување на океаните се споредени со настанот на стаклена градина на границата Палеоцен-Еоцен (околу 55 пред милиони години) кога температурата на површината на океаните се зголемила за 5-6 степени целзиусови. Не била забележана катастрофа во површинските екосистеми, но сепак организмите кои живеат на дното во длабоките океани доживеале големо истребување. Тековната киселост е на пат да достигне нивоа повисоки од било кое забележано во последните 65 милиони години,[54][55][56] и стапката на пораст е околу десет пати поголема од стапката што му претходела на палеоценско-еоценското масовно изумирање. Сегашната и проектираната киселост е опишана како речиси невиден геолошки настан.[57] Студијата на Националниот совет за истражување објавена во април 2010 година исто така заклучила дека „нивото на киселина во океаните се зголемува со невидена брзина“.[58][59] Еден труд од 2012 година во списанието Science го испитувала геолошкиот запис во обид да најде историски аналог за сегашните глобални услови, како и за оние во иднината. Истражувачите утврдиле дека моменталната стапка на закиселување на океаните е побрза отколку кога било во изминатите 300 милиони години.[60][61]
Преглед на климатските научници на блогот RealClimate, на извештајот од 2005 година на Кралското друштво на Обединетото Кралство на сличен начин ја истакнала централноста на стапките на промена во сегашниот процес на антропогена киселост, пишувајќи:[62]
„Природната pH вредност на океанот е одредена од потребата да се балансира таложењето и закопувањето на CaCO3 на морското дно против приливот на Ca2+ и CO2−
3 во океанот од растворање на карпите на копно, наречено атмосферски влијанија. Овие процеси ја стабилизираат pH вредноста на океанот, со механизам наречен CaCO3 компензација... Поентата да се изнесе повторно е да се забележи дека ако CO2 концентрацијата на атмосферата се менува побавно од ова, pH вредноста на океанот ќе биде релативно непроменета бидејќи CaCO3 може да продолжи. [сегашната] киселост на фосилните горива е многу побрза од природните промени, и затоа скокот на киселината ќе биде поинтензивен отколку што Земјата видела во најмалку 800.000 години."
Само во 15-годишниот период 1995-2010 година, киселоста се зголемила за 6 проценти во горните 100 метри на Тихиот Океан од Хаваи до Алјаска.[63] Според изјавата во јули 2012 година на Џејн Лубченко, шеф на американската Национална океанска и атмосферска администрација „површинските води се менуваат многу побрзо отколку што сугерираа првичните пресметки. Тоа е уште една причина да бидеме многу сериозно загрижени за количината на јаглерод диоксид што сега е во атмосферата и дополнителната количина што продолжуваме да ја исфрламе.“ [26]
Една студија од 2013 година тврди дека киселоста се зголемува со брзина 10 пати побрзо отколку во која било од еволутивните кризи во историјата на Земјата.[64] Во синтетичкиот извештај објавен во Science во 2015 година, 22 водечки поморски научници изјавиле дека од согорувањето на фосилните горива ја менува хемијата на океаните побрзо од кога било од Големото истребување, најтешкиот познат настан на истребување на Земјата, нагласувајќи дека 2 °C максималното зголемување на температурата договорено од владите го одразува премалото намалување на емисиите за да се спречат „драматичните влијанија“ врз светските океани, при што водечкиот автор Жан-Пјер Гатузо забележал дека „Океанот беше минимално земен предвид на претходните преговори за климата. Нашата студија дава убедливи аргументи за радикална промена на конференцијата на ОН (во Париз) за климатските промени.“ [65]
Брзината со која ќе се појави закиселување на океаните може да биде под влијание на стапката на затоплување на површинските океани, бидејќи хемиските рамнотежи кои управуваат со pH на морската вода зависат од температурата.[66] Поголемото затоплување на морската вода може да доведе до помала промена на pH вредноста за дадено зголемување на CO2.[66] Разликата во промените во температурата и соленоста помеѓу басените е една од главните причини за разликите во стапките на закиселување во различни локалитети.
| Место | Стапка на закиселување (10 −3 pH единици / година) | Период | Извор на податоци |
|---|---|---|---|
| Исланд [67] | -2.4 | 1984 – 2009 година | Директни мерења |
| Пасаж Дрејк [68] | -1,8 | 2002 – 2012 година | Директни мерења |
| Канари[69] | -1,7 | 1995 – 2004 година | Директни мерења |
| Хаваи[70] | -1,9 | 1989 – 2007 година | Директни мерења |
| Бермуди [71] | -1,7 | 1984 – 2012 година | Директни мерења |
| Коралното море [72] | -0,2 | ~ 1700 - ~ 1990 година | Реконструкција на прокси |
| Источен Медитеран [73] | -2.3 | 1964 – 2005 година | Реконструкција на прокси |
Предвидени идни стапки
[уреди | уреди извор]Проектот Наука за Земјиниот систем информира дека, до околу 2008 година, киселоста на океаните ги надминала историските аналози [74] и, во комбинација со други биогеохемиски промени на океаните, може да го поткопа функционирањето на морските екосистеми и да го наруши обезбедувањето на многу добра и услуги поврзани со почетокот на океанот како уште во 2100 г.[39]
Доколку опстојува моделот „бизнис како и обично“ за човековата активност, се проценува дека pH вредноста на океаните во 2100 година би можела да се намали за 0,2 до 0,5 единици во споредба со денешниот ден.[75] Океаните не го доживеале ова ниво на киселост 14 милиони години.[76]
Се предвидува дека ќе се случи еколошка пресвртна точка до 2030 година, а најдоцна до 2038 година [77] Томас Лавџој, поранешен главен советник за биолошка разновидност на Светската банка, посочил дека киселоста на океаните ќе се удвои во следните 40 години. Тој изјавил дека оваа стапка е 100 пати поголема од какви било промени во киселоста на океаните во последните 20 милиони години, што го прави малку веројатно дека морскиот живот некако може да се прилагоди на промените.[78] Се предвидува дека до 2100 година, доколку истовремените биогеохемиски промени влијаат на испораката на океанските добра и услуги, тогаш тие исто така би можеле да имаат значителен ефект врз човековата благосостојба на оние кои многу се потпираат на океанот за храна, работа и приходи.
Експерти кои претходно учествувале во извештаите на IPCC утврдиле дека сè уште не е можно да се одреди праг за киселост на океаните што не треба да се надмине.[79]
Ефекти врз калцификацијата
[уреди | уреди извор]Промените во хемијата на океаните може да имаат екстензивни директни и индиректни ефекти врз организмите и нивните живеалишта. Една од најважните последици од зголемената киселост на океаните се однесува на производството на школки и плочи од калциум карбонат (CaCO3).[80] Овој процес се нарекува калцификација и е важен за биологијата и опстанокот на широк опсег на морски организми. Калцификацијата вклучува таложење на растворени јони во цврст CaCO3 структури, како што се коколити. Откако ќе се образуваат, таквите структури се ранливи на растворање, освен ако околната морска вода содржи заситени концентрации на карбонатни јони (CO 3 2-).
Механизам
[уреди | уреди извор]
Од дополнителниот јаглерод диоксид додаден во океаните, дел останува како растворен јаглерод диоксид, додека остатокот придонесува за создавање дополнителен бикарбонат (и дополнителна јаглеродна киселина). Ова исто така ја зголемува концентрацијата на водородните јони, а процентот на зголемување на водородот е поголем од процентуалното зголемување на бикарбонатот,[81] создавајќи нерамнотежа во реакцијата HCO 3 − ⇌ CO 3 2− + H +. За да се одржи хемиската рамнотежа, некои од карбонатните јони кои се веќе во океанот се комбинираат со некои од водородните јони за да направат понатамошен бикарбонат. Така, концентрацијата на карбонатните јони во океанот е намалена, создавајќи нерамнотежа во реакцијата Ca 2+ + CO 3 2− ⇌ CaCO 3 и со што се прави растворање на образуваните CaCO3 структури поверојатно.
Зголемувањето на концентрациите на растворениот јаглерод диоксид и бикарбонат, и намалувањето на карбонатот, се прикажани на Бјерум.
Состојба на растворливост
[уреди | уреди извор]Состојбата на растворливост (позната како Ω) на морската вода за минерал е мерка за термодинамичкиот потенцијал за образување или растворање на минералот, а за калциум карбонат е опишан со следнава равенка:
Овде Ω е производ на концентрациите (или активностите) на јоните кои реагираат што го образуваат минералот (Ca2+ и CO2− 3), поделено со производот од концентрациите на тие јони кога минералот е во рамнотежа (К sp), односно кога минералот ниту се образува ниту се раствора. Во морската вода, природната хоризонтална граница се образува како резултат на температурата, притисокот и длабочината и е позната како хоризонт на заситеност[80]. Над овој хоризонт на растворливост, Ω има вредност поголема од 1, а CaCO3 не се раствора лесно. Повеќето калцифицирачки организми живеат во такви води. Под оваа длабочина, Ω има вредност помала од 1, а CaCO3 ќе се раствори. Меѓутоа, ако неговата стапка на производство е доволно висока за да се надомести растворањето, CaCO3 сè уште може да се појави каде што Ω е помало од 1. Длабочината на компензација на карбонат се јавува на длабочината во океанот каде што производството е надминато со растворање[82].
Намалувањето на концентрацијата на CO3 2− го намалува Ω, и оттука го прави CaCO3 поверојатно е распаѓање.
Калциум карбонатот се јавува во два вообичаени полиморфи (кристални форми): арагонит и калцит. Арагонитот е многу порастворлив од калцитот, така што хоризонтот на растворливост на арагонит е секогаш поблиску до површината од хоризонтот на заситеност со калцит.[80] Ова исто така значи дека оние организми кои произведуваат арагонит може да бидат поранливи на промени во киселоста на океаните отколку оние што произведуваат калцит.[13] Зголемување на CO2 нивоа и резултирачката пониска pH вредност на морската вода ја намалува состојбата на заситеност на CaCO3 и ги подига хоризонтите на заситеност на двете форми поблиску до површината.[83] Се верува дека ова намалување на состојбата на растворливост е еден од главните фактори што доведува до намалена калцификација кај морските организми, бидејќи неорганските врнежи на CaCO3 е правопропорционална на неговата состојба на растворливост.[84]
Влијанија
[уреди | уреди извор]Зголемувањето на киселоста има веројатно штетни последици, како што се депресивни стапки на метаболизмот кај џамбо лигњите,[85] депресирање на имунолошките одговори на сините школки,[86] и белење на коралите.
Извештаите „Резиме за закиселување на океаните за креаторите на политиките 2013“ и IPCC одобриле „Специјален извештај за океанот и криосферата во климата што се менува“ од 2019 година ги опишуваат наодите од истражувањето и можните влијанија.[87][88]
Корално белење
[уреди | уреди извор]Феноменот на корално белење или избелување на коралите и дегенерација на екосистемите на коралните гребени е една од последиците на зголемената киселост на океаните. Тропските и суптропските средини, вклучувајќи области како што се Карибите и околните региони, тропска Азија (на пр. Индонезија, Филипини, Тајланд, Малдиви) и тропскиот Тихи Океан (на пр Австралискиот корален гребен, тихоокеанските острови, Папуа Нова Гвинеја) се најмногу погодени од корално белење, бидејќи тоа се регионите во светот кои ги содржат најголемите и најобемните системи на корални гребени.[89]
Влијанија врз океанските организми
[уреди | уреди извор]
Зголеменото закиселување на океаните го отежнува пристапот на организмите што создаваат школки до карбонатните јони, неопходни за производство на нивната тврда егзоскелетна обвивка. Океанските калцифицирачки организми го опфаќаат синџирот на исхрана од автотрофи до хетеротрофи и вклучуваат организми како што се коколитофори, корали, фораминифери, ехинодерми, ракови и мекотели. Како што е опишано погоре, во нормални услови, калцитот и арагонитот се стабилни во површинските води бидејќи карбонатниот јон е во презаситени концентрации. Меѓутоа, како што опаѓа pH на океаните, концентрацијата на карбонатните јони исто така се намалува, а кога карбонатот станува недозаситен, структурите направени од калциум карбонат се ранливи на растворање. Затоа, дури и ако нема промена во стапката на калцификација, стапката на растворање на варовничкиот материјал се зголемува.[90]

Корали,[91][92][93][94] коколитофорни алги,[95][96][97][98] коралини алги,[99] фораминифери,[100] школки [101] и птероподи[13][102] имаат зголемено растворање кога се изложени на покачен CO2.
Кралското друштво објавило сеопфатен преглед на закиселувањето на океаните и неговите потенцијални последици, во јуни 2005 година.[80] Сепак, некои студии пронашле различни одговори на закиселувањето на океаните, при што калцификацијата и фотосинтезата на коколитофор се зголемуваат при покачена атмосферска pCO2,[103][104][105] еднаков пад на примарното производство и калцификацијата како одговор на покаченото CO2 [106] или насоката на одговорот варира помеѓу видовите.[107] Студијата во 2008 година, која го испитувала јадрото на седиментот од Северен Атлантик, покажала дека иако составот на видовите на коколитофоридите останал непроменет за индустрискиот период од 1780 до 2004 година, калцификацијата на коколитите се зголемила до 40% во исто време.[105] Студијата од 2010 година од Универзитетот Стони Брук сугерирала дека додека некои области се прекумерно ожнеани и други риболовни терени се обновуваат, поради закиселувањето на океаните можеби е невозможно да се вратат многу претходни популации на школки. Иако целосните еколошки последици од овие промени во калцификацијата се сè уште неизвесни, се чини дека многу видови кои калцифицираат ќе бидат негативно погодени.
Кога биле изложени во експерименти на pH намалена за 0,2 до 0,4, ларвите на умерена кршлива ѕвезда, роднина на обичната морска ѕвезда, помалку од 0,1 отсто преживеале повеќе од осум дена. Исто така, постои сугестија дека падот на коколитофорите може да има секундарни ефекти врз климата, придонесувајќи за глобалното затоплување со намалување на албедото на Земјата преку нивните ефекти врз облачноста на океаните.[108] Сите морски екосистеми на Земјата ќе бидат изложени на промени во закиселувањето и на неколку други биогеохемиски промени во океаните.
Течноста во внатрешните одделенија (целентерон) каде коралите го растат нивниот егзоскелет е исто така исклучително важна за растот на калцификацијата. Кога стапката на заситеност на арагонитот во надворешната морска вода е на амбиентално ниво, коралите брзо ќе ги растат своите арагонитни кристали во нивните внатрешни прегради, па оттука нивниот егзоскелет брзо расте. Ако нивото на арагонит во надворешната морска вода е пониско од нивото на околината, коралите мора да работат понапорно за да ја одржат вистинската рамнотежа во внатрешниот оддел. Кога тоа ќе се случи, процесот на растење на кристалите се забавува, а тоа ја забавува брзината на тоа колку расте нивниот егзоскелет. Во зависност од тоа колку арагонит има во околната вода, коралите може дури и да престанат да растат бидејќи нивоата на арагонит се премногу ниски за да се втурнат во внатрешниот оддел. Тие дури може да се растворат побрзо отколку што можат да направат кристали во нивниот скелет, во зависност од нивото на арагонит во околната вода.[109] Според сегашната прогресија на емисиите на јаглерод, околу 70% од северноатлантските ладни корали ќе живеат во корозивни води до 2050-60 година.[110]
Студијата спроведена од океанографската институција Вудс Хол во јануари 2018 година покажала дека скелетниот раст на коралите во закиселени услови е примарно под влијание на намалениот капацитет за градење густи егзоскелети, наместо да влијае на линеарното проширување на егзоскелетот. Користејќи глобални климатски модели, тие покажуваат дека густината на некои видови корали може да се намали за над 20% до крајот на овој век.[111]
Експериментот на самото место на површина од 400 m 2 на Големиот корален гребен за намалување на нивото на CO2 на морската вода (покачување на pH) до приближно до прединдустриската вредност покажала зголемување од 7% во нето калцификацијата.[112] Сличен експеримент за подигање на нивото на CO2 на морската вода на ниво што се очекува наскоро по средината на овој век покажала дека нето калцификацијата се намалила за 34%.[113]
Закиселувањето на океаните може да принуди некои организми да ги прераспределат ресурсите подалеку од продуктивни крајни точки како што е растот со цел да се одржи калцификацијата.[114] На пример, остригите, Magallana gigas, се препознаваат дека доживуваат метаболички промени заедно со изменетите стапки на калцификација поради енергетските размени кои произлегуваат од нерамнотежа на pH.[115]
На некои места јаглерод диоксидот излегува од морското дно, локално менувајќи ја pH вредноста и другите аспекти на хемијата на морската вода. Студиите за овие протекувања на јаглерод диоксид документирале различни одговори од различни организми. Заедниците на коралните гребени сместени во близина на вливот на јаглерод диоксид се од особен интерес поради чувствителноста на некои видови корали на закиселување. Во Папуа Нова Гвинеја, намалувањето на pH вредноста предизвикано од навлегувањето на јаглерод диоксид е поврзано со падот на разновидноста на видовите на коралите.[116] Сепак, во Палау протекувањето на јаглерод диоксид не е поврзано со намалената разновидност на видовите на коралите, иако биоерозијата на коралните скелети е многу повисока на места со ниска pH вредност.
Закиселувањето на океаните може да влијае на океанските биолошки водени секвестрации на јаглерод од атмосферата во внатрешноста на океаните и седиментот на морското дно, слабеејќи ја таканаречената биолошка пумпа.[117] Закиселувањето на морската вода, исто така, може да ги направи фитопланктоните на Антарктикот помали и помалку ефикасни во складирањето на јаглеродот.[118] Ваквите промени се повеќе се проучуваат и синтетизираат преку употреба на физиолошки рамки.
Други биолошки влијанија
[уреди | уреди извор]Освен забавувањето и/или враќањето на калцификацијата, организмите може да претрпат други негативни ефекти, или индиректно преку негативни влијанија врз ресурсите на храна,[80] или директно како репродуктивни или физиолошки ефекти. На пример, покачените океански нивоа на CO може да произведат CO2 индуцирана закиселување на телесните течности, позната како хиперкапнија. Исто така, се верува дека зголемувањето на киселоста на океаните има низа директни последици. На пример, зголемената киселост е забележана за: намалување на метаболичките стапки во џамбо лигњите;[85] ги намалува имунолошките одговори на сините школки.[86] Ова е веројатно затоа што закиселувањето на океаните може да ги промени акустичните својства на морската вода, дозволувајќи му на звукот дополнително да се шири и да ја зголеми бучавата од океанот.[119] Ова влијае на сите животни кои користат звук за ехолокација или комуникација.[120] На јајцата на лигњите од Атлантикот им било потребно подолго време да се изведат во закиселена вода, а статолитот на лигњите бил помал и погрешно образуван кај животните сместени во морска вода со пониска pH вредност. Пониската PH била симулирана со 20-30 пати повеќе од нормалната количина на CO2.[121] Сепак, како и кај калцификацијата, сè уште нема целосно разбирање на овие процеси во морските организми или екосистеми.[122]
Друг можен ефект би бил зголемувањето на појавата на црвените плими, што може да придонесе за акумулација на токсини кај малите организми како што се сарделата и школките, за возврат зголемување на појавата на труење со амнестични школки, невротоксично труење со школки и паралитично труење со школки.[123]
Иако црвената плима е штетна, други корисни фотосинтетички организми можат да имаат корист од зголеменото ниво на јаглерод диоксид. Што е најважно, морските треви ќе имаат корист.[124] Експериментот направен во 2018 година заклучил дека како што морските треви ја зголемуваат својата фотосинтетичка активност, стапките на калцификација на алгите се зголемуваат. Ова може да биде потенцијална техника за ублажување во услови на зголемена киселост.[124]
Закиселувањето на океаните може да биде од корист за некои видови, на пример зголемување на стапката на раст на морската ѕвезда, Pisaster ochraceus. [125]
Рибини лаври
[уреди | уреди извор]Закиселувањето на океаните исто така може да има влијание врз ларвите на морските риби. Тоа внатрешно влијае на нивните миризливи системи, што е клучен дел од нивниот развој, особено во почетната фаза од нивниот живот. Портокаловите ларви претежно живеат на океанските гребени кои се опкружени со вегетативни острови.[126] Со користење на нивното сетило за мирис, познато е дека ларвите можат да ги откријат разликите помеѓу гребените опкружени со вегетативни острови и гребените кои не се опкружени со вегетативни острови.[126] Ларвите на рибите-кловн треба да бидат способни да прават разлика помеѓу овие две дестинации за да имаат способност да лоцираат област која е задоволителна за нивниот раст. Друга употреба на системите за миризба на морските риби е да се помогне во одредувањето на разликата помеѓу нивните родители и другите возрасни риби со цел да се избегне оплодување помеѓу крвни сродници.
Во експерименталниот објект за аквариум на Универзитетот Џејмс Кук, рибите-кловн се одржувале во неманипулирана морска вода која добила pH од 8,15 ± 0,07, што е слична на pH вредноста на нашиот сегашен океан. За да се тестираат ефектите на различни нивоа на pH, морската вода била манипулирана на три различни pH нивоа, вклучувајќи ја и неманипулираната pH вредност. Двете спротивставени нивоа на pH кореспондираат со моделите за климатски промени кои ги предвидуваат идните атмосферски нивоа на CO2.[126] Во 2100 година, моделот предвидува дека потенцијално би можеле да се добие ново на 1.000 ppm, што е во корелација со pH од 7,8 ± 0,05. Резултатите од овој експеримент покажуваат дека кога ларвите се изложени на pH од 7,8 ± 0,05, нивната реакција на знаците на животната средина драстично се разликува од реакцијата на ларвите на знаците во неманипулирана pH вредност. На pH од 7,6 ± 0,05 ларвите немале реакција на било кој тип на знак. Овие резултати ги прикажуваат негативните исходи што веројатно би можеле да бидат иднината за ларвите на морските риби.
Однесување на корални риби
[уреди | уреди извор]Студијата во 2020 година го оспорува потенцијалното негативно влијание на нивото на закиселување на океаните на крајот на векот врз однесувањето на коралните риби и сугерира дека ефектот може да биде занемарлив.[127] Лабораториските експерименти во контролирана средина покажале раст на видовите фитопланктони предизвикани од јаглерод диоксид.[128] Теренската студија на коралниот гребен во Квинсленд и Западна Австралија од 2007 до 2012 година тврди дека коралите се поотпорни на промените на pH на животната средина отколку што се сметло, поради внатрешната регулација на хомеостазата; ова ги прави топлинските промени, наместо закиселувањето, главниот фактор за ранливоста на коралните гребени поради климатските промени.[129]
Влијанијата на екосистемот
[уреди | уреди извор]
Додека целосните импликации на покачениот јаглерод диоксид врз морските екосистеми сè уште се документираат, постои значителен број на истражувања кои покажуваат дека комбинацијата на закиселување на океаните и покачена температура на океаните, предизвикани главно од јаглерод диоксид и други емисии на стакленички гасови, имаат сложен ефект за морскиот живот и океанската средина. Овој ефект далеку го надминува индивидуалното штетно влијание на било кој од нив.[132][133][134] Дополнително, затоплувањето на океаните ја влошува деоксигенацијата на океаните, што е дополнителен стрес за морските организми, со зголемување на стратификацијата на океаните, преку ефектите на густината и растворливоста, со што се ограничуваат хранливите материи,[135][136] додека во исто време се зголемува метаболичката побарувачка.
Анализите ја квантифицирале насоката и големината на штетните ефекти од закиселувањето на океаните, затоплувањето и деоксигенацијата на океанот.[137][138][139] Овие мета-анализи се дополнително тестирани од мезокосмочните студии [140][141] кои откриле катастрофален ефект врз мрежата на морската храна.
Небиолошки влијанија
[уреди | уреди извор]Доколку се тргнат настрана директните биолошки ефекти, се очекува дека закиселувањето на океаните во иднина ќе доведе до значително намалување на закопувањето на карбонатните седименти за неколку векови, па дури и до растворање на постоечките карбонатни седименти.[142] Ова ќе предизвика зголемување на алкалноста на океаните, што ќе доведе до подобрување на океанот како резервоар за CO2 со импликации за климатските промени бидејќи повеќе CO2 ја напушта атмосферата за океанот.[143]
Влијанија врз човечката индустрија
[уреди | уреди извор]Заканата од закиселување вклучува пад на комерцијалниот риболов и на арктичката туристичка индустрија и економија. Комерцијалниот риболов е загрозен бидејќи закиселувањето им штети на калцифицирачките организми кои ја сочинуваат основата на арктичките прехранбени мрежи.
Птероподите и кршливите ѕвезди ја сочинуваат основата на арктичките прехранбени мрежи и и двете се сериозно оштетени од киселоста. Школките на птероподите се раствораат со зголемена киселост и кршливите ѕвезди губат мускулна маса кога повторно растат додатоци.[144] За птероподите да создадат школки, потребен им е арагонит кој се произведува преку карбонатните јони и растворениот калциум. Птероподите се сериозно погодени бидејќи зголемените нивоа на закиселување постојано ја намалуваат количината на вода презаситена со карбонат што е потребна за создавање арагонит.[145] Водите на Арктикот се менуваат толку брзо што ќе станат незаситени со арагонит веќе во 2016 година [145] Дополнително, јајцата на кршливите ѕвезди умираат во рок од неколку дена кога се изложени на очекуваните услови кои произлегуваат од закиселувањето на Арктикот.[146] Закиселувањето се заканува да ги уништи арктичките прехранбени мрежи од основата нагоре. Арктичките прехранбени мрежи се сметаат за едноставни, што значи дека има неколку чекори во синџирот на исхрана од мали организми до поголеми грабливци. На пример, птероподите се „клучен плен на голем број повисоки грабливци - поголеми планктони, риби, морски птици, китови“.[147] И птероподите и морските ѕвезди служат како значителен извор на храна и нивното отстранување од едноставната прехранбена мрежа би претставувало сериозна закана за целиот екосистем. Ефектите врз калцифицирачките организми во основата на прехранбените мрежи може потенцијално да го уништат риболовот. Вредноста на рибата уловена од американскиот комерцијален риболов во 2007 година била проценета на 3,8 милијарди долари и од тие 73% се добиени од калцификатори и нивните директни грабливци.[148] Другите организми се директно оштетени како резултат на закиселување. На пример, намалувањето на растот на морските калцификатори како што се американскиот јастог, океанскиот квахог значи дека има помалку месо од школки достапно за продажба и потрошувачка.[149] Риболовот на црвениот рак е исто така во сериозна закана бидејќи раковите се калцификатори и се потпираат на карбонатните јони за развој на школка. Бебешкиот црвен кралски рак е изложен на зголемени нивоа на киселост и доживеал 100% смртност по 95 денови. Во 2006 година, црвениот крал сочинувал 23% од вкупната жетва, а сериозното намалување на популацијата на црвените ракови ќе ја загрози индустријата за берба на ракови.[150] Неколку океански стоки и услуги веројатно ќе бидат поткопани од идната киселост на океаните што потенцијално ќе влијае на егзистенцијата на околу 400 до 800 милиони луѓе во зависност од сценариото за емисија.[39]
Влијанија врз домородните народи
[уреди | уреди извор]Закиселувањето може да ја оштети туристичката економија на Арктикот и да влијае на начинот на живот на домородните народи. Главниот столб на арктичкиот туризам е спортскиот риболов и ловната индустрија. Индустријата за спортски риболов е загрозена од уривање на прехранбените мрежи кои обезбедуваат храна за ценетите риби. Падот на туризмот го намалува влезот на приходите во областа и ги загрозува економиите кои се повеќе зависни од туризмот.[151] Брзото намалување или исчезнување на морскиот свет може да влијае и на исхраната на домородните народи.
Можни одговори
[уреди | уреди извор]
Намалување на емисиите на стакленички гасови
[уреди | уреди извор]Членовите на Интеракадемскиот панел препорачале до 2050 година, глобалните антропогени емисии на јаглерод диоксид да се намалат за помалку од 50% од нивото од 1990 година.[16] Изјавата од 2009 година [16] исто така ги повикала светските лидери да:
- Признајте дека закиселувањето на океаните е директна и реална последица на зголемувањето на атмосферските концентрации на јаглерод диоксид, веќе има ефект при сегашните концентрации и веројатно ќе предизвика сериозна штета на важните морски екосистеми бидејќи концентрациите на јаглерод диоксид достигнуваат 450 [делови на милион (ppm)] и погоре;
- ... Признајте дека намалувањето на акумулацијата на јаглерод диоксид во атмосферата е единственото практично решение за ублажување на закиселувањето на океаните;
- ... Засилете ги активностите за намалување на стресните фактори, како што се прекумерниот риболов и загадувањето, на морските екосистеми за да се зголеми отпорноста на киселоста на океаните.[152]
Стабилизирањето на концентрациите на јаглерод диоксид во атмосферата на 450 ppm ќе бара краткорочни намалувања на емисиите, со поостри намалувања со текот на времето. [153] Германскиот советодавен совет за глобални промени [154] изјавил:
Со цел да се спречи нарушување на калцификацијата на морските организми и резултирачкиот ризик од фундаментално менување на морските прехранбени мрежи, треба да се почитува следнава заштитна шина: pH вредноста на блиските површински води не треба да падне повеќе од 0,2 единици под просечната вредност пред индустријата. во кој било поголем океански регион (ниту во глобалната средина).
Една цел на политиката поврзана со киселоста на океаните е големината на идното глобално затоплување. Страните на Рамковната конвенција на Обединетите нации за климатски промени (UNFCCC) усвоиле цел за ограничување на затоплувањето на под 2 °C, во однос на прединдустриското ниво.[155] Исполнувањето на оваа цел ќе бара значителни намалувања на антропогените емисии на јаглерод диоксид. [156]
Ограничување на глобалното затоплување на под 2 °C би значело намалување на pH на површината на океаните од 0,16 од прединдустриските нивоа. Ова би претставувало значителен пад на pH на површината на океаните. [157]
На 25 септември 2015 година, USEPA негирала [158] граѓанска петиција од 30 јуни 2015 година [159] со која се барало од ЕПА да го регулира јаглерод диоксидот под закон со цел да се ублажи закиселувањето на океаните. Во негирањето, ЕПА изјавила дека ризиците од закиселување на океаните се „поефикасно и поефективно третирани“ во рамките на домашните активности, на пример, во рамките на Претседателскиот акционен план за климата,[160] и дека се следат повеќе начини за работа со и во други нации да се намалат емисиите и уништувањето на шумите и да се промовира чиста енергија и енергетска ефикасност.
На 28 март 2017 година, САД со извршна наредба го укинале Акциониот план за климата.[161] На 1 јуни 2017 година било објавено дека САД ќе се повлечат од Париските договори [162] и на 12 јуни 2017 година дека САД ќе се воздржат од ветувањето за климатските промени на Г7,[163] два големи меѓународни напори за намалување на емисиите на јаглерод диоксид.
Други решенија како што се зголемување на земјиштето посветено на шумите и поттикнување на растот на морските растенија кои дишат CO2 може да го ублажат закиселувањето на океаните.[164]
Геоинженеринг
[уреди | уреди извор]Геоинженерингот е предложен како можен одговор на закиселувањето на океаните. Изјавата на IAP (2009) [16] вели дека се потребни повеќе истражувања за да се докаже дека ова би било безбедно, достапно и вредно:
Пристапите за ублажување, како што е додавањето хемикалии за да се спротивстават на ефектите од закиселувањето, веројатно ќе бидат скапи, само делумно ефективни и само на локално ниво и може да претставуваат дополнителни неочекувани ризици за морската средина. Имаше многу малку истражувања за изводливоста и влијанијата на овие пристапи. Потребно е суштинско истражување пред да се применат овие техники.
Извештаите на WGBU (2006),[154] Кралското друштво на Обединетото Кралство (2009), [165] и Националниот совет за истражување на САД (2011) [166] предупредиле на потенцијалните ризици и тешкотии поврзани со климатското инженерство.
Железно оплодување
[уреди | уреди извор]Железното оплодување на океанот може да ја стимулира фотосинтезата во фитопланктонот. Фитопланктонот би го претворил растворениот јаглерод диоксид во океанот во јаглехидрати и кислороден гас, од кои некои би потонале во подлабокиот океан пред да оксидираат. Повеќе од десетина експерименти на отворено море потврдиле дека додавањето на железо во океанот ја зголемува фотосинтезата во фитопланктонот до 30 пати.[167] Додека овој пристап е предложен како потенцијално решение за проблемот со киселоста на океаните, ублажувањето на закиселувањето на површинските океани може да ја зголеми закиселувањето во помалку населениот длабок океан.[168]
Извештајот на Кралското друштво на Обединетото Кралство (2009) [165] го прегледал пристапот за делотворност, достапност, навременост и безбедност. Оценката за достапност била „средна“ или „не се очекува да биде многу исплатлива“. За останатите три критериуми, оценките се движеле од „ниска“ до „многу ниска“ (т.е. не е добра). На пример, во однос на безбедноста, извештајот открил „[висок] потенцијал за несакани еколошки несакани ефекти“ и дека оплодувањето на океаните „може да ги зголеми аноксичните региони на океаните („ мртвите зони“)“. [165]
Глобални цели
[уреди | уреди извор]
Проблемот со закиселувањето на океаните е вклучен во една од целите на Обединетите нации: Цел 14 за одржлив развој на:[17] Закиселувањето на океаните директно се решава со целта SDG 14.3. Целосниот наслов на Целта 14.3 е: „Минимизирање и решавање на влијанијата од закиселувањето на океаните, вклучително и преку засилена научна соработка на сите нивоа“.[170] Оваа цел има еден индикатор: Индикатор 14.3.1 е „Просечна киселост на морето (pH) измерена на договорениот пакет на претставителни станици за земање примероци“.[171]
Закиселување во геолошкото минато
[уреди | уреди извор]Закиселувањето на океаните се случило претходно во историјата на Земјата,[18] и резултирачкиот еколошки колапс во океаните имал долготрајни ефекти врз глобалниот циклус на јаглерод и климата.[19][20] Најзабележителен пример е палеоценско-еоценскиот топлински максимум (PETM),[172] кој се случил приближно пред 56 милиони години кога огромни количества јаглерод навлегле во океанот и атмосферата и довело до растворање на карбонатните седименти во сите океански басени.
Три од големите пет настани на масовно истребување во геолошкото минато биле поврзани со брзо зголемување на јаглерод диоксидот во атмосферата, веројатно поради вулканизам и/или топлинска дисоцијација на хидратите на морскиот гас.[173][174] Раните истражувања фокусирани на климатските ефекти на покачените нивоа на јаглерод диоксид врз биолошката разновидност,[175] но во 2004 година, намалената заситеност на CaCO3 поради навлегувањето во морска вода на вулканогениот јаглерод диоксид било предложено како можен механизам за убивање за време на морското масовно изумирање на крајот на Тријас.[176] Крајната тријаска биотска криза сè уште е најдобро воспоставениот пример за морско масовно изумирање поради закиселување на океаните, бидејќи (а) вулканската активност, промените во јаглеродните изотопи, намалувањето на карбонатната седиментација и морското изумирање се совпаднале токму во стратиграфскиот запис,[177][178][179][180] и (б) имало изразена селективност на истребувањето против организми со дебели арагонитни скелети,[177][181][182] што е предвидено од експериментални студии.[91][92][183][184] Закиселувањето на океаните, исто така, е предложено како причина за крајно-пермското масовно изумирање [185][186] и крајната криза во периодот Креда.[187]
Галерија
[уреди | уреди извор]-
„Денешен ден“ (1990-ти) pH на морската површина
-
Денешна алкалност
-
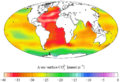
„Денешен ден“ (1990-ти) антропоген CO2 на морската површина
-
Вертикален инвентар на „денешно време“ (1990-ти) антропогени CO2
-
Промена на површинскиот CO2−
3 јони од 1700-тите до 1990-тите -
Денешниот DIC
-
Прединдустриски DIC
Наводи
[уреди | уреди извор]- ↑ 1,0 1,1 1,2 Feely, R. A.; Sabine, C. L.; Hernandez-Ayon, J. M.; Ianson, D.; Hales, B. (June 2008). „Evidence for upwelling of corrosive "acidified" water onto the continental shelf“. Science. 320 (5882): 1490–2. Bibcode:2008Sci...320.1490F. CiteSeerX 10.1.1.328.3181. doi:10.1126/science.1155676. PMID 18497259. Посетено на 2014-01-25 – преку Pacific Marine Environmental Laboratory (PMEL).
- ↑ 2,0 2,1 Caldeira, K.; Wickett, M. E. (2003). „Anthropogenic carbon and ocean pH“. Nature. 425 (6956): 365. Bibcode:2001AGUFMOS11C0385C. doi:10.1038/425365a. PMID 14508477.
- ↑ 3,0 3,1 „Ocean acidification | National Oceanic and Atmospheric Administration“. www.noaa.gov. Посетено на 2020-09-07.
- ↑ „Ocean Acidification“. www.whoi.edu/ (англиски). Посетено на 2021-09-13.
- ↑ Jacobson, M. Z. (2005). „Studying ocean acidification with conservative, stable numerical schemes for nonequilibrium air-ocean exchange and ocean equilibrium chemistry“. Journal of Geophysical Research: Atmospheres. 110: D07302. Bibcode:2005JGRD..11007302J. doi:10.1029/2004JD005220.
- ↑ Hall-Spencer, J. M.; Rodolfo-Metalpa, R.; Martin, S.; и др. (July 2008). „Volcanic carbon dioxide vents show ecosystem effects of ocean acidification“. Nature. 454 (7200): 96–9. Bibcode:2008Natur.454...96H. doi:10.1038/nature07051. PMID 18536730.
|hdl-access=бара|hdl=(help) - ↑ 7,0 7,1 „Report of the Ocean Acidification and Oxygen Working Group, International Council for Science's Scientific Committee on Ocean Research (SCOR) Biological Observatories Workshop“ (PDF).
- ↑ US EPA, OAR (2016-06-27). „Climate Change Indicators: Ocean Acidity“. www.epa.gov (англиски). Посетено на 2021-09-03.
- ↑ Doney, Scott C.; Fabry, Victoria J.; Feely, Richard A.; Kleypas, Joan A. (2009). „Ocean Acidification: The Other CO 2 Problem“. Annual Review of Marine Science (англиски). 1 (1): 169–192. Bibcode:2009ARMS....1..169D. doi:10.1146/annurev.marine.010908.163834. ISSN 1941-1405. PMID 21141034. Архивирано од изворникот на 2022-02-25. Посетено на 2022-02-21.
- ↑ Anthony, KRN; и др. (2008). „Ocean acidification causes bleaching and productivity loss in coral reef builders“. Proceedings of the National Academy of Sciences. 105 (45): 17442–17446. Bibcode:2008PNAS..10517442A. doi:10.1073/pnas.0804478105. PMC 2580748. PMID 18988740.
- ↑ Rivera, Hanny E.; Chan, Andrea N.; Luu, Victoria (2020-08-05). „Coral reefs are critical for our food supply, tourism, and ocean health. We can protect them from climate change“. MIT Science Policy Review (англиски). Посетено на 2021-09-03.
- ↑ Kump, L.R.; Bralower, T.J.; Ridgwell, A. (2009). „Ocean acidification in deep time“. Oceanography. 22: 94–107. doi:10.5670/oceanog.2009.10. Посетено на 16 May 2016.
- ↑ 13,0 13,1 13,2 13,3 13,4 Orr, James C.; и др. (2005). „Anthropogenic ocean acidification over the twenty-first century and its impact on calcifying organisms“ (PDF). Nature. 437 (7059): 681–686. Bibcode:2005Natur.437..681O. doi:10.1038/nature04095. PMID 16193043. Архивирано од изворникот (PDF) на 25 June 2008.
- ↑ Cornelia Dean (30 January 2009). „Rising Acidity Is Threatening Food Web of Oceans, Science Panel Says“. New York Times.
- ↑ Robert E. Service (13 July 2012). „Rising Acidity Brings and Ocean Of Trouble“. Science. 337 (6091): 146–148. Bibcode:2012Sci...337..146S. doi:10.1126/science.337.6091.146. PMID 22798578.
- ↑ 16,0 16,1 16,2 16,3 IAP (June 2009). „Interacademy Panel (IAP) Member Academies Statement on Ocean Acidification“., Secretariat: TWAS (the Academy of Sciences for the Developing World), Trieste, Italy.
- ↑ 17,0 17,1 „Goal 14 targets“. UNDP (англиски). Посетено на 2020-09-24.
- ↑ 18,0 18,1 Zeebe, R.E. (2012). „History of Seawater Carbonate Chemistry, Atmospheric CO2, and Ocean Acidification“. Annual Review of Earth and Planetary Sciences. 40 (1): 141–165. Bibcode:2012AREPS..40..141Z. doi:10.1146/annurev-earth-042711-105521.
- ↑ 19,0 19,1 Henehan, Michael J.; Ridgwell, Andy; Thomas, Ellen; Zhang, Shuang; Alegret, Laia; Schmidt, Daniela N.; Rae, James W. B.; Witts, James D.; Landman, Neil H. (2019-10-17). „Rapid ocean acidification and protracted Earth system recovery followed the end-Cretaceous Chicxulub impact“. Proceedings of the National Academy of Sciences. 116 (45): 22500–22504. Bibcode:2019PNAS..11622500H. doi:10.1073/pnas.1905989116. ISSN 0027-8424. PMC 6842625. PMID 31636204.
- ↑ 20,0 20,1 Carrington, Damian (2019-10-21). „Ocean acidification can cause mass extinctions, fossils reveal“. The Guardian. ISSN 0261-3077. Посетено на 2019-10-22.
- ↑ Raven, J. A.; Falkowski, P. G. (1999). „Oceanic sinks for atmospheric CO2“. Plant, Cell & Environment. 22 (6): 741–755. doi:10.1046/j.1365-3040.1999.00419.x.
- ↑ Cramer, W.; и др. (2001). „Global response of terrestrial ecosystem structure and function to CO2 and climate change: results from six dynamic global vegetation models“. Global Change Biology. 7 (4): 357–373. Bibcode:2001GCBio...7..357C. doi:10.1046/j.1365-2486.2001.00383.x.
- ↑ 23,0 23,1 Feely, R. A.; Sabine, C. L.; Lee, K.; Berelson, W.; Kleypas, J.; Fabry, V. J.; Millero, F. J. (July 2004). „Impact of Anthropogenic CO2on the CaCO3 System in the Oceans“. Science. 305 (5682): 362–366. Bibcode:2004Sci...305..362F. doi:10.1126/science.1097329. PMID 15256664. Посетено на 2014-01-25 – преку Pacific Marine Environmental Laboratory (PMEL).
- ↑ Woods Hole Oceanographic Institution (August 2016). „Changes in Aragonite Saturation of the World's Oceans, 1880–2015“. epa.gov.
- ↑ Kump, Lee R.; Kasting, James F.; Crane, Robert G. (2003). The Earth System (2. изд.). Upper Saddle River: Prentice Hall. стр. 162–164. ISBN 978-0-613-91814-5.
- ↑ 26,0 26,1 „Ocean Acidification Is Climate Change's 'Equally Evil Twin,' NOAA Chief Says“. Huffington Post. 9 July 2012. Архивирано од изворникот на 12 July 2012. Посетено на 2012-07-09.
- ↑ 27,0 27,1 Nina Notman (29 July 2014). „The other carbon dioxide problem“. Chemistry World.
- ↑ Alex Rogers (9 October 2013). „Global warming's evil twin: ocean acidification“. The Conversation.
- ↑ 29,0 29,1 Hennige, S.J. (2014). „Short-term metabolic and growth responses of the cold-water coral Lophelia pertusa to ocean acidification“. Deep-Sea Research Part II. 99: 27–35. Bibcode:2014DSRII..99...27H. doi:10.1016/j.dsr2.2013.07.005.
- ↑ Pelejero, C. (2010). „Paleo-perspectives on ocean acidification“. Trends in Ecology and Evolution. 25 (6): 332–344. doi:10.1016/j.tree.2010.02.002. PMID 20356649.
- ↑ Doney, S.C. (2009). „Ocean Acidification: The Other CO2 Problem“. Annual Review of Marine Science. 1: 169–192. Bibcode:2009ARMS....1..169D. doi:10.1146/annurev.marine.010908.163834. PMID 21141034.
- ↑ „Ocean acidification (Issues Brief)“ (PDF). IUCN (International Union for Conservation of Nature). November 2017. Архивирано од изворникот (PDF) на 2020-12-30. Посетено на 3 November 2020.
- ↑ Gies, E. (11 January 2018). „Like Oceans, Freshwater Is Also Acidifying“. Scientific American. Посетено на 2018-01-13.
- ↑ Weiss, L. C.; Pötter, L.; Steiger, A.; Kruppert, S.; Frost, U.; Tollrian, R. (2018). „Rising pCO2 in Freshwater Ecosystems Has the Potential to Negatively Affect Predator-Induced Defenses in Daphnia“. Current Biology. 28 (2): 327–332.e3. doi:10.1016/j.cub.2017.12.022. PMID 29337079.
- ↑ Millero, Frank J. (1995). „Thermodynamics of the carbon dioxide system in the oceans“. Geochimica et Cosmochimica Acta. 59 (4): 661–677. Bibcode:1995GeCoA..59..661M. doi:10.1016/0016-7037(94)00354-O.
- ↑ Paul Freund; Stefan Bachu; Dale Simbeck; Kelly (Kailai) Thambimuthu; Murlidhar Gupta (2005). „Annex I: Properties of CO2 and carbon-based fuels“. Во Bert Metz; Ogunlade Davidson; Heleen de Coninck; Manuela Loos; Leo Meyer (уред.). IPCC Special Report on Carbon Dioxide Capture and Storage (PDF). IPCC. стр. 390. Архивирано од изворникот (PDF) на 10 February 2010. Посетено на 1 November 2014.
- ↑ Sabine, C. L. (2004). „The Oceanic Sink for Anthropogenic CO2“. Science (англиски). 305 (5682): 367–371. Bibcode:2004Sci...305..367S. doi:10.1126/science.1097403. ISSN 0036-8075. PMID 15256665.
- ↑ „Ocean Acidification“. www.oceanscientists.org. Посетено на 2018-12-11.
- ↑ 39,0 39,1 39,2 Mora, C.; и др. (2013). „Biotic and Human Vulnerability to Projected Changes in Ocean Biogeochemistry over the 21st Century“. PLOS Biology. 11 (10): e1001682. doi:10.1371/journal.pbio.1001682. PMC 3797030. PMID 24143135.
- ↑ Bows, Kevin; Bows, Alice (2011). „Beyond 'dangerous' climate change: emission scenarios for a new world“. Philosophical Transactions of the Royal Society A. 369 (1934): 20–44. Bibcode:2011RSPTA.369...20A. doi:10.1098/rsta.2010.0290. PMID 21115511.
- ↑ Turley, C. (2008). „Impacts of changing ocean chemistry in a high-CO2 world“. Mineralogical Magazine. 72 (1): 359–362. Bibcode:2008MinM...72..359T. doi:10.1180/minmag.2008.072.1.359.
- ↑ 42,0 42,1 Key, R. M.; Kozyr, A.; Sabine, C. L.; Lee, K.; Wanninkhof, R.; Bullister, J.; Feely, R. A.; Millero, F.; Mordy, C. (2004). „A global ocean carbon climatology: Results from GLODAP“. Global Biogeochemical Cycles. 18 (4): GB4031. Bibcode:2004GBioC..18.4031K. doi:10.1029/2004GB002247.

- ↑ „Ocean acidification and the Southern Ocean“. Australian Antarctic Division — Australia in Antarctica.
- ↑ „EPA weighs action on ocean acidification“. 4 February 2009.
- ↑ 45,0 45,1 Carstensen, Jacob; Duarte, Carlos M. (2019-04-16). „Drivers of pH Variability in Coastal Ecosystems“. Environmental Science & Technology. 53 (8): 4020–4029. Bibcode:2019EnST...53.4020C. doi:10.1021/acs.est.8b03655. ISSN 0013-936X. PMID 30892892.
- ↑ Duarte, Carlos M.; Hendriks, Iris E.; Moore, Tommy S.; Olsen, Ylva S.; Steckbauer, Alexandra; Ramajo, Laura; Carstensen, Jacob; Trotter, Julie A.; McCulloch, Malcolm (2013-03-01). „Is Ocean Acidification an Open-Ocean Syndrome? Understanding Anthropogenic Impacts on Seawater pH“. Estuaries and Coasts (англиски). 36 (2): 221–236. doi:10.1007/s12237-013-9594-3. ISSN 1559-2731.
- ↑ Lowe, Alexander T.; Bos, Julia; Ruesink, Jennifer (2019-01-30). „Ecosystem metabolism drives pH variability and modulates long-term ocean acidification in the Northeast Pacific coastal ocean“. Scientific Reports (англиски). 9 (1): 963. Bibcode:2019NatSR...9..963L. doi:10.1038/s41598-018-37764-4. ISSN 2045-2322. PMC 6353961. PMID 30700764.
- ↑ Dong, Xu; Huang, Haining; Zheng, Nan; Zhang, Junpeng; Wang, Sumin; Zhou, Kaiwen; Zhang, Yuanbiao; Ji, Weidong; Lin, Hui (2021-02-05). „Role of biological activity in mediating acidification in a coastal upwelling zone at the east coast of Hainan Island“. Estuarine, Coastal and Shelf Science (англиски). 249: 107124. Bibcode:2021ECSS..24907124D. doi:10.1016/j.ecss.2020.107124. ISSN 0272-7714.
- ↑ Ruesink, Jennifer L.; Yang, Sylvia; Trimble, Alan C. (2015-11-01). „Variability in Carbon Availability and Eelgrass (Zostera marina) Biometrics Along an Estuarine Gradient in Willapa Bay, WA, USA“. Estuaries and Coasts (англиски). 38 (6): 1908–1917. doi:10.1007/s12237-014-9933-z. ISSN 1559-2731.
- ↑ Fairchild, William; Hales, Burke (2021). „High-Resolution Carbonate System Dynamics of Netarts Bay, OR From 2014 to 2019“. Frontiers in Marine Science (англиски). 7. doi:10.3389/fmars.2020.590236. ISSN 2296-7745.
- ↑ Cited in Tim Flannery, Atmosphere of Hope. Solutions to the Climate Crisis, Penguin Books, 2015, page 47 (ISBN 9780141981048).
- ↑ Wootton, J. T.; Pfister, C. A.; Forester, J. D. (2008). „Dynamic patterns and ecological impacts of declining ocean pH in a high-resolution multi-year dataset“. Proceedings of the National Academy of Sciences. 105 (48): 18848–18853. Bibcode:2008PNAS..10518848W. doi:10.1073/pnas.0810079105. PMC 2596240. PMID 19033205.
- ↑ „Ocean Growing More Acidic Faster Than Once Thought; Increasing Acidity Threatens Sea Life“. Science Daily. 2008-11-26. Посетено на 26 November 2008.
- ↑ „Rate of ocean acidification the fastest in 65 million years“. Physorg.com. 2010-02-14. Посетено на 2013-08-29.
- ↑ Joel, Lucas (21 October 2019). „The Dinosaur-Killing Asteroid Acidified the Ocean in a Flash - The Chicxulub event was as damaging to life in the oceans as it was to creatures on land, a study shows“. The New York Times. Посетено на 22 October 2019.
- ↑ Henehan, Michael J.; и др. (21 October 2019). „Rapid ocean acidification and protracted Earth system recovery followed the end-Cretaceous Chicxulub impact“. Proceedings of the National Academy of Sciences of the United States of America. 116 (45): 22500–22504. Bibcode:2019PNAS..11622500H. doi:10.1073/pnas.1905989116. PMC 6842625. PMID 31636204.
- ↑ „An Ominous Warning on the Effects of Ocean Acidification by Carl Zimmer: Yale Environment 360“. e360.yale.edu. Архивирано од изворникот на 16 February 2014. Посетено на 2014-01-25.
- ↑ Newspapers, Les Blumenthal-McClatchy (2010-04-22). „Report: Ocean acidification rising at unprecedented rate“. mcclatchydc.
- ↑ United States National Research Council, 2010. Ocean Acidification: A National Strategy to Meet the Challenges of a Changing Ocean Архивирано на 14 јануари 2014 г.
- ↑ „The Geological Record of Ocean Acidification“. JournalistsResource.org, retrieved 14 March 2012
- ↑ Hönisch, Bärbel; Ridgwell, Andy; Schmidt, Daniela N.; Thomas, E.; Gibbs, S. J.; Sluijs, A.; Zeebe, R.; Kump, L.; Martindale, R. C. (2012). „The Geological Record of Ocean Acidification“. Science. 335 (6072): 1058–1063. Bibcode:2012Sci...335.1058H. doi:10.1126/science.1208277. PMID 22383840.
- ↑ David (2 July 2005). „The Acid Ocean – the Other Problem with CO2 Emission“. Real Climate.
- ↑ Marah J. Hardt; Carl Safina (9 August 2010). „How Acidification Threatens Oceans from the Inside Out“. Scientific American. Архивирано од изворникот на 2010-12-26.
- ↑ Fiona Harvey (2013-08-25). „Rising levels of acids in seas may endanger marine life, says study“. The Guardian. Посетено на 2013-08-29.
- ↑ Harrabin, Roger (3 July 2015). „CO2 emissions threaten ocean crisis“. BBC News.
- ↑ 66,0 66,1 Humphreys, M. P. (2016). „Climate sensitivity and the rate of ocean acidification: future impacts, and implications for experimental design“. ICES Journal of Marine Science. 74 (4): 934–940. doi:10.1093/icesjms/fsw189.
- ↑ Olafsson, J.; Olafsdottir, S. R.; Benoit-Cattin, A.; Danielsen, M.; Arnarson, T. S.; Takahashi, T. (25 November 2009). „Rate of Iceland Sea acidification from time series measurements“. Biogeosciences. 6 (11): 2661–2668. Bibcode:2009BGeo....6.2661O. doi:10.5194/bg-6-2661-2009.
- ↑ Midorikawa, Takashi; Inoue, Hisayuki Y.; Ishii, Masao; Sasano, Daisuke; Kosugi, Naohiro; Hashida, Gen; Nakaoka, Shin-ichiro; Suzuki, Toru (March 2012). „Decreasing pH trend estimated from 35-year time series of carbonate parameters in the Pacific sector of the Southern Ocean in summer“. Deep Sea Research Part I: Oceanographic Research Papers. 61: 131–139. Bibcode:2012DSRI...61..131M. doi:10.1016/j.dsr.2011.12.003.
- ↑ González-Dávila, M.; Santana-Casiano, J. M.; Rueda, M. J.; Llinás, O. (11 October 2010). „The water column distribution of carbonate system variables at the ESTOC site from 1995 to 2004“. Biogeosciences. 7 (10): 3067–3081. Bibcode:2010BGeo....7.3067G. doi:10.5194/bg-7-3067-2010.
- ↑ Dore, J. E.; Lukas, R.; Sadler, D. W.; Church, M. J.; Karl, D. M. (28 July 2009). „Physical and biogeochemical modulation of ocean acidification in the central North Pacific“. Proceedings of the National Academy of Sciences. 106 (30): 12235–12240. doi:10.1073/pnas.0906044106. PMC 2716384. PMID 19666624.
- ↑ Bates, N. R.; Best, M. H. P.; Neely, K.; Garley, R.; Dickson, A. G.; Johnson, R. J. (11 July 2012). „Detecting anthropogenic carbon dioxide uptake and ocean acidification in the North Atlantic Ocean“. Biogeosciences. 9 (7): 2509–2522. Bibcode:2012BGeo....9.2509B. doi:10.5194/bg-9-2509-2012.
- ↑ Pelejero, Carles; Calvo, Eva; McCulloch, Malcolm T.; Marshall, John F.; Gagan, Michael K.; Lough, Janice M.; Opdyke, Bradley N. (30 September 2005). „Preindustrial to Modern Interdecadal Variability in Coral Reef pH“. Science. 309 (5744): 2204–2207. Bibcode:2005Sci...309.2204P. doi:10.1126/science.1113692. PMID 16195458.
- ↑ Bialik, Or M.; Sisma-Ventura, Guy (December 2016). „Proxy-based reconstruction of surface water acidification and carbonate saturation of the Levant Sea during the Anthropocene“. Anthropocene. 16: 42–53. doi:10.1016/j.ancene.2016.08.001.
- ↑ Mora, Camilo; Frazier, Abby G.; Longman, Ryan J.; Dacks, Rachel S.; Walton, Maya M.; Tong, Eric J.; Sanchez, Joseph J.; Kaiser, Lauren R.; Stender, Yuko O. (2013-10-10). „The projected timing of climate departure from recent variability“. Nature (англиски). 502 (7470): 183–187. Bibcode:2013Natur.502..183M. doi:10.1038/nature12540. ISSN 0028-0836. PMID 24108050.
- ↑ Cummings, Vonda; Hewitt, Judi; Van Rooyen, Anthony; Currie, Kim; Beard, Samuel; Thrush, Simon; Norkko, Joanna; Barr, Neill; Heath, Philip (2011). Gilbert, Jack Anthony (уред.). „Ocean Acidification at High Latitudes: Potential Effects on Functioning of the Antarctic Bivalve Laternula elliptica“. PLOS ONE (англиски). 6 (1): e16069. Bibcode:2011PLoSO...616069C. doi:10.1371/journal.pone.0016069. ISSN 1932-6203. PMC 3016332. PMID 21245932.
- ↑ Sosdian, S. M.; Lear, C. H. (2020). „Initiation of the Western Pacific Warm Pool at the Middle Miocene Climate Transition?“. Paleoceanography and Paleoclimatology (англиски). 35 (12): 3920. Bibcode:2020PaPa...35.3920S. doi:10.1029/2020PA003920. ISSN 2572-4517.
- ↑ McNeil BI; Matear RJ (December 2, 2008), „Southern Ocean acidification: A tipping point at 450-ppm atmospheric CO2“, Proceedings of the National Academy of Sciences, 105 (48): 18860–4, Bibcode:2008PNAS..10518860M, doi:10.1073/pnas.0806318105, PMC 2596239, PMID 19022908
- ↑ „UN: Oceans are 30 percent more acidic than before fossil fuels“. Архивирано од изворникот на 3 January 2011.
- ↑ Gattuso, Jean-Pierre; Mach, Katharine J.; Morgan, Granger (April 2013). „Ocean acidification and its impacts: an expert survey“. Climatic Change. 117 (4): 725–738. Bibcode:2013ClCh..117..725G. doi:10.1007/s10584-012-0591-5. ISSN 0165-0009.[мртва врска]
- ↑ 80,0 80,1 80,2 80,3 80,4 Raven, JA, et al. (2005) "Ocean acidification due to increasing atmospheric carbon dioxide". Royal Society, London, UK.
- ↑ Mitchell, M. J.; и др. (2010). „A model of carbon dioxide dissolution and mineral carbonation kinetics“. Proceedings of the Royal Society A. 466 (2117): 1265–1290. Bibcode:2010RSPSA.466.1265M. doi:10.1098/rspa.2009.0349.
- ↑ Thurman, H.V.; Trujillo, A.P. (2004). Introductory Oceanography. Prentice Hall. ISBN 978-0-13-143888-0.
- ↑ The Royal Society. Ocean Acidification Due To Increasing Atmospheric Carbon Dioxide, The Clyvedon Press Ltd. (2005): 11.
- ↑ Marubini, F.; Ferrier-Pagès, C.; Furla, P.; Allemand, D. (2008). „Coral calcification responds to seawater acidification: a working hypothesis towards a physiological mechanism“. Coral Reefs. 27 (3): 491–499. Bibcode:2008CorRe..27..491M. doi:10.1007/s00338-008-0375-6.
- ↑ 85,0 85,1 Rosa, R.; Seibel, B. (2008). „Synergistic effects of climate-related variables suggest future physiological impairment in a top oceanic predator“. PNAS. 105 (52): 20776–20780. Bibcode:2008PNAS..10520776R. doi:10.1073/pnas.0806886105. PMC 2634909. PMID 19075232.
- ↑ 86,0 86,1 Bibby, R.; и др. (2008). „Effects of ocean acidification on the immune response of the blue mussel Mytilus edulis“. Aquatic Biology. 2: 67–74. doi:10.3354/ab00037.
- ↑ „Ocean Acidification Summary for Policymakers“. IGBP.
- ↑ „Special Report on the Ocean and Cryosphere in a Changing Climate — Special Report on the Ocean and Cryosphere in a Changing Climate“. IPCC. 2019-09-25. Посетено на 2019-11-12.
- ↑ Day, Jon C.; Heron, Scott F. „'Severely threatened and deteriorating': global authority on nature lists the Great Barrier Reef as critical“. The Conversation (англиски). Посетено на 2021-09-03.
- ↑ Nienhuis, S.; Palmer, A.; Harley, C. (2010). „Elevated CO2 affects shell dissolution rate but not calcification rate in a marine snail“. Proceedings of the Royal Society B. 277 (1693): 2553–2558. doi:10.1098/rspb.2010.0206. PMC 2894921. PMID 20392726.
- ↑ 91,0 91,1 Gattuso, J.-P.; Frankignoulle, M.; Bourge, I.; Romaine, S.; Buddemeier, R. W. (1998). „Effect of calcium carbonate saturation of seawater on coral calcification“. Global and Planetary Change. 18 (1–2): 37–46. Bibcode:1998GPC....18...37G. doi:10.1016/S0921-8181(98)00035-6. Архивирано од изворникот на 2019-07-20. Посетено на 2022-02-21.
- ↑ 92,0 92,1 Gattuso, J.-P.; Allemand, D.; Frankignoulle, M. (1999). „Photosynthesis and calcification at cellular, organismal and community levels in coral reefs: a review on interactions and control by carbonate chemistry“. American Zoologist. 39: 160–183. doi:10.1093/icb/39.1.160. Архивирано од изворникот на 2019-07-20. Посетено на 2022-02-21.
- ↑ Langdon, C.; Atkinson, M. J. (2005). „Effect of elevated pCO2 on photosynthesis and calcification of corals and interactions with seasonal change in temperature/irradiance and nutrient enrichment“. Journal of Geophysical Research. 110 (C09S07): C09S07. Bibcode:2005JGRC..11009S07L. doi:10.1029/2004JC002576.
- ↑ D'Olivo, Juan P.; Ellwood, George; DeCarlo, Thomas M.; McCulloch, Malcolm T. (2019-11-15). „Deconvolving the long-term impacts of ocean acidification and warming on coral biomineralisation“. Earth and Planetary Science Letters. 526: 115785. Bibcode:2019E&PSL.52615785D. doi:10.1016/j.epsl.2019.115785. ISSN 0012-821X.
- ↑ Riebesell, Ulf; Zondervan, Ingrid; Rost, Björn; Tortell, Philippe D.; Zeebe, Richard E.; Morel, François M. M. (2000). „Reduced calcification of marine plankton in response to increased atmospheric CO2“ (PDF). Nature. 407 (6802): 364–367. Bibcode:2000Natur.407..364R. doi:10.1038/35030078. PMID 11014189.
- ↑ Zondervan, I.; Zeebe, R. E.; Rost, B.; Rieblesell, U. (2001). „Decreasing marine biogenic calcification: a negative feedback on rising atmospheric CO2“ (PDF). Global Biogeochemical Cycles. 15 (2): 507–516. Bibcode:2001GBioC..15..507Z. doi:10.1029/2000GB001321.
- ↑ Zondervan, I.; Rost, B.; Rieblesell, U. (2002). „Effect of CO2 concentration on the PIC/POC ratio in the coccolithophore Emiliania huxleyi grown under light limiting conditions and different day lengths“ (PDF). Journal of Experimental Marine Biology and Ecology. 272 (1): 55–70. doi:10.1016/S0022-0981(02)00037-0.
- ↑ Delille, B.; Harlay, J.; Zondervan, I.; Jacquet, S.; Chou, L.; Wollast, R.; Bellerby, R.G.J.; Frankignoulle, M.; Borges, A.V. (2005). „Response of primary production and calcification to changes of pCO2 during experimental blooms of the coccolithophorid Emiliania huxleyi“. Global Biogeochemical Cycles. 19 (2): GB2023. Bibcode:2005GBioC..19.2023D. doi:10.1029/2004GB002318. Архивирано од изворникот на 2019-07-20. Посетено на 2022-02-21.
- ↑ Kuffner, I. B.; Andersson, A. J.; Jokiel, P. L.; Rodgers, K. S.; Mackenzie, F. T. (2007). „Decreased abundance of crustose coralline algae due to ocean acidification“. Nature Geoscience. 1 (2): 114–117. Bibcode:2008NatGe...1..114K. doi:10.1038/ngeo100.
- ↑ Phillips, Graham; Chris Branagan (2007-09-13). „Ocean Acidification – The BIG global warming story“. ABC TV Science: Catalyst. Australian Broadcasting Corporation. Посетено на 2007-09-18.
- ↑ Gazeau, F.; Quiblier, C.; Jansen, J. M.; Gattuso, J.-P.; Middelburg, J. J.; Heip, C. H. R. (2007). „Impact of elevated CO2 on shellfish calcification“. Geophysical Research Letters. 34 (7): L07603. Bibcode:2007GeoRL..3407603G. doi:10.1029/2006GL028554. Архивирано од изворникот на 2019-07-20. Посетено на 2022-02-21.
|hdl-access=бара|hdl=(help) - ↑ Comeau, C.; Gorsky, G.; Jeffree, R.; Teyssié, J.-L.; Gattuso, J.-P. (2009). „Impact of ocean acidification on a key Arctic pelagic mollusc ("Limacina helicina")“. Biogeosciences. 6 (9): 1877–1882. Bibcode:2009BGeo....6.1877C. doi:10.5194/bg-6-1877-2009.
- ↑ Buitenhuis, E. T.; de Baar, H. J. W.; Veldhuis, M. J. W. (1999). „Photosynthesis and calcification by Emiliania huxleyi (Prymnesiophyceae) as a function of inorganic carbon species“. Journal of Phycology. 35 (5): 949–959. doi:10.1046/j.1529-8817.1999.3550949.x.
- ↑ Nimer, N. A.; Merrett, M. J. (1993). „Calcification rate in Emiliania huxleyi Lohmann in response to light, nitrate and availability of inorganic carbon“. New Phytologist. 123 (4): 673–677. doi:10.1111/j.1469-8137.1993.tb03776.x.
- ↑ 105,0 105,1 Iglesias-Rodriguez, M.D.; Halloran, P.R.; Rickaby, R.E.M.; Hall, I.R.; Colmenero-Hidalgo, E.; Gittins, J.R.; Green, D.R.H.; Tyrrell, T.; Gibbs, S.J. (2008). „Phytoplankton Calcification in a High-CO2 World“. Science. 320 (5874): 336–340. Bibcode:2008Sci...320..336I. doi:10.1126/science.1154122. PMID 18420926.
- ↑ Sciandra, A.; Harlay, J.; Lefevre, D.; и др. (2003). „Response of coccolithophorid Emiliania huxleyi to elevated partial pressure of CO2 under nitrogen limitation“. Marine Ecology Progress Series. 261: 111–112. Bibcode:2003MEPS..261..111S. doi:10.3354/meps261111.
- ↑ Langer, G.; Geisen, M.; Baumann, K. H.; и др. (2006). „Species-specific responses of calcifying algae to changing seawater carbonate chemistry“ (PDF). Geochemistry, Geophysics, Geosystems. 7 (9): Q09006. Bibcode:2006GGG.....709006L. doi:10.1029/2005GC001227.
- ↑ Ruttiman, J. (2006). „Sick Seas“. Nature. 442 (7106): 978–980. Bibcode:2006Natur.442..978R. doi:10.1038/442978a. PMID 16943816.
- ↑ Cohen, A.; Holcomb, M. (2009). „Why Corals Care About Ocean Acidification: Uncovering the Mechanism“. Oceanography. 24 (4): 118–127. doi:10.5670/oceanog.2009.102.
- ↑ Pérez, F.; Fontela, M.; García-Ibañez, M.; Mercier, H.; Velo, A.; Lherminier, P.; Zunino, P.; de la Paz, M.; Alonso, F. (22 February 2018). „Meridional overturning circulation conveys fast acidification to the deep Atlantic Ocean“. Nature. 554 (7693): 515–518. Bibcode:2018Natur.554..515P. doi:10.1038/nature25493. PMID 29433125.
- ↑ Mollica, Nathaniel R.; Guo, Weifu; Cohen, Anne L.; Huang, Kuo-Fang; Foster, Gavin L.; Donald, Hannah K.; Solow, Andrew R. (20 February 2018). „Ocean acidification affects coral growth by reducing skeletal density“. Proceedings of the National Academy of Sciences. 115 (8): 1754–1759. Bibcode:2018PNAS..115.1754M. doi:10.1073/pnas.1712806115. PMC 5828584. PMID 29378969.
- ↑ Albright, R.; Caldeira, L.; Hosfelt, J.; Kwiatkowski, L.; Maclaren, J. K.; Mason, B. M.; Nebuchina, Y.; Ninokawa, A.; Pongratz, J. (24 February 2016). „Reversal of ocean acidification enhances net coral reef calcification“. Nature. 531 (7594): 362–365. Bibcode:2016Natur.531..362A. doi:10.1038/nature17155. PMID 26909578.
- ↑ Albright, R.; Takeshita, T.; Koweek, D. A.; Ninokawa, A.; Wolfe, K.; Rivlin, T.; Nebuchina, Y.; Young, J.; Caldeira, K. (14 March 2018). „Carbon dioxide addition to coral reef waters suppresses net community calcification“. Nature. 555 (7697): 516–519. Bibcode:2018Natur.555..516A. doi:10.1038/nature25968. PMID 29539634.
- ↑ Hannah L. Wood; John I. Spicer; Stephen Widdicombe (2008). „Ocean acidification may increase calcification rates, but at a cost“. Proceedings of the Royal Society B. 275 (1644): 1767–1773. doi:10.1098/rspb.2008.0343. PMC 2587798. PMID 18460426.
- ↑ Ducker, James; Falkenberg, Laura J. (2020). „How the Pacific Oyster Responds to Ocean Acidification: Development and Application of a Meta-Analysis Based Adverse Outcome Pathway“. Frontiers in Marine Science (англиски). 7. doi:10.3389/fmars.2020.597441. ISSN 2296-7745.
- ↑ Fabricius, Katharina (2011). „Losers and winners in coral reefs acclimatized to elevated carbon dioxide concentrations“. Nature Climate Change. 1 (3): 165–169. Bibcode:2011NatCC...1..165F. doi:10.1038/nclimate1122.
- ↑ Henehan, Michael J.; Ridgwell, Andy; Thomas, Ellen; Zhang, Shuang; Alegret, Laia; Schmidt, Daniela N.; Rae, James W. B.; Witts, James D.; Landman, Neil H. (2019-11-05). „Rapid ocean acidification and protracted Earth system recovery followed the end-Cretaceous Chicxulub impact“. Proceedings of the National Academy of Sciences. 116 (45): 22500–22504. Bibcode:2019PNAS..11622500H. doi:10.1073/pnas.1905989116. ISSN 0027-8424. PMC 6842625. PMID 31636204.
- ↑ Petrou, Katherina; Nielsen, Daniel (2019-08-27). „Acid oceans are shrinking plankton, fueling faster climate change“. phys.org. Посетено на 2019-11-12.
- ↑ Hester, K. C.; и др. (2008). „Unanticipated consequences of ocean acidification: A noisier ocean at lower pH“. Geophysical Research Letters. 35 (19): L19601. Bibcode:2008GeoRL..3519601H. doi:10.1029/2008GL034913.
- ↑ Acid In The Oceans: A Growing Threat To Sea Life by Richard Harris. All Things Considered, 12 August 2009.
- ↑ Kwok, Roberta (4 June 2013). „Ocean acidification could make squid develop abnormally“. University of Washington. Посетено на 2013-08-24.
- ↑ „Swiss marine researcher moving in for the krill“. The Australian. 2008. Архивирано од изворникот на 11 December 2008. Посетено на 28 September 2008.
- ↑ „Ocean Acidification Promotes Disruptive and Harmful Algal Blooms on Our Coasts“. 2014.
- ↑ 124,0 124,1 Turley, Carol; Gattuso, Jean-Pierre (July 2012). „Future biological and ecosystem impacts of ocean acidification and their socioeconomic-policy implications“. Current Opinion in Environmental Sustainability. 4 (3): 278–286. doi:10.1016/j.cosust.2012.05.007.
- ↑ Gooding, R.; и др. (2008). „Elevated water temperature and carbon dioxide concentration increase the growth of a keystone echinoderm“. Proceedings of the National Academy of Sciences. 106 (23): 9316–21. Bibcode:2009PNAS..106.9316G. doi:10.1073/pnas.0811143106. PMC 2695056. PMID 19470464.
- ↑ 126,0 126,1 126,2 Munday, Philip L. (2009). „Ocean Acidification Impairs Olfactory Discrimination and Homing Ability of a Marine Fish“ (PDF). Proceedings of the National Academy of Sciences. 106 (6): 1848–52. Bibcode:2009PNAS..106.1848M. doi:10.1073/pnas.0809996106. PMC 2644126. PMID 19188596. Архивирано од изворникот (PDF) на 2022-02-25. Посетено на 2022-02-22.
- ↑ Clark, Timothy D.; Raby, Graham D.; Roche, Dominique G.; Binning, Sandra A.; Speers-Roesch, Ben; Jutfelt, Fredrik; Sundin, Josefin (January 2020). „Ocean acidification does not impair the behaviour of coral reef fishes“. Nature (англиски). 577 (7790): 370–375. Bibcode:2020Natur.577..370C. doi:10.1038/s41586-019-1903-y. ISSN 1476-4687. PMID 31915382.
- ↑ Pardew, Jacob; Blanco Pimentel, Macarena; Low-Decarie, Etienne (April 2018). „Predictable ecological response to rising CO 2 of a community of marine phytoplankton“. Ecology and Evolution (англиски). 8 (8): 4292–4302. doi:10.1002/ece3.3971. PMC 5916311. PMID 29721298.
- ↑ McCulloch, Malcolm T.; D’Olivo, Juan Pablo; Falter, James; Holcomb, Michael; Trotter, Julie A. (2017-05-30). „Coral calcification in a changing World and the interactive dynamics of pH and DIC upregulation“. Nature Communications (англиски). 8 (1): 15686. Bibcode:2017NatCo...815686M. doi:10.1038/ncomms15686. ISSN 2041-1723. PMC 5499203. PMID 28555644.
- ↑ Chan, F., Barth, J.A., Kroeker, K.J., Lubchenco, J. and Menge, B.A. (2019) "The dynamics and impact of ocean acidification and hypoxia". Oceanography, 32(3): 62–71. doi:10.5670/oceanog.2019.312.
 Material was copied from this source, which is available under a Creative Commons Attribution 4.0 International License.
Material was copied from this source, which is available under a Creative Commons Attribution 4.0 International License.
- ↑ Gewin, V. (2010) "Oceanography: Dead in the water". Nature, 466(7308): 812. doi:10.1038/466812a.
- ↑ Kroeker, et al. (June 2013) "Impacts of ocean acidification on marine organisms: quantifying sensitivities and interaction with warming." Glob Chang Biol. 19(6): 1884–1896
- ↑ Harvey, et al. (April 2013) "Meta-analysis reveals complex marine biological responses to the interactive effects of ocean acidification and warming." Ecol Evol. 3(4): 1016–1030
- ↑ Nagelkerken Global alteration of ocean ecosystem functioning due to increasing human CO2 emissions, PNAS vol. 112 no. 43, 2015
- ↑ Bednaršek, N.; Harvey, C.J.; Kaplan, I.C.; Feely, R.A.; Možina, J. (2016). „Pteropods on the edge: Cumulative effects of ocean acidification, warming, and deoxygenation“. Progress in Oceanography. 145: 1–24. Bibcode:2016PrOce.145....1B. doi:10.1016/j.pocean.2016.04.002.
- ↑ Keeling, Ralph F.; Garcia, Hernan E. (2002). „The change in oceanic O2 inventory associated with recent global warming“. Proceedings of the National Academy of Sciences. 99 (12): 7848–7853. Bibcode:2002PNAS...99.7848K. doi:10.1073/pnas.122154899. PMC 122983. PMID 12048249.
- ↑ Harvey wt al Ecol Evol. 2013 Apr; 3(4): 1016–1030
- ↑ Gruber, Nicolas. "Warming up, turning sour, losing breath: ocean biogeochemistry under global change." Philosophical Transactions of the Royal Society of London A: Mathematical, Physical and Engineering Sciences 369.1943 (2011): 1980–1996.
- ↑ Anthony, et al. (May 2011) "Ocean acidification and warming will lower coral reef resilience." Global Change biology, Volume 17, Issue 5, Pages 1798–1808
- ↑ Goldenberg, Silvan U, et al. (2017) "Boosted food web productivity through ocean acidification collapses under warming." Global Change Biology.
- ↑ Pistevos, Jennifer CA, et al. (2015) "Ocean acidification and global warming impair shark hunting behaviour and growth." Scientific reports 5: 16293.
- ↑ Ridgwell, A.; Zondervan, I.; Hargreaves, J. C.; Bijma, J.; Lenton, T. M. (2007). „Assessing the potential long-term increase of oceanic fossil fuel CO2 uptake due to CO2-calcification feedback“. Biogeosciences. 4 (4): 481–492. Bibcode:2007BGeo....4..481R. doi:10.5194/bg-4-481-2007.
- ↑ Tyrrell, T. (2008). „Calcium carbonate cycling in future oceans and its influence on future climates“. Journal of Plankton Research. 30 (2): 141–156. doi:10.1093/plankt/fbm105.
- ↑ „Effects of Ocean Acidification on Marine Species & Ecosystems“. Report. OCEANA. Архивирано од изворникот на 2014-12-25. Посетено на 13 October 2013.
- ↑ 145,0 145,1 Lischka, S.; Büdenbender J.; Boxhammer T.; Riebesell U. (15 April 2011). „Impact of ocean acidification and elevated temperatures on early juveniles of the polar shelled pteropod Limacina helicina : mortality, shell degradation, and shell growth“ (PDF). Report. Biogeosciences. стр. 919–932. Посетено на 14 November 2013.
- ↑ „Comprehensive study of Arctic Ocean acidification“. Study. CICERO. Архивирано од изворникот на 10 December 2013. Посетено на 14 November 2013.
- ↑ „Antarctic marine wildlife is under threat, study finds“. BBC Nature. Посетено на 13 October 2013.
- ↑ V. J. Fabry; C. Langdon; W. M. Balch; A. G. Dickson; R. A. Feely; B. Hales; D. A. Hutchins; J. A. Kleypas; C. L. Sabine. „Present and Future Impacts of Ocean Acidification on Marine Ecosystems and Biogeochemical Cycles“ (PDF). Report of the Ocean Carbon and Biogeochemistry Scoping Workshop on Ocean Acidification Research. Архивирано од изворникот (PDF) на 2010-11-17. Посетено на 2022-02-22.
- ↑ „Canada's State of the Oceans Report, 2012“. Report. Fisheries and Oceans Canada. 2012. Архивирано од изворникот на 6 November 2013. Посетено на 21 October 2013.
- ↑ „Bering Sea Crab Fishery“. Report. Seafood Market Bulletin. November 2005. Архивирано од изворникот на 11 December 2013. Посетено на 10 November 2013.
- ↑ Snyder, John. „Tourism in the Polar Regions: The Sustainability Challenge“ (PDF). Report. UNEP, The International Ecotourism Society. Архивирано од изворникот (PDF) на 2016-06-16. Посетено на 13 October 2013.
- ↑ Harvey, Fiona (2019-12-04). „Tackling degraded oceans could mitigate climate crisis - report“. The Guardian (англиски). ISSN 0261-3077. Посетено на 2019-12-07.
- ↑ Clarke & others (2007).
- ↑ 154,0 154,1 WBGU (2006)
- ↑ UNFCCC (15 March 2011). „Report of the Conference of the Parties on its sixteenth session, held in Cancun from 29 November to 10 December 2010. Addendum. Part two: Action taken by the Conference of the Parties at its sixteenth session“ (PDF). Framework Convention on Climate Change. Geneva, Switzerland: United Nations. p. 3, paragraph 4. Document available in UN languages and text format.
- ↑ UNEP (2010).
- ↑ Good & others (2010).
- ↑ „Carbon Dioxide Emissions and Ocean Acidification; TSCA Section 21 Petition; Reasons for Agency Response“. Environmental Protection Agency (EPA). 2015-10-07.
- ↑ Center for Biological Diversity; Donn J. Viviani. „TSCA Section 21 Petition Requesting EPA to Regulate Anthropogenic Emissions Carbon Dioxide“ (PDF). US EPA.
- ↑ „The President's Climate Action Plan“ (PDF). Посетено на 27 June 2017.
- ↑ Dan Merica (28 March 2017). „Trump dramatically changes US approach to climate change“. CNN Politics. CNN.
- ↑ Shear, Michael D. (1 June 2017). „Trump Will Withdraw U.S. From Paris Climate Agreement“. The New York Times.
- ↑ „US opts out of G7 pledge stating Paris climate accord is 'irreversible'“. The Guardian. 12 June 2017.
- ↑ „How Can Trees Help the Seas?“. The Nature Conservancy (англиски). Посетено на 2021-09-03.
- ↑ 165,0 165,1 165,2 UK Royal Society (2009).
- ↑ US NRC (2011).
- ↑ Trujillo, Alan (2011). Essentials of Oceanography. Pearson Education, Inc. стр. 157. ISBN 9780321668127.
- ↑ Cao, L.; Caldeira, K. (2010). „Can ocean iron fertilization mitigate ocean acidification?“. Climatic Change. 99 (1–2): 303–311. Bibcode:2010ClCh...99..303C. doi:10.1007/s10584-010-9799-4.
- ↑ Ritchie, Roser, Mispy, Ortiz-Ospina. "SDG 14 - Measuring progress towards the Sustainable Development Goals." SDG-Tracker.org, website (2018).
- ↑ United Nations (2017) Resolution adopted by the General Assembly on 6 July 2017, Work of the Statistical Commission pertaining to the 2030 Agenda for Sustainable Development (A/RES/71/313)
- ↑ „Goal 14: Sustainable Development Knowledge Platform“. sustainabledevelopment.un.org. Посетено на 2020-09-05.
- ↑ Zachos, J.C.; Röhl, U.; Schellenberg, S.A.; Sluijs, A.; Hodell, D.A.; Kelly, D.C.; Thomas, E.; Nicolo, M.; Raffi, I. (2005). „Rapid acidification of the ocean during the Paleocene-Eocene thermal maximum“. Science. 308 (5728): 1611–1615. Bibcode:2005Sci...308.1611Z. doi:10.1126/science.1109004. PMID 15947184.
- ↑ Beerling, D. J.; Berner, R. A. (September 2002). „Biogeochemical constraints on the Triassic-Jurassic boundary carbon cycle event: TR-J BOUNDARY C-CYCLE DYNAMICS“. Global Biogeochemical Cycles (англиски). 16 (3): 10–1–10–13. Bibcode:2002GBioC..16.1036B. doi:10.1029/2001GB001637.
- ↑ Bond, David P.G.; Wignall, Paul B. (2014), „Large igneous provinces and mass extinctions: An update“, Volcanism, Impacts, and Mass Extinctions: Causes and Effects (англиски), Geological Society of America: 29–55, doi:10.1130/2014.2505(02), ISBN 978-0-8137-2505-5, Посетено на 2020-05-04
- ↑ Hallam, A. (1997). Mass extinctions and their aftermath. Oxford University Press. ISBN 0-19-854917-2. OCLC 37141126.
- ↑ Hautmann, M. (2004). „Effect of end-Triassic CO2 maximum on carbonate sedimentation and marine mass extinction“. Facies (англиски). 50 (2). doi:10.1007/s10347-004-0020-y. ISSN 0172-9179.
- ↑ 177,0 177,1 Hautmann, Michael; Benton, Michael J.; Tomašových, Adam (2008-07-01). „Catastrophic ocean acidification at the Triassic-Jurassic boundary“. Neues Jahrbuch für Geologie und Paläontologie - Abhandlungen (англиски). 249 (1): 119–127. doi:10.1127/0077-7749/2008/0249-0119.[мртва врска]
- ↑ Greene, Sarah E.; Martindale, Rowan C.; Ritterbush, Kathleen A.; Bottjer, David J.; Corsetti, Frank A.; Berelson, William M. (June 2012). „Recognising ocean acidification in deep time: An evaluation of the evidence for acidification across the Triassic-Jurassic boundary“. Earth-Science Reviews (англиски). 113 (1–2): 72–93. Bibcode:2012ESRv..113...72G. doi:10.1016/j.earscirev.2012.03.009.
- ↑ Blackburn, T. J.; Olsen, P. E.; Bowring, S. A.; McLean, N. M.; Kent, D. V.; Puffer, J.; McHone, G.; Rasbury, E. T.; Et-Touhami, M. (2013-03-21). „Zircon U-Pb Geochronology Links the End-Triassic Extinction with the Central Atlantic Magmatic Province“. Science. 340 (6135): 941–945. Bibcode:2013Sci...340..941B. doi:10.1126/science.1234204. ISSN 0036-8075. PMID 23519213.
- ↑ Lindström, Sofie; van de Schootbrugge, Bas; Hansen, Katrine H.; Pedersen, Gunver K.; Alsen, Peter; Thibault, Nicolas; Dybkjær, Karen; Bjerrum, Christian J.; Nielsen, Lars Henrik (July 2017). „A new correlation of Triassic–Jurassic boundary successions in NW Europe, Nevada and Peru, and the Central Atlantic Magmatic Province: A time-line for the end-Triassic mass extinction“. Palaeogeography, Palaeoclimatology, Palaeoecology (англиски). 478: 80–102. Bibcode:2017PPP...478...80L. doi:10.1016/j.palaeo.2016.12.025.
|hdl-access=бара|hdl=(help) - ↑ Hautmann, M.; Stiller, F.; Huawei, C.; Jingeng, S. (2008-10-01). „Extinction-Recovery Pattern of Level-Bottom Faunas Across the Triassic-Jurassic Boundary in Tibet: Implications for Potential Killing Mechanisms“. PALAIOS (англиски). 23 (10): 711–718. Bibcode:2008Palai..23..711H. doi:10.2110/palo.2008.p08-005r. ISSN 0883-1351.
- ↑ Hautmann, Michael (2012-08-15), „Extinction: End-Triassic Mass Extinction“, eLS (англиски), John Wiley & Sons, стр. a0001655.pub3, doi:10.1002/9780470015902.a0001655.pub3, ISBN 978-0-470-01617-6
- ↑ Riebesell, Ulf; Zondervan, Ingrid; Rost, Björn; Tortell, Philippe D.; Zeebe, Richard E.; Morel, François M. M. (September 2000). „Reduced calcification of marine plankton in response to increased atmospheric CO2“ (PDF). Nature. 407 (6802): 364–367. Bibcode:2000Natur.407..364R. doi:10.1038/35030078. ISSN 0028-0836. PMID 11014189.
- ↑ Fine, M.; Tchernov, D. (2007-03-30). „Scleractinian Coral Species Survive and Recover from Decalcification“. Science (англиски). 315 (5820): 1811. Bibcode:2007Sci...315.1811F. doi:10.1126/science.1137094. ISSN 0036-8075. PMID 17395821.
- ↑ Payne, J. L.; Lehrmann, D. J.; Follett, D.; Seibel, M.; Kump, L. R.; Riccardi, A.; Altiner, D.; Sano, H.; Wei, J. (2007-07-01). „Erosional truncation of uppermost Permian shallow-marine carbonates and implications for Permian-Triassic boundary events“. Geological Society of America Bulletin (англиски). 119 (7–8): 771–784. Bibcode:2007GSAB..119..771P. doi:10.1130/B26091.1. ISSN 0016-7606.
|hdl-access=бара|hdl=(help) - ↑ Clarkson, M. O.; Kasemann, S. A.; Wood, R. A.; Lenton, T. M.; Daines, S. J.; Richoz, S.; Ohnemueller, F.; Meixner, A.; Poulton, S. W. (2015-04-10). „Ocean acidification and the Permo-Triassic mass extinction“ (PDF). Science (англиски). 348 (6231): 229–232. Bibcode:2015Sci...348..229C. doi:10.1126/science.aaa0193. ISSN 0036-8075. PMID 25859043.
- ↑ Henehan, Michael J.; Ridgwell, Andy; Thomas, Ellen; Zhang, Shuang; Alegret, Laia; Schmidt, Daniela N.; Rae, James W. B.; Witts, James D.; Landman, Neil H. (2019-11-05). „Rapid ocean acidification and protracted Earth system recovery followed the end-Cretaceous Chicxulub impact“. Proceedings of the National Academy of Sciences (англиски). 116 (45): 22500–22504. Bibcode:2019PNAS..11622500H. doi:10.1073/pnas.1905989116. ISSN 0027-8424. PMC 6842625. PMID 31636204.

![{\displaystyle {\Omega }={\frac {\left[{\ce {Ca^2+}}\right]\left[{\ce {CO3^2-}}\right]}{K_{sp}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0422ec8bbb280ae8547a20d486b928b0c21846f4)