Од Википедија — слободната енциклопедија
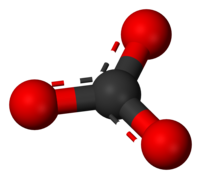 Модел со топчиња и стапчиња на карбонатниот јон, CO2−
Модел со топчиња и стапчиња на карбонатниот јон, CO2−
3
Карбонатот е анјон со електричен полнеж -2 и емпириска формула CO32−.
Едноставните карбонатни соли тежнеат да се нерастворливи во вода, со константи на растворливост помали од 1×10−8. Исклучоци од ова се солите формирани со амониум јонот (NH4+) или јоните на алкалните метали.
Во воден раствор карбонатот постои во три форми. Во силни базни услови, доминира карбонатниот јон од видот CO32−. Во слаби базни услови доминира бикарбонатниот јон HCO3−. Во кисели услови, водниот јаглерод диокисд CO2(aq) е главната форма. Со него постои и минутна количина на јаглеродна киселина H2CO3. Натриум карбонатот е базен, натриум бикарбонатот е слабо базен, додека јаглерод диоксиодот е слаба киселина.
Во биолошките системи, ензимот јаглеродна анхидраза ја катализира интерконверзијата меѓу јаглеродниот диоксид и карбонатните јони.
Карбонатите можат да се формираат и во меѓупланетарниот простор. Исто така, тие се детектирани на кратерот Гусев на Марс.
-
Одредување на карбонати во
почва
|
|---|
|
| H2CO3
|
|
|
|
He
|
Li2CO3,
LiHCO3
|
BeCO3
|
+BO3
|
+C2O4
|
(NH4)2CO3,
NH4HCO3
|
O
|
+F
|
Ne
|
Na2CO3,
NaHCO3,
Na3H(CO3)2
|
MgCO3,
Mg(HCO3)2
|
Al2(CO3)3
|
Si
|
P
|
+SO4
|
+Cl
|
Ar
|
K2CO3,
KHCO3
|
CaCO3,
Ca(HCO3)2
|
|
Sc
|
Ti
|
V
|
CrCO3,
Cr2(CO3)3
|
MnCO3
|
FeCO3
|
CoCO3,
Co2(CO3)3
|
NiCO3
|
Cu2CO3,
CuCO3, Cu2CO3(OH)2
|
ZnCO3
|
Ga
|
Ge
|
As
|
Se
|
Br
|
Kr
|
| Rb2CO3
|
SrCO3
|
|
Y
|
Zr
|
Nb
|
Mo
|
Tc
|
Ru
|
Rh
|
PdCO3
|
Ag2CO3
|
CdCO3
|
In
|
Sn
|
Sb
|
Te
|
I
|
Xe
|
Cs2CO3,
CsHCO3
|
BaCO3
|
*
|
Lu2(CO3)3
|
Hf
|
Ta
|
W
|
Re
|
Os
|
Ir
|
Pt
|
Au
|
HgCO3
|
Tl2CO3
|
PbCO3
|
(BiO)2CO3
|
Po(CO3)2
|
At
|
Rn
|
| Fr
|
RaCO3
|
**
|
Lr
|
Rf
|
Db
|
Sg
|
Bh
|
Hs
|
Mt
|
Ds
|
Rg
|
Cn
|
Nh
|
Fl
|
Mc
|
Lv
|
Ts
|
Og
|
|
|
|
| *
|
La2(CO3)3
|
Ce2(CO3)3
|
Pr2(CO3)3
|
Nd2(CO3)3
|
Pm
|
Sm2(CO3)3
|
EuCO3,
Eu2(CO3)3
|
Gd2(CO3)3
|
Tb2(CO3)3
|
Dy2(CO3)3
|
Ho2(CO3)3
|
Er2(CO3)3
|
Tm2(CO3)3
|
Yb2(CO3)3
|
| **
|
Ac
|
Th(CO3)2
|
Pa
|
UO2CO3
|
Np
|
Pu
|
Am
|
Cm
|
Bk
|
Cf
|
Es
|
Fm
|
Md
|
No
|
|
|
|
|---|
| | Соединенија | |
|---|
| | Јаглеродни јони | |
|---|
| | Наноструктури | |
|---|
| | Оксиди и поврзано | |
|---|
|
|
|---|
| | Обични оксиди | |
|---|
| | Егзотични оксиди | |
|---|
| | Полимери | |
|---|
| | Соединенија изведени од оксиди | |
|---|
|

