Арсен тријодид
| |
Претпочитано име по МСЧПХ: Arsenic triiodide | |
| Систематско име | Тријодоарсен |
Други називи Арсен(III) јодид | |
| Назнаки | |
|---|---|
| 7784-45-4 | |
| ChemSpider | 22979 |
| EC-број | 232-068-4 |
| |
| 3Д-модел (Jmol) | Слика |
| PubChem | 24575 |
| RTECS-бр. | CG1950000 |
| |
| UNII | 3029988O2T |
| Својства | |
| Хемиска формула | |
| Моларна маса | 0 g mol−1 |
| Изглед | портокалово-црвена кристална супстанца |
| Густина | 4.69 g/cm3 |
| Точка на топење | |
| Точка на вриење | |
| 6 g/100 mL | |
| Растворливост | растворливо во алкохол, диетил етер, CS2 целосно се раствора во хлороформ, бензен, толуен |
| -142.0·10−6 cm3/mol | |
| Показател на прекршување (nD) | 2.23 |
| Структура | |
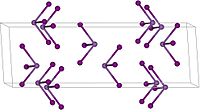
| Кристална структура | Ромбоедар, hR24, SpaceGroup = R-3, No. 148 |
| Опасност | |
| NIOSH (здравствени граници во САД): | |
PEL (дозволива)
|
[1910.1018] TWA 0.010 mg/m3[1] |
REL (препорачана)
|
Ca C 0.002 mg/m3 [15-minute][1] |
IDLH (непосредна опасност)
|
Ca [5 mg/m3 (as As)][1] |
| Дополнителни податоци | |
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |
| Наводи | |
Арсен тријодид е неорганско соединение со формулата AsI3.[2][3][4][5] Тоа е портокалово до темноцрвена цврста супстанца[2][3] што лесно сублимира. Тоа е пирамидална молекула која е корисна за подготовка на органоарсенско соединение.
Подготовка[уреди | уреди извор]
Се подготвува со реакција на арсен трихлорид и калиум јодид:[6]
- AsCl3 + 3KI → AsI3 + 3 KCl
Реакции[уреди | уреди извор]
Хидролизата се случува само бавно во вода која формира арсен триоксид и јодоводородна киселина. Реакцијата се одвива преку формирање на арсенеста киселина која постои во рамнотежа со јодоводородната киселина. Водениот раствор е многу кисел, pH од 0,1N раствор е 1,1. Се распаѓа до арсен триоксид, елементарен арсен и јод кога се загрева во воздух на 200 °C. Разградувањето, сепак, започнува на 100 ° C и се случува со ослободување на јод.
Претходни употреби[уреди | уреди извор]
Растворот по името на Лиам Донели, во минаттот бил користен за лечење на ревматизам, артритис, маларија, трипанозомиски инфекции, туберкулоза и дијабетес.[7]
Наводи[уреди | уреди извор]
- ↑ 1,0 1,1 1,2 „Џебен водич за опасните хемиски материи #0038“. Национален институт за безбедност и здравје при работа (NIOSH). (англиски)
- ↑ 2,0 2,1 „Arsenic triiodide - Hazardous Agents | Haz-Map“. haz-map.com. Посетено на 2023-01-20.
- ↑ 3,0 3,1 „T3DB: Arsenic triiodide“. www.t3db.ca. Посетено на 2023-01-20.
- ↑ „arsenic triiodide“. webbook.nist.gov (англиски). Посетено на 2023-01-20.
- ↑ PubChem. „Arsenic triiodide“. pubchem.ncbi.nlm.nih.gov (англиски). Посетено на 2023-01-20.
- ↑ John C. Bailar, Jr. "Arsenic Triiodide" Inorganic Syntheses 1939, volume 1, pp. 103–104, 2007. doi:10.1002/9780470132326.ch36
- ↑ Shakhashiri BZ, "Chemical of the Week: Arsenic" Архивирано на 2 август 2008 г., University of Wisconsin–Madison Chemistry Dept.
| ||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
