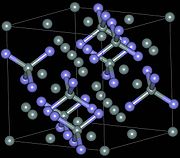
Силициум нитрид
 Силициум нитрид
| |
Претпочитано име по МСЧПХ: Силициум нитрид | |
Други називи нитрид | |
| Назнаки | |
|---|---|
| 12033-89-5 | |
| ChemSpider | 2341213 |
| EC-број | 234-796-8 |
| |
| 3Д-модел (Jmol) | Слика |
| MeSH | Силициум+нитрид |
| PubChem | 3084099 |
| |
| UNII | QHB8T06IDK |
| Својства | |
| Хемиска формула | |
| Моларна маса | 0 g mol−1 |
| Изглед | сив прашок без мирис |
| Густина | 3.17 g/cm3 |
| Точка на топење | |
| Нерастворлив | |
| Показател на прекршување (nD) | 2.016[1] |
| Термохемија | |
| Стандардна моларна ентропија S |
101.3 J·mol−1·K−1 |
| Опасност | |
| Безбедност при работа: | |
Главни опасности
|
[2] |
| Слични супстанци | |
| Други анјони | силициум карбид, силициум диоксид |
| Други катјони | бор нитрид |
| Дополнителни податоци | |
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |
| Наводи | |
Силициум нитрид — хемиско соединение на елементите силициум и азот. Si3N4 е термодинамички најстабилен и комерцијално важен од силициумските нитриди,[3] и терминот „силициум нитрид“ најчесто се однесува на овој специфичен состав. Тоа е бела цврста супстанца со висока точка на топење која е релативно хемиски инертна, нападната од разреден HF и топла H3PO4. Многу е тежок (8,5 на Мохсовата скала). Има висока термичка стабилност со силни оптички нелинеарности за целосно оптички апликации.[4]
Производство[уреди | уреди извор]
Силициум нитрид се подготвува со загревање на силициум во прав помеѓу 1300 г °C и 1400 °C во азотна атмосфера:
- 3 Si + 2 N2 → Si3N4
Тежината на примерокот на силикон постепено се зголемува поради хемиската комбинација на силициум и азот. Без железен катализатор, реакцијата е завршена по неколку часа (~ 7), кога не е откриено дополнително зголемување на тежината поради апсорпција на азот (по грам силициум).
Покрај Si3N4 во литературата се пријавени неколку други фази на силициум нитрид (со хемиски формули кои одговараат на различни степени на нитридација/Si оксидациона состојба). Тие го вклучуваат гасовитиот дисилициум мононитрид ( Si2N), силициум мононитрид (SiN) и силициум секвинитрид ( Si2N3), од кои секоја се стехиометриски фази. Како и кај другите огноотпорни материјали, производите добиени во овие високотемпературни синтези зависат од условите на реакцијата (на пр. време, температура и почетни материјали вклучувајќи ги реактантите и материјалите од контејнери), како и од начинот на прочистување. Сепак, постоењето на сесквинитрид оттогаш е доведено во прашање.[5]
Може да се подготви и по диимиден пат:[6]
- SiCl4 + 6 NH3 → Si(NH)2 + 4 NH4Cl(s) at 0 °C
- 3 Si(NH)2 → Si3N4 + N2 + 3 H2(g) at 1000 °C
Карботермално намалување на силициум диоксид во азотна атмосфера на 1400-1450 Испитувани се и °C:[6]
3 SiO2 + 6 C + 2 N2 → Si3N4 + 6 CO
Нитридацијата на силициумскиот прав била развиена во 1950-тите, по „повторното откривање“ на силициум нитрид и бил првиот метод од големи размери за производство на прав. Сепак, употребата на сиров силикон со ниска чистота предизвика контаминација на силициум нитрид со силикати и железо. Распаѓањето на диимидот резултира со аморфен силициум нитрид, кој треба дополнително да се жари под азот на 1400-1500 °C за да се претвори во кристален прав; ова е сега вториот најважен пат за комерцијално производство. Карботермалното намалување бил најраниот користен метод за производство на силициум нитрид и сега се смета за најисплатлив индустриски пат до прашок од силициум нитрид со висока чистота.[6]
Депонирање[уреди | уреди извор]
Диликон нитрид од електронска класа се формираат со користење на хемиско таложење на пареа (CVD), или една од неговите варијанти, како што е хемиско таложење на пареа засилено со плазма (PECVD):[6][7]
- 3 SiH4(g) + 4 NH3(g) → Si3N4(s) + 12 H2(g) at 750–850°C[8]
- 3 SiCl4(g) + 4 NH3(g) → Si3N4(s) + 12 HCl(g)
- 3 SiCl2H2(g) + 4 NH3(g) → Si3N4(s) + 6 HCl(g) + 6 H2(g)
2 SiH4(g) + N2(g) → 2 SiNH(s) + 3 H2(g)
SiH4(g) + NH3(g) → SiNH(s) + 3 H2(g)
За таложење на слоеви силициум нитрид на полупроводнички (обично силиконски) подлоги, се користат два методи:[7]
- Технологија на хемиско таложење на пареа со низок притисок (LPCVD), која работи на прилично висока температура и се прави или во вертикална или во хоризонтална печка со цевки,[9] или
- Технологија за хемиско таложење на пареа (PECVD) засилена со плазма, која работи при прилично ниски температури и вакуумски услови.
Бидејќи константите на решетката на силициум нитрид и силициум се различни, може да се појави напнатост или стрес, во зависност од процесот на таложење. Особено кога се користи технологијата PECVD, оваа напнатост може да се намали со прилагодување на параметрите на таложење.[10]
Наножиците од силициум нитрид може да се произведуваат и со метод на сол-гел користејќи јаглеродна редукција проследена со нитридација на силика гел, кој содржи ултрафини јаглеродни честички. Честичките може да се произведат со распаѓање на декстроза во температурен опсег 1200-1350 °C. Можните синтезни реакции се:[11]
- SiO2(s) + C(s) → SiO(g) + CO(g) и
- 3 SiO(g) + 2 N2(g) + 3 CO(g) → Si3N4(s) + 3 CO2(g) or
- 3 SiO(g) + 2 N2(g) + 3 C(s) → Si3N4(s) + 3 CO(g).
Обработка[уреди | уреди извор]
Силициум нитрид е тешко да се произведе како рефус материјал - не може да се загрее над 1850 °C, што е многу под неговата точка на топење, поради дисоцијација на силициум и азот. Затоа, примената на конвенционалните техники на синтерување со топла преса е проблематична. Сврзувањето на прашокот од силициум нитрид може да се постигне на пониски температури преку додавање материјали наречени помагала за синтерување или „врзувачи“, кои вообичаено предизвикуваат одреден степен на синтерување во течна фаза. Почиста алтернатива е да се користи синтерување со плазма со искра, каде што загревањето се спроведува многу брзо (секунди) со минување на импулси на електрична струја низ набиениот прав. Со оваа техника се добиени густи компактни силициум нитрид на температури од 1500–1700 °C.
Кристалната структура и својства[уреди | уреди извор]
-
тригонална α-Si3N4.
-
шестоаголна β-Si3N4
-
кубna γ-Si3N4
Постојат три кристалографски структури на силициум нитрид (Si3N4), означени како α, β и γ фази.[12] α и β фазите се најчестите форми на Si3N4, и може да се произведува под нормален притисок. Фазата γ може да се синтетизира само при високи притисоци и температури и има цврстина од 35 GPa.[13][14]
Постојат три кристалографски структури на силициум нитрид (Si3N4), означени како α, β и γ фази.[15] α и β фази се најчестите форми на Si3N4 и може да се произведуваат под нормални услови на притисок. Фазата γ може да се синтетизира само при високи притисоци и температури и има цврстина од 35 GPa.[16][17]

α- и β-Si3N4 имаат тригонална (Пирсонов симбол hP28, просторна група P31c, бр. 159) и хексагонален (hP14, P63, бр. 173) структури, соодветно, кои се изградени со делење на аголот SiN4 тетраедрално. Може да се смета дека се состојат од слоеви на атоми на силициум и азот во низата ABAB... или ABCDABCD... во β-Si3N4 и α-Si3N4, соодветно. Слојот AB е ист во α и β фазите, а CD-слојот во α фазата е поврзан со AB со рамнина со c-лизгање. Si3N4 тетраедрите во β-Si3N4 се меѓусебно поврзани на таков начин што се формираат тунели, кои се движат паралелно со оската c на единица ќелија. Поради рамнината c-лизгање што ги поврзува AB со CD, структурата α содржи шуплини наместо тунели. Кубната γ-Si3N4 често се означува како модификација c во литературата, во аналогија со кубната модификација на бор нитрид (c-BN). Има структура од типот Магнезиум алуминат во која два атоми силикон координираат шест атоми на азот октаедрално, а еден силикон атом координира четири атоми на азот тетраедрално.[18]
Подолгата низа на редење резултира со α-фазата да има поголема цврстина од β-фазата. Сепак, α-фазата е хемиски нестабилна во споредба со β-фазата. При високи температури кога е присутна течна фаза, α-фазата секогаш се трансформира во β-фаза. Затоа, β-Si3N4 е главната форма што се користи во керамиката Si3N4[19].Абнормален раст на зрната може да се појави кај допирани β-Si3N4, при што ненормално големите издолжени зрна се формираат во матрица од пофини изедначени зрна и може да послужат како техника за подобрување на цврстината на фрактура во овој материјал со премостување на пукнатини.[20]. Абнормалниот раст на зрната во допираниот силициум нитрид се јавува поради дифузија засилена со адитиви и резултира со композитни микроструктури, кои исто така може да се сметаат како „in-situ композити“ или „само-засилени материјали.[21]
Покрај кристалните полиморфи на силициум нитрид, стаклени аморфни материјали може да се формираат како производи за пиролиза на прекерамички полимери, кои најчесто содржат различни количества остаток на јаглерод (оттука тие посоодветно се сметаат за силициум карбонитриди). Поточно, поликарбосилазанот може лесно да се конвертира во аморфна форма на материјал базиран на силициум карбонитрид при пиролиза, со вредни импликации во обработката на материјалите од силициум нитрид преку техники на обработка кои почесто се користат за полимери.[22]
Примена[уреди | уреди извор]
Генерално, главниот проблем со примената на силициум нитрид не се техничките перформанси, туку цената. Како што цената се намалува, бројот на апликации за производство се забрзува.[23]
Автомобилската индустрија[уреди | уреди извор]
Една од главните примени на синтеруваниот силициум нитрид е во автомобилската индустрија како материјал за делови од моторот. Тие вклучуваат, кај дизел моторите, приклучоци за осветлување за побрзо палење; комори за предсогорување (комори за вртење) за помали емисии, побрзо стартување и помал шум; турбополнач за намалено доцнење на моторот и емисии. Кај моторите со палење со искра, силициум нитрид се користи за подлоги на ролерите за пониско трошење, турбини со турбополначи за помала инерција и помало заостанување на моторот и во контролните вентили за издувни гасови за зголемено забрзување. Како примери за нивоа на производство, се проценува дека годишно се произведуваат повеќе од 300.000 турбополначи со синтеруван силикон нитрид.[6][23][24]
Лежишта[уреди | уреди извор]

Лежиштата со силициум нитрид се и целосни керамички лежишта и керамички хибридни лежишта со топчиња во керамика и раси во челик. Керамиката со силикон нитрид има добра отпорност на удар во споредба со другите керамики. Затоа, топчести лежишта изработени од силициум нитрид керамика се користат во лежишта за изведба. Репрезентативен пример е употребата на лежишта од силициум нитрид во главните мотори на вселенскиот шатл на НАСА.[25][26]
Бидејќи топчестите лежишта од силикон нитрид се поцврсти од металот, ова го намалува контактот со патеката на лежиштето. Ова резултира со 80% помалку триење, три до десет пати подолг век на траење, 80% поголема брзина, 60% помала тежина, поголема отпорност на корозија и повисока работна температура, во споредба со традиционалните метални лежишта.[23] Топките од силициум нитрид тежат 79% помалку од топчињата од волфрам карбид. Топчести лежишта од силикон нитрид може да се најдат во автомобилски лежишта со висока класа, индустриски лежишта, ветерни турбини, мотоспортови, велосипеди, ролери и скејтборди. Лежиштата со силициум нитрид се особено корисни во апликации каде што корозијата или електричните или магнетните полиња забрануваат употреба на метали, на пример, во мерачи на плимски проток, каде што нападот на морската вода е проблем, или кај барателите на електрично поле.[24]
Si3N4 за прв пат бил демонстриран како супериорно лежиште во 1972 година, но не достигнал производство до скоро 1990 година поради предизвиците поврзани со намалувањето на трошоците. Од 1990 година, цената е значително намалена бидејќи обемот на производството се зголемил. Иако Si3N4 лежишта се уште два до пет пати поскапи од најдобрите челични лежишта, нивните супериорни перформанси и живот го оправдуваат брзото прифаќање. Околу 15-20 милиони во САД во 1996 година биле произведени Si3N4 топчиња за лежишта за машински алати. Растот се проценува на 40% годишно, но би можел да биде уште поголем доколку се изберат керамички лежишта за потрошувачки апликации како што се лизгалки и компјутерски дискови.[23]
Тестирањето на НАСА вели дека керамичко-хибридните лежишта покажуваат многу помал век на трошење од стандардните целосно челични лежишта.[27]
Високотемпературен материјал[уреди | уреди извор]

Силициум нитрид долго време се користи во апликации на високи температури. Особено, тој бил идентификуван како еден од ретките монолитни керамички материјали способни да го преживеат силниот термички удар и топлинските градиенти генерирани во водород/кислород ракетни мотори. За да ја покажат оваа способност во сложена конфигурација, научниците на НАСА користеле напредна технологија за брзо прототипирање за да произведат компонента комора за согорување/млазница (потиснувач) со пречник од еден инч. Потиснувачот бил тестиран на топол оган со водород/кислород погонско гориво и преживеал пет циклуси, вклучително и 5-минутен циклус до 1320 °C температура на материјалот.[28]
Во 2010 година силициум нитрид бил искористен како главен материјал во погонувачите на вселенската сонда на JAXA, Акацуки.[29]
Силициум нитрид бил искористен за „микросклопки“ развиени за Блискиот инфрацрвен спектрограф на вселенскиот телескоп Џејмс Веб. Според НАСА: „Работната температура е криогена, така што уредот треба да може да работи на екстремно ниски температури. Друг предизвик беше развивањето ролетни кои ќе можат: постојано да се отвораат и затвораат без замор; отворете поединечно; и отворен доволно широк за да ги исполни научните барања на инструментот. Силициум нитрид е избран за употреба во микроролетни, поради неговата висока јачина и отпорност на замор. Овој систем на микробленда му овозможува на инструментот да набљудува и анализира до 100 небесни објекти истовремено“.[30]
Медицинска употреба[уреди | уреди извор]
Силициум нитрид има многу ортопедски употреби.[31][32] Материјалот е исто така алтернатива на PEEK (полиетер етер кетон) и титаниум, кои се користат за уреди за спинална фузија (при што вторите се релативно скапи).[33][34] Тоа е хидрофилна, микротекстурирана површина на силициум нитрид која придонесува за јачината, издржливоста и сигурноста на материјалот во споредба со PEEK и титаниумот.[32][33][35] Одредени композиции од овој материјал покажуваат антибактериски,[36] антигабични,[37] или антивирусни својства.[38]
Работа и сечење на метал[уреди | уреди извор]
Првата голема примена на Si3N4 била абразивна и како алат за сечење. Масовниот, монолитен силициум нитрид се користи како материјал за алати за сечење, поради неговата цврстина, термичка стабилност и отпорност на трошење. Посебно се препорачува за обработка на леано железо со голема брзина. Топла цврстина, цврстина на фрактура и отпорност на термички удар значат дека синтеруваниот силициум нитрид може да сече леано железо, тврд челик и легури базирани на никел со површински брзини до 25 пати побрзи од оние добиени со конвенционални материјали како што е волфрам карбид.[24] Употребата на Si3N4 алатки за сечење имале драматичен ефект врз производниот резултат. На пример, мелењето со лице на сиво леано железо со влошки од силициум нитрид ја удвоило брзината на сечењето, го зголемило животниот век на алатот од еден дел на шест делови по раб и ја намалило просечната цена на влошките за 50%, во споредба со традиционалните алатки од волфрам карбид.[6][23]
Електроника[уреди | уреди извор]

Силиконскиот нитрид често се користи како изолатор и хемиска бариера во производството на интегрирани кола, за електрично изолирање на различни структури или како маска за офорт при микромашина на големо. Како пасивационен слој за микрочипови, тој е супериорен во однос на силициум диоксидот, бидејќи е значително подобра дифузна бариера против молекулите на водата и натриумовите јони, два главни извори на корозија и нестабилност во микроелектрониката. Се користи и како диелектрик помеѓу полисилициумските слоеви во кондензаторите во аналогните чипови.[39]

Силициум нитрид депониран од LPCVD содржи до 8% водород. Сепак, тој има поголема отпорност и диелектрична сила од повеќето изолатори вообичаено достапни во микрофабрикацијата (10 16 Ω · cm и 10 MV/cm, соодветно).[7]
Не само силициум нитрид, туку и разни тројни соединенија на силициум, азот и водород (SiN x H y ) се користат како изолациски слоеви. Тие се депонираат во плазмата со помош на следните реакции:[7]
Овие SiNH имаат многу помал стрес на истегнување, но полоши електрични својства (отпорност 10 6 до 10 15 Ω·cm и диелектрична јачина од 1 до 5 MV/cm),[7][40] и се термички стабилни на високи температури под специфични физички услови. Силициум нитрид се користи и во ксерографскиот процес како еден од слоевите на фототапанот.[41] Силициум нитрид исто така се користи како извор на палење за домашни апарати за гас.[42] Поради неговите добри еластични својства, силициум нитрид, заедно со силициум и силициум оксид, е најпопуларниот материјал за конзоли - сензорните елементи на микроскопите со атомска сила.[43]
Соларни ќелии[уреди | уреди извор]
Соларните ќелии често се обложени со антирефлектирачка обвивка. За ова може да се користи силициум нитрид и можно е да се прилагоди неговиот индекс на рефракција со менување на параметрите на процесот на таложење.[44][45]
Фотонски интегрирани кола[уреди | уреди извор]
Фотонските интегрирани кола може да се произведуваат со различни материјали, наречени и материјални платформи. Силициум нитрид е една од тие материјални платформи, веднаш до, на пример, силикон фотоника и индиум фосфид. Фотонските интегрирани кола со силикон нитрид имаат широка спектрална покриеност и се одликуваат со слаби загуби на светлина. Ова ги прави многу прилагодени за детектори, спектрометри, биосензори и квантни компјутери. Најмали загуби на ширење пријавени во SiN (0,1 dB/cm до 0,1 dB/m) се постигнати со брановодите TriPleX на LioniX International.[46]
Историја[уреди | уреди извор]
Првата подготовка била пријавена во 1857 година од Анри Етјен Сент-Клер Девил и Фридрих Волер.[47] Во нивниот метод, силиконот се загревал во сад, сместен во друг сад полн со јаглерод за да се намали продорот на кислородот во внатрешната садница. Тие пријавиле производ што го нарекле силициум нитрид, но без да го наведат неговиот хемиски состав. Пол Шуценбергер прв пријавил производ со составот на тетранитрид, Si3N4 во 1879 година, кој бил добиен со загревање на силициум со брусна (паста направена со мешање на јаглен, јаглен или кокс со глина која потоа се користи за обложување на садници) во висока печка. Во 1910 година, Лудвиг Вајс и Теодор Енгелхард загреале силициум под чист азот за да произведат Si3N4.[48] Е. Фридерих и Л. Ситинг направиле Si3N4 во 1925 година преку карботермална редукција под азот, односно со загревање силициум диоксид, јаглерод и азот на 1250–1300 °C.
Силиконскиот нитрид останал само хемиска љубопитност со децении пред да се користи во комерцијални апликации. Од 1948 до 1952 година, компанијата Carborundum, Њујорк, аплицирала за неколку патенти за производство и примена на силициум нитрид.[6] До 1958 година, силициум нитридот ма Хејнс Интернационал бил во комерцијално производство за цевки за термоспој, ракетни млазници и чамци и садници за топење метали. Британската работа на силициум нитрид, започната во 1953 година, била насочена кон високотемпературни делови од гасни турбини и резултирала со развој на силициум нитрид поврзан со реакција и силициум нитрид со топло пресување. Во 1971 година, Агенцијата за напреден истражувачки проект на Министерството за одбрана на САД направила договор во вредност од 17 милиони американски долари со Форд и Вестингхаус за две керамички гасни турбини.[49]
Иако својствата на силициум нитрид биле добро познати, неговата природна појава била откриена дури во 1990-тите, како ситни подмножества (околу 2 μm × 0,5 μm во големина) во метеорити. Минералот го добил името ниерит по пионерот на масената спектрометрија, Алфред О.Ц. Нир .[50] Овој минерал можеби бил откриен порано, повторно исклучиво во метеорити, од советски геолози.[51]
Наводи[уреди | уреди извор]
- ↑ Refractive index database. refractiveindex.info
- ↑ ITEM # SI-501, SILICON NITRIDE POWDER MSDS Архивирано на 6 јуни 2014 г.. metal-powders-compounds.micronmetals.com
- ↑ Mellor, Joseph William (1947). A Comprehensive Treatise on Inorganic and Theoretical Chemistry. 8. Longmans, Green and Co. стр. 115–7. OCLC 493750289.
- ↑ López-Suárez, A.; Torres-Torres, C.; Rangel-Rojo, R.; Reyes-Esqueda, J. A.; Santana, G.; Alonso, J. C.; Ortiz, A.; Oliver, A. (2009-06-08). „Modification of the nonlinear optical absorption and optical Kerr response exhibited by nc-Si embedded in a silicon-nitride film“. Optics Express (англиски). 17 (12): 10056–10068. Bibcode:2009OExpr..1710056L. doi:10.1364/OE.17.010056. ISSN 1094-4087. PMID 19506657.
- ↑ Carlson, O. N. (1990). „The N-Si (Nitrogen-Silicon) system“. Bulletin of Alloy Phase Diagrams. 11 (6): 569–573. doi:10.1007/BF02841719.
- ↑ 6,0 6,1 6,2 6,3 6,4 6,5 6,6 Riley, Frank L. (2004). „Silicon Nitride and Related Materials“. Journal of the American Ceramic Society. 83 (2): 245–265. doi:10.1111/j.1151-2916.2000.tb01182.x.
- ↑ 7,0 7,1 7,2 7,3 7,4 Nishi, Yoshio; Doering, Robert (2000). Handbook of semiconductor manufacturing technology. CRC Press. стр. 324–325. ISBN 978-0-8247-8783-7.
- ↑ Morgan, D. V.; Board, K. (1991). An Introduction To Semiconductor Microtechnology (2. изд.). Chichester, West Sussex, England: John Wiley & Sons. стр. 27. ISBN 978-0471924784.
- ↑ „Crystec Technology Trading GmbH, Comparison of vertical and horizontal tube furnaces in the semiconductor industry“. crystec.com. Посетено на 2009-06-06.
- ↑ „Crystec Technology Trading GmbH, deposition of silicon nitride layers“. Посетено на 2009-06-06.
- ↑ Ghosh Chaudhuri, Mahua; Dey, Rajib; Mitra, Manoj K.; Das, Gopes C.; Mukherjee, Siddhartha (2008). „A novel method for synthesis of α-Si3N4 nanowires by sol-gel route“. Science and Technology of Advanced Materials. 9 (1): 5002. Bibcode:2008STAdM...9a5002G. doi:10.1088/1468-6996/9/1/015002. PMC 5099808. PMID 27877939.
- ↑ „Crystal structures of Si3N4“. hardmaterials.de. Посетено на 2009-06-06.
- ↑ Jiang, J. Z.; Kragh, F.; Frost, D. J.; Ståhl, K.; Lindelov, H. (2001). „Hardness and thermal stability of cubic silicon nitride“. Journal of Physics: Condensed Matter. 13 (22): L515. Bibcode:2001JPCM...13L.515J. doi:10.1088/0953-8984/13/22/111.
- ↑ „Properties of gamma-Si3N4“. Архивирано од изворникот на July 15, 2006. Посетено на 2009-06-06.
- ↑ „Crystal structures of Si3N4“. hardmaterials.de. Посетено на 2009-06-06.
- ↑ Jiang, J. Z.; Kragh, F.; Frost, D. J.; Ståhl, K.; Lindelov, H. (2001). „Hardness and thermal stability of cubic silicon nitride“. Journal of Physics: Condensed Matter. 13 (22): L515. Bibcode:2001JPCM...13L.515J. doi:10.1088/0953-8984/13/22/111. S2CID 250763667 Проверете ја вредноста
|s2cid=(help). - ↑ „Properties of gamma-Si3N4“. Архивирано од изворникот на July 15, 2006. Посетено на 2009-06-06.
- ↑ Peng, pp. 1-3
- ↑ Zhu, Xinwen; Sakka, Yoshio (2008). „Textured silicon nitride: Processing and anisotropic properties“. Science and Technology of Advanced Materials. 9 (3): 3001. Bibcode:2008STAdM...9c3001Z. doi:10.1088/1468-6996/9/3/033001. PMC 5099652. PMID 27877995.
- ↑ Abnormal grain growth Journal of Crystal growth
- ↑ Effect of Grain Growth of B-Silicon Nitride on Strength, Weibull Modulus, and Fracture Toughness Архивирано на 11 декември 2021 г. Journal of the American Ceramic Society
- ↑ Wang, Xifan; Schmidt, Franziska; Hanaor, Dorian; Kamm, Paul H.; Li, Shuang; Gurlo, Aleksander (2019). „Additive manufacturing of ceramics from preceramic polymers: A versatile stereolithographic approach assisted by thiol-ene click chemistry“. Additive Manufacturing. 27: 80–90. arXiv:1905.02060. Bibcode:2019arXiv190502060W. doi:10.1016/j.addma.2019.02.012. S2CID 104470679.
- ↑ 23,0 23,1 23,2 23,3 23,4 Richerson, David W.; Freita, Douglas W. „Ceramic Industry“. Opportunities for Advanced Ceramics to Meet the Needs of the Industries of the Future. Oak Ridge National Laboratory. hdl:2027/coo.31924090750534. OCLC 692247038.
- ↑ 24,0 24,1 24,2 „Silicon Nitride – An Overview“. azom.com. 2001-02-06. Посетено на 2009-06-06.
- ↑ „Ceramic Balls Increase Shuttle Engine Bearing Life“. NASA. Архивирано од изворникот на 2004-10-24. Посетено на 2009-06-06.
- ↑ „Space Shuttle Main Engine Enhancements“. NASA. Архивирано од изворникот на 2012-10-11. Посетено на 2009-06-06.
- ↑ Zaretsky, Erwin V.; Vlcek, Brian L.; Hendricks, Robert C. (1 April 2005). „Effect of Silicon Nitride Balls and Rollers on Rolling Bearing Life“ (англиски). Наводот journal бара
|journal=(help) - ↑ Eckel, Andrew J. (1999). „Silicon Nitride Rocket Thrusters Test Fired Successfully“. NASA. Архивирано од изворникот на April 4, 2009.
- ↑ Orbit Control Maneuver Result of the Venus Climate Orbiter 'AKATSUKI'.
- ↑ James Webb Space Telescope / Goddard Space Flight Center > Innovations > Microshutters / Nasa (2020-06-25).
- ↑ Olofsson, Johanna; Grehk, T. Mikael; Berlind, Torun; Persson, Cecilia; Jacobson, Staffan; Engqvist, Håkan (2012). „Evaluation of silicon nitride as a wear resistant and resorbable alternative for total hip joint replacement“. Biomatter. 2 (2): 94–102. doi:10.4161/biom.20710. PMC 3549862. PMID 23507807.
- ↑ 32,0 32,1 Mazzocchi, M; Bellosi, A (2008). „On the possibility of silicon nitride as a ceramic for structural orthopaedic implants. Part I: Processing, microstructure, mechanical properties, cytotoxicity“. Journal of Materials Science: Materials in Medicine. 19 (8): 2881–7. doi:10.1007/s10856-008-3417-2. PMID 18347952.
- ↑ 33,0 33,1 Webster, T.J.; Patel, A.A.; Rahaman, M.N.; Sonny Bal, B. (2012). „Anti-infective and osteointegration properties of silicon nitride, poly(ether ether ketone), and titanium implants“. Acta Biomaterialia. 8 (12): 4447–54. doi:10.1016/j.actbio.2012.07.038. PMID 22863905.
- ↑ Anderson, MC; Olsen, R (2010). „Bone ingrowth into porous silicon nitride“. Journal of Biomedical Materials Research Part A. 92 (4): 1598–605. doi:10.1002/jbm.a.32498. PMID 19437439.
- ↑ Arafat, Ahmed; Schroën, Karin; De Smet, Louis C. P. M.; Sudhölter, Ernst J. R.; Zuilhof, Han (2004). „Tailor-Made Functionalization of Silicon Nitride Surfaces“. Journal of the American Chemical Society. 126 (28): 8600–1. doi:10.1021/ja0483746. PMID 15250682.
- ↑ Pezzotti, Giuseppe; Marin, Elia; Adachi, Tetsuya; Lerussi, Federica; Rondinella, Alfredo; Boschetto, Francesco; Zhu, Wenliang; Kitajima, Takashi; Inada, Kosuke (2018-04-24). „Incorporating Si3 N4 into PEEK to Produce Antibacterial, Osteocondutive, and Radiolucent Spinal Implants“. Macromolecular Bioscience. 18 (6): 1800033. doi:10.1002/mabi.201800033. ISSN 1616-5187. PMID 29687593.
- ↑ McEntire, B., Bock, R., & Bal, B.S. U.S Application.
- ↑ Pezzotti, Giuseppe; Ohgitani, Eriko; Shin-Ya, Masaharu; Adachi, Tetsuya; Marin, Elia; Boschetto, Francesco; Zhu, Wenliang; Mazda, Osam (2020-06-20). „Rapid Inactivation of SARS-CoV-2 by Silicon Nitride, Copper, and Aluminum Nitride“. doi:10.1101/2020.06.19.159970. Посетено на 2020-09-21. Наводот journal бара
|journal=(help) - ↑ Pierson, Hugh O. (1992). Handbook of chemical vapor deposition (CVD). William Andrew. стр. 282. ISBN 978-0-8155-1300-1.
- ↑ Sze, S.M. (2008). Semiconductor devices: physics and technology. Wiley-India. стр. 384. ISBN 978-81-265-1681-0.
- ↑ Schein, L.B. (1988). Electrophotography and Development Physics, Springer Series in Electrophysics. 14. Springer-Verlag, Berlin. ISBN 978-3-642-97085-6.
- ↑ Levinson, L. M. et al. (17 April 2001) "Ignition system for a gas appliance" U.S. Patent 6.217.312
- ↑ Ohring, M. (2002). The materials science of thin films: deposition and structure. Academic Press. стр. 605. ISBN 978-0-12-524975-1.
- ↑ Rajinder Sharma (Jul 2, 2019). „Effect of obliquity of incident light on the performance of silicon solar cells“. Heliyon. 5 (7): e01965. doi:10.1016/j.heliyon.2019.e01965. PMC 6611928. PMID 31317080.
- ↑ Rajinder Sharma (May 2018). „Silicon nitride as antireflection coating to enhance the conversion efficiency of silicon solar cells“. Turkish Journal of Physics. 42 (4): 350–355. doi:10.3906/fiz-1801-28.
- ↑ Roeloffzen, Chris G. H.; Hoekman, Marcel; Klein, Edwin J.; Wevers, Lennart S.; Timens, Roelof Bernardus; Marchenko, Denys; Geskus, Dimitri; Dekker, Ronald; Alippi, Andrea (July 2018). „Low-Loss Si3N4 TriPleX Optical Waveguides: Technology and Applications Overview“. IEEE Journal of Selected Topics in Quantum Electronics. 24 (4): 1–21. Bibcode:2018IJSTQ..2493945R. doi:10.1109/JSTQE.2018.2793945. ISSN 1077-260X.
- ↑ „Ueber das Stickstoffsilicium“. Annalen der Chemie und Pharmacie. 104 (2): 256. 1857. doi:10.1002/jlac.18571040224.
- ↑ Weiss, L.; Engelhardt, T (1910). „Über die Stickstoffverbindungen des Siliciums“. Z. Anorg. Allg. Chem. 65 (1): 38–104. doi:10.1002/zaac.19090650107.
- ↑ Carter, C. Barry; Norton, M. Grant (2007). Ceramic Materials: Science and Engineering. Springer. стр. 27. ISBN 978-0-387-46270-7.
- ↑ Lee, M. R.; Russell, S. S.; Arden, J. W.; Pillinger, C. T. (1995). „Nierite (Si3N4), a new mineral from ordinary and enstatite chondrites“. Meteoritics. 30 (4): 387. Bibcode:1995Metic..30..387L. doi:10.1111/j.1945-5100.1995.tb01142.x.
- ↑ „Nierite“. Mindat. Посетено на 2009-08-08.
Цитирани извори[уреди | уреди извор]
- Peng, Hong (2004). Spark Plasma Sintering of Si3N4-based Ceramics: Sintering mechanism-Tailoring microstructure-Evaluating properties (PhD thesis). Stockholm University. ISBN 978-91-7265-834-9.
| ||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||