Диетил малонат

| |

| |
Претпочитано име по МСЧПХ: Диетил пропандиоат | |
Други називи Диетил малонат | |
| Назнаки | |
|---|---|
| 105-53-3 | |
| Кратенки | DEM |
| Бајлштајн | 774687 |
| ChEBI | CHEBI:391281 |
| ChEMBL | ChEMBL177114 |
| ChemSpider | 13863636 |
| EC-број | 203-305-9 |
| |
| 3Д-модел (Jmol) | Слика |
| MeSH | Diethyl+malonate |
| PubChem | 7761 |
| RTECS-бр. | OO0700000 |
| |
| UNII | 53A58PA183 |
| Својства | |
| Хемиска формула | |
| Моларна маса | 0 g mol−1 |
| Изглед | безбојна течност |
| Густина | 1.05 g/cm3, течно |
| Точка на топење | |
| Точка на вриење | |
| занемарлив | |
| Киселост (pKa) | 14 16.37 (DMSO)[2] |
| -92.6·10−6 cm3/mol | |
| Структура | |
| Диполен момент | 2.54 D (течно)[3] |
| Термохемија | |
| Специфичен топлински капацитет, C | 285.0 J·mol−1·K−1[3] |
| Опасност | |
| Безбедност при работа: | |
Главни опасности
|
Штетен (X), запалив (F) |
| Температура на запалување | {{{value}}} |
| Безбедносен лист | Oxford University MSDS |
| Дополнителни податоци | |
| Освен ако не е поинаку укажано, податоците се однесуваат на материјалите во нивната стандардна состојба (25 °C, 100 kPa) | |
| Наводи | |
Диетил малонат, познат и како DEM, е диетилен естер на маланската киселина . Природно се наоѓа во грозјето и јагодите како безбојна течност со мирис на јаболко и се користи во парфемите . Се користи и за синтеза на други соединенија како што се барбитурати, вештачки ароми, витамин Б1 и витамин Б6 .
Структура и својства[уреди | уреди извор]
Малонската киселина е прилично едноставна дикарбоксилна киселина, со две карбоксилни групи блиску една до друга. При формирањето на диетил малонат од маланска киселина, хидроксилната група (-OH) на двете карбоксилни групи се заменува со етокси група (-OEt; -OCH2CH3 ). Метиленската група (−CH 2 −) во средината на малонскиот дел од молекулата на диетил малонат е соседна со две карбонилни групи (−C(=O)−).[4]
Атомите на водород на јаглеродот во непосредна близина на карбонилната група во молекулата се значително покисели од атомите на водород на јаглерод во непосредна близина на алкилните групи (до 30 реда големина). (Ова е познато како α позиција во однос на карбонилот. ) Атомите на водород на јаглерод во непосредна близина на две карбонилни групи се уште покисели бидејќи карбонилните групи помагаат да се стабилизира карбанионот што произлегува од отстранувањето на протонот од метиленската група меѓу нив. Степенот на резонантна стабилизација на конјугираната база на ова соединение е предложен од трите резонантни форми подолу:
Подготовка[уреди | уреди извор]
Диетил малонат се добива од реакцијата на натриумовата сол на хлорооцетна киселина со натриум цијанид, кој го произведува нитрилот. Овој посредник потоа се третира со етанол во присуство на киселински катализатор:
- ClCH
2CO
2Na + NaCN → NCCH
2CO
2Na + NaCl - NCCH
2CO
2Na + 2 C
2H
5OH + 2 HCl → C
2H
5O
2CCH
2CO
2C
2H
5 + NH
4Cl + NaCl
Алтернативно, натриум хлороацетат се подложува на карбоксистерификација со третман со јаглерод моноксид и етанол:
- ClCH
2CO
2Na + CO + 2 C
2H
5OH → C
2H
5O
2CCH
2CO
2C
2H
5 + NaCl
Како катализатор со него се користи дикобалт октакарбонил .[5]
Реакции[уреди | уреди извор]
Синтеза на малонски естер[уреди | уреди извор]
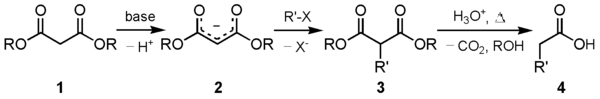
Една од главните употреби на ова соединение е синтезата на малонски естер . Карбанионот ( 2 ) формиран со реакција на диетил малонат ( 1 ) со соодветна база може да се алкилира со соодветен електрофил. Ова алкилизирано 1,3-дикарбонил соединение ( 3 ) лесно се подложува на декарбоксилација со губење на јаглерод диоксид, за да се добие супституирана оцетна киселина ( 4 ):
Општо земено, како основа се претпочитаат соли на алкоксидниот анјон чиј алкилен дел одговара на оној што се користи во горенаведената алкилација. Употребата на конвенционална база може да даде производи за хидролиза на базата - на пример, натриум хидроксид едноставно ќе произведе натриум малонат и алкохол, додека другите соли на алкоксид ќе предизвикаат мешање со трансестерификација . Само „истиот“ алкоксиден анјон како оној што се користел за алкилирање на депротонираната активна метиленска локација ќе спречи и базна хидролиза и трансестерификација.
Други реакции[уреди | уреди извор]
Како и многу други естри, ова соединение е подложно на кондензации на естер на Клајзен . Предноста на користењето на ова соединение е што се избегнуваат несакани реакции на самокондензација. Како и другите естри, ова соединение се подложува на бромирање на алфа позиција.
Диетил малонат може да се нитрозира со вишок натриум нитрит во оцетна киселина за да се добие диетил оксиминомалонат, чија каталитичка хидрогенолиза во етанол над Pd/C дава диетил аминомалонат (DEAM). DEAM може да се ацетилира за да произведе диетил ацетамидомалонат (корисен во синтезата на амино-киселини), или може да се додаде со 3-супституирани 2,4-дикетони во зовриена оцетна киселина за да се добие максимален принос различно супституирани етил пирол-2-карбоксилати од интерес за синтеза на порфирин.[6]
Апликации[уреди | уреди извор]

Диетил малонат може да се користи во подготовката на неколку медицински корисни соединенија вклучувајќи вигабатрин, фенилбутазон, налидиксична киселина и ребамипид . Неколку пестициди се произведуваат и од диетилмалонат, вклучувајќи ги сетоксидим и дериватите на 2-амино-4-хлоро-6-метокси пиримидин .[5]
Наводи[уреди | уреди извор]
- ↑ 'malonic acid' is recognised as a valid, expert-verified name for what would systematically be called 'propanedioic acid' according to ChemSpider.
- ↑ Olmstead, William N.; Bordwell, Frederick G. (1980). „Ion-pair association constants in dimethyl sulfoxide“. The Journal of Organic Chemistry. 45 (16): 3299–3305. doi:10.1021/jo01304a033.
- ↑ 3,0 3,1 CRC handbook of chemistry and physics : a ready-reference book of chemical and physical data. William M. Haynes, David R. Lide, Thomas J. Bruno (2016-2017, 97th. изд.). Boca Raton, Florida. 2016. ISBN 978-1-4987-5428-6. OCLC 930681942.CS1-одржување: друго (link)
- ↑ „IR spectrum of Malonic acid“. Архивирано од изворникот на 2010-06-26. Посетено на 2010-02-14.
- ↑ 5,0 5,1 Strittmatter, Harald; Hildbrand, Stefan; Pollak, Peter (2007). „Malonic Acid and Derivatives“. Ullmann's Encyclopedia of Industrial Chemistry. doi:10.1002/14356007.a16_063.pub2. ISBN 978-3527306732.
- ↑ Paine, John B.; Dolphin, David (1985-12-01). „Pyrrole chemistry. An improved synthesis of ethyl pyrrole-2-carboxylate esters from diethyl aminomalonate“. The Journal of Organic Chemistry. 50 (26): 5598–5604. doi:10.1021/jo00350a033. ISSN 0022-3263.