Етер
- За други значења видете во Етер (појаснување).

Етри — органски соединенија кои содржат две функционални групи кои можат да бидат алкил или арил групи поврзани со кислороден атом. Кај симетричните етри групите се еднакви, а кај несиметричните тие се различни.
Како и алкохолите, и етрите може да се сметаат за органски аналози ("роднини") на водата.
Претставници и примена[уреди | уреди извор]
| Скелетна формула | 3D приказ |
|---|---|

| |

|

|

|
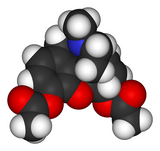
|
Диетил етер, обично наречен етил етер или само етер, нашироко се употребува како растворувач и како општ анестетик што се внесува во облик на пареи. Тој делува како депресант на централниот нервен систем и предизвикува несвестица. Диетил етер се употребува заедно со кислород, а смесата е потенцијално експлозивна. Статичкиот електрицитет може лесно да предизвика експлозија.
Познати се и многу циклични етри. Тетрахидроканабинол (ТНС), активна супстанца во марихуаната, има шестчлен етерски прстен. Други циклични етри вклучуваат дроги како кодеин, морфин и хероин.
Одредени циклични етри што содржат неколку кислородни атоми можат да ги транспортираат јоните во биолошките мембрани. Еден од нив е нонактинот, антибиотик што селективно го транспортира калиумот надвор од бактериските клетки. Ова соединение што содржи петчлени етерски прстени поврзани со естерски единици се поврзува со калиумот десет пати подобро отколку со натриумот. Бидејќи клетките мораат да одржуваат повисока концентрација на калиум од натриум јони, селективното отстранување на калиумот ги убива бактериите. Моненсинот, посложен полиетер, образува комплекси со натриум јони, а комплексот ги транспортира натриум јоните во клетките. Зголемувањето на концентрацијата на натриум јоните во клетките го зголемува осмотскиот притисок, а клеточната мембрана се раскинува, убивајќи ја клетката. Моненсинот се додава во храната на живината за уништување на цревните паразити.
Именување[уреди | уреди извор]
Едноставните етри се именуваат како алкил-алкил етри. Името се прави со наведување на алкил (или арил) групите по азбучен редослед и со додавање на името етер. На пример, несиметричниот етер што има една бутил група и една метил група поврзани со еден кислороден атом се вика бутил метил етер. Симетричните етри го добиваат своето име со додавање на претставката ди- на името за алкил групата. На пример, еден етер со две изопропил групи поврзани со еден кислороден атом се вика диизопропил етер.
Физички својства[уреди | уреди извор]
Етерските молекули не можат да образуваат водородни врски меѓу себе, што резултира во релативно ниската температура на вриење споредено со таа на аналогните алкани. Етрите се повеќе хидрофобни отколку естерите или амидите со споредлива структура.
Етрите се однесуваат како Луисови бази. На пример, диетил етер образува комплекс со соединенијата составени од бор, како бор трифлуорид диетил етерат .F3B:O(CH2CH3)2. Етрите исто така се координираат со магнезиумот во Грињаровите реагенси.
Слични структури[уреди | уреди извор]

Етрите не треба да се мешаат со следните класи соединенија со истата општа структура R-O-R:
- Ароматични соединенија како фуранот, каде кислородот е дел од ароматичниот прстен.
- Соединенија каде еден од јаглеродните атоми до кислородот е поврзан за кислороден атом, азот или сулфур:
Примарни, вторични и третични етри[уреди | уреди извор]
Термините "примарен етер", "вторичен етер" и "третичен етер" се користат повремено и се однесуваат на јаглеродниот атом до етерскиот кислороден атом. Во еден примарен етер, овој јаглероден атом е поврзан со само еден друг јаглероден атом, како што е во диетил етер: CH3-CH2-O-CH2-CH3. Пример за вторичен етер е диизопропил етер (CH3)2CH-O-CH(CH3)2, додека за третичен етер е ди-терт-бутил етер (CH3)3C-O-C(CH3)3.
Диметил етер, примарен, вторичен и третичен етер.
Полиетри[уреди | уреди извор]
Полиетрите се соединенија со повеќе од една етерска група. Додека терминот општо се однесува на полимери, како полиетилен гликол и полипропилен гликол, нискомолекуларните соединенија од типот на крунски етри понекогаш можат да се вклучат во оваа група.
Синтеза[уреди | уреди извор]
Етрите можат да се подготват во лабораторија на неколку начини:
- R-OH + R-OH → R-O-R + H2O
- За оваа директна реакција се потребни драстични услови (температура и кисел катализатор) и обично не е применлива. Такви услови можат да ги уништат деликатните структури на некои функционални групи. Постојат неколку поблаги методи за подготовка на етри.
- R-O- + R-X → R-O-R + X-
- Оваа реакција се вика Вилијамсонова етерска синтеза. Вклучува дејство на матичен алкохол со силна база, при што се образува алкоксиден анјон, следено со адиција на соодветно алифатично соединение кое носи соодветна заминувачка група (R-X). Соодветни заминувачки групи (X) се јодид, бромид или сулфонати. Овој метод не е можен доколку R е ароматичен, како во бромобензенот. Исто така, овој метод ги дава само најдобрите приноси за примарни јаглеродни атоми, бидејќи вторичните ќе подлежат на Е2 елиминација на сметка на базниот алкоксиден анјон кој се користи во реакцијата. Арил етрите можат да се подготват со Улманова кондензација:
- Електрофилна адиција на алкохоли на алкени.
- R2C=CR2 + R-OH → R2CH-C(-O-R)-R2
- Кисела катализа е потребна за оваа реакција. Тетрахидропиранилните етри се користат како заштитни групи за алкохоли.
Цикличните етри, кои се познати и како епоксиди, можат да се подготват:
- Со оксидација на алкени со пероксикиселина, каква што е m-CPBA.
- Со базна меѓумолекулска нуклеофилна супституција на халохидрин.
Хемиски реакции[уреди | уреди извор]

Општо, етрите се многу нереактивни. Најчести реакции се:
- Етрите се хидролизираат само под драстични услови, како загревање со бор трибромид или загревање во бромоводородна киселина. Пониските минерални киселини кои содржат халоген елемент, како што е хлороводородната киселина ги расцепуваат етрите, но многу споро. Овие две киселини се единствените кои го прават тоа во доволен размер. Одредени арил етри можат да се расцепат со алуминиум хлорид.
- Епоксидите, или цикличните етри со тричлени прстени се високо осетливи на нуклеофилен напад и се реактивни во таа смисла.
- Пероксидна формација.
- Примарните и вторичните етри со CH група до етерскиот кислород полесно образуваат високо експлозивни органски пероксиди (како на пример, диетил етер пероксид) во присуство на кислород, светлина и метални и алдехидни нечистотии. Поради ова, етрите како диетил етер и THF обично се избегнуваат како растворувачи во индустриските процеси.
Етерот како тема во популарната култура[уреди | уреди извор]
- „Етер“ (Ether) - песна на британската рок-група „Генг оф фор“ (Gang Of Four) од 1979 година.[1]
Наводи[уреди | уреди извор]
|
