Атом
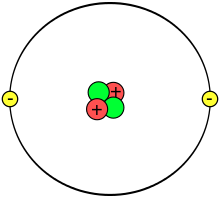
Во физиката и хемијата, атомот (на грчки άτομον — неделив) — најмалата структурна честица на секој хемиски елемент (со тоа и на материјата) што ги има неговите карактеристични својства. Секој атом се состои од атомско јадро и електронска обвивка. Притоа, и во јадрото, а и во електронската обвивка се наоѓаат неколку типови на елементарни честички: во јадрото се наоѓаат неутралните неутрони и позитивно наелектризираните протони (или позитрони), додека во електронската обвивка се наоѓаат негативно наелектризираните електрони (односно негатрони). Сите овие елементарни честички играат голема улога при идентификувањето на атомите, како и при нивното поврзување со други атоми од ист или различен хемиски елемент (род).
Историјатa на атомот[уреди | уреди извор]
Уште од времето на старогрчките филозофи луѓето размислувале од што и како е изградена материјата. Постоеле две групи на филозофи, од кои едните сметале дека материјата може бесконечно да се дели на помали делчиња, а другите сметале дека постојат најмали делчиња од супстанцијата кои понатаму не можат да се делат. Позначајни филозофи кои се занимавале со оваа тематика се Аристотел, Левкип и Демокрит.
Меѓутоа, многу години подоцна, во август 1945 година, по појавата на кобната печурка над Хирошима и Нагасаки, кај човештвото длабоко се втисна поимот "атом". Во ова време се мислело дека атомите се создадени при создавањето на универзумот и дека тие не можат ниту да се уништат, ниту да се трансформираат од еден во друг вид. Ваквото сфаќање е разнишано кон крајот на XIX и почетокот на XX век.
Во годините меѓу 1895-1900 беа откриени пет необични зрачења со голема продорност и енергија. X и γ зрачењата се однесуваат како светлински (електромагнетни) бранови со многу куса бранова должина, а катодните, α и β зраците се однесуваат како снопови од наелектризирани честички.
Новите откритија наметнаа размислување за концепцијата на атомот, чија реализација започна со започнувањето 20 век, а врз основа на акумулираните откритија. Се дозна дека атомот е електронеутрален, но се очекуваше дека електростатичките сили кај него да бидат од примарно значење. Според откритијата, електронот беше кандидат за носител на негативното електричество.
Атомски модели[уреди | уреди извор]
Вилјем Томсонов модел[уреди | уреди извор]
Првиот атомски модел е предложен од Вилјем Томсон во 1898, според кој атомот е топче со полупречник приближно еднаков на 0,1 nm во кое е распределено позитивно електричество, а на определени места во него се наоѓаат негативните електрони, кои придонесуваат атомот надворешно да манифестира неутралност. Овој модел беше скромна претпоставка и без експериментална поддршка.
Класичен модел[уреди | уреди извор]
Џозеф Џон Томсон во 1904 го развил класичниот модел на атомот, базирајќи се на претпоставката дека зрачењето од атомот треба да се покорува на максвеловите равенки на класичната електромагнетна теорија и дека динамиката на атомот треба да е во согласност со Њутновите закони од класичната механика. Според тоа, електроните во неговиот модел не се во статичка, туку во осцилирачка (динамичка) состојба.
Радерфордов модел[уреди | уреди извор]

Врз основа на експерименталните факти од страна на Ернест Радерфорд е предложен нов модел на атомот. Тој се заснова на резултатите добиени од Гајгер (студент на Радерфорд), кој имал задача да го регистрира расејувањето на α-честичките од тенка златна фолија со дебелина од неколку илјади атомски слоеви. Подоцна ќе биде објаснето дека α-честичките се двојно позитивно јонизирани хелиумови јадра.
Експериментирањата на Гајгер покажаа дека фолијата од злато не е некоја позначајна препрека за поминување на α-честичките. Најголемиот број од честичките поминуваат низ фолијата, определен број се отклонуваат од нивната првобитна насока, а многу мал број се рефлектираат од самата фолија. Според расудувањата на Радерфорд, расејувањето на α-честичките се должи на кулоновите сили од јадрата на златото кои се концентрирани на многу мал волумен во атомите од златото. Овие експериментирања дадоа можност да се процени големината на атомот и на атомското јадро.
Ако α-честичката е со полнеж q = + ze (z е атомски број, за златото неговата вредност е 79), тогаш потенцијалната енергија на системот ќе биде:
Со доближуавње на α-честичката до атомот на златото, кулоновата сила кинетичката енергија ја трансформира во потенцијална, од каде следува:
Од овде е можно да се определи големината на полупречникот на позитивниот полнеж кој ќе ја запре или пренасочи ;alpha;-честичката. Најголемо можно доближување на честичката е:
Направените пресметки од страна на Радерфорд покажуваат дека атомското јадро е со полупречник од редот на големината 10−15-10−14, а полупречникот на атомот е од редот на 10−10 m. Според тоа, позитивното количество што го содржи атомот е сконцентрирано во негов мал централен дел наречен јадро или nucleus на латински. Поради тоа повеќето α-честички кои наидуваат на фолијата од злато не се среќаваат со позитивните атомски јадра.
Планетарен модел[уреди | уреди извор]
- Главна статија: Планетарен модел на атомот.
Со Радерфордовата претпоставка за расејувањето на α-честичките се создадоа услови за појава на планетарниот модел за градбата на атомот. Според него, најголемото количество на маса е сконцентрирано во централниот дел, околу кој кружат електроните, слично како планетите околу Сонцето.
Боров модел[уреди | уреди извор]
- Главна статија: Боров модел на атомот.
Напорите кон создавање на стабилен модел на атомот не престанаа со добивањето на претставата за планетарниот модел. Нилс Бор во 1913 година направи една од најславните примени на енергетското квантување на системите во микросветот. Боровиот модел на атомот е претставен низ неговите три („Борови“) постулати:
- Секој атом може да постои само во определени (дискретни) атомски состојби кои одговараат на определени енергетски состојби E1, E2, E3... Во овие состојби атомот ниту емитира, ниту апсорбира енергија. Затоа овој постулат е наречен постулат на стационарните состојби.
- Атомот емитира (или апсорбира) енергија само при преминот од една стационарна состојба во друга. Преминот од повисоко кон пониско енергетско ниво е придружено со емисија на енергетски квант (hv = En - Em), а обратно со апсорпција. Овој постулат е наречен правило на честотите: v = (En - Em) / h.
- На стационарните состојби соодветствува движење на електронот по кружни орбити со определен полупречник r. При движењето по стационарните орбити, импулсниот момент на електронот L ги прима дискретните (квантизирани) вредности:
каде што n = 1, 2, 3, ...; m е маса на електронот, а v е линиската брзина. Константата h / 2π = 1,05 10−34 Js е квантната единица на импулсниот момент. Третиот Боров постулат е наречен правило за квантување на орбитите.
Квантномеханички модел[уреди | уреди извор]
- Главна статија: Квантномеханички модел на атомот.
Врз основа на добиените сознанија за квантната механика (1925) беше создаден новиот квантномеханички модел на атомското јадро, кој во себе ја вклучува идејата за квантување при опишување на состојбата на атомот. Притоа се искористени сознанијата за брановидност при движење на електроните, поради што овде се користи брановата функција. Во таа смисла, електронот нема свое количество на движење и координати, што би се користеле од класичната механика, туку ќе се разгледува веројатноста тој да се најде во одредена зона и соодветна точка во доменот на атомот.
Атомска орбитала[уреди | уреди извор]
- Атомска орбитала е математичка функција која го опишува брановидното однесување на електроните во еден атом. Тргнувајќи од оваа функција, може да се одреди (пресмета) регионот во кој може да се најде електронот кој кружи околу еден атом. Всушност, атомските орбитали ги претставуваат можните квантни состојби на еден електрон во електронскиот облак околу еден атом.
Електронски атомски и молекулски орбитали. Табелата со орбитали (на лево) е одредена со зголемувањето на енергијата (види Маделунгово правило). Забележи дека атомските орбитали се функции од три променливи (два агли и растојанието од атомското јадро, r). Овие илустрации ја претставуваат аголната компонента на орбиталата, а не целосната орбитала. Идејата за орбитоидното движење на електроните внатре во атомот била за првпат објавена во 1904 година. Од 1913, па до 1926 година, за електроните се мислело дека кружат околу атомското јадро на сличен начин како планетите околу Сонцето. Објаснувањето на природата на електронските "орбити" било една од главните причини за развојот на квантната механика. Во квантната механика, атомските орбитали се дефинираат како бранови функции над просторот, индексирани со квантните броеви n, l и m на орбиталата, или со имињата користени при електронските конфигурации, како што е покажано на десно. Бидејќи електроните неможат да се опишат како цврсти честички (како што е планетата), посоодветна аналогија за дефинирање на електронот е онаа која вели дека тој претставува чудно обликувана атмосфера (облак) која кружи околу релативно мала планета (атомското јадро). Поради разликите кои постојат со класично-механичките орбити, терминот „орбита“ (која го опишува движењето на електроните околу атомот) е заменет со орбитала. Имињата на орбиталите (s, p, d, f, g, h,...) се изведени од одликите на нивните спектроскопски линии: sharp (остра), principal (главна), diffuse (дифузна) и fundamental (основна), а останатите се именуваат по азбучен ред.
Атомот како тема во уметноста и во популарната култура[уреди | уреди извор]
Атомот се јавува како тема во некои дела од уметноста и популарната култура, како:
- „Верувам во атомите“ (Verujem u atome) - песна на српската поетеса Десанка Максимовиќ од 1983 година.[1]
- „Атомска градина“ (Atomic Garden) - песна на американската хард-кор група „Бед релиџн“ (Bad Religion).[2]
- „Атомизер“ (Atomizer) - албум на американската рок-група „Биг Блек“ (Big Black) од 1986.[3]
Наводи[уреди | уреди извор]
- ↑ Desanka Maksimović, Izabrane pesme (peto dopunjeno izdanje). Beograd: BIGZ, 1985, стр. 128.
- ↑ YouTube, Bad Religion - Atomic Garden (пристапено на 13.1.2017)
- ↑ YouTube, Big Black - Atomizer (Full Album) (пристапено на 14.5.2017)
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|




