Орбитален квантен број
| Квантна механика |
|---|
Орбитален квантен број - квантен број за атомската орбитала што го одредува импулсот на орбиталната аголна динамика и го претставува обликот на орбитата. Овој број е втор од низа на квантни броеви кои ја опишуваат уникатната квантна состојба на еден електрон (другите главни квантни броеви, според спектроскопската нотација се магнетниот квантен број и спинскиот квантен број). Тој е исто така познат како квантен број на орбитален аголен момент, орбитален квантен број или втор квантен број, и е претставен со ℓ.
Изведување[уреди | уреди извор]
Поврзани со енергетските состојби на електроните во атомот се четирите квантни броеви: n, ℓ, mℓ, and ms. Овие броеви ја претставуваат комплетната и уникатна квантна состојба на еден електрон во атомот, и ја сочинуваат неговата бранова функција или орбита. Брановата функција на Шредингеровата равенка се менува во три равенки, кои решени ги даваат првите три квантни броеви. Затоа, равенките за првите три квантни броеви се меѓусебно поврзани. Орбиталниот квантен број настанал во решението на поларниот дел од равенката за брановата функција како што е прикажано подолу. Да се помогне во разбирањето на овој концепт на азимут, исто така може да се проверат сферични координатни системи, или други алтернативни математички координатни системи покрај Декартовиот координатен систем. Општо земено, сферичните координатни системи работат најдобро со сферични модели, цилиндрични системи со цилиндри, итн.
Аголниот момент на еден атомски електрон, L, е поврзан со неговиот квантен број ℓ со следната равенка :
каде ħ е намалената Планкова константа, L2 е орбиталниот аголен момент и е брановата функција на електроните. Квантниот број ℓ е секогаш позитивен цел број : 0,1,2,3 итн. Додека голем број на учебници за основата на квантната механика ќе се однесуваат на L само по себе, L нема вистинско значење освен неговата употреба како операторот за аголниот момент. Кога се однесува на аголен момент, подобро е да се користи квантениот број ℓ.

Атомските орбитали имаат карактеристични форми означени со букви. На илустрацијата, буквите ѕ, p и d го опишуваат обликот на атомската орбитала.
Нивните бранови функции се во форма на сферични хармоники, и така се опишани од страна Лежандреевите полиноми. Различните орбитали кои се однесуваат на различни вредности на ℓ се понекогаш наречени под- школки, и (главно од историски причини) се означени со букви, како што следува:
ℓ Буква Макс. бр. на електрони Облик Име 0 s 2 сфера s остра 1 p 6 три ѕвона p принципална 2 d 10 четири ѕвона или единечна d дифузна 3 f 14 осум ѕвона или двојна f фундаментална 4 g 18 5 h 22 6 i 26
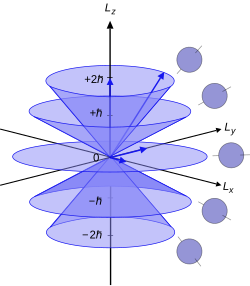
Секоја состојба на различните аголни моменти може да земе 2( 2ℓ + 1) електрони. Тоа е затоа што третиот квантен број mℓ (што може да се смета како квантна проекција на векторот на аголниот моментум на z-оската) трае од −ℓ to ℓ во множеството на цели броеви, и така постојат 2ℓ +1 можни состојби. Секоја посебна n, ℓ, mℓ орбитала може да биде заземена од страна на два електрона со спротивни спинови (дадени од квантниот број ms), давајќи 2( 2ℓ + 1) електрони во целина. Орбитали со повисоки ℓ од дадените во табелата се совршено дозволени, но овие вредности ги покриваат сите досега откриени атоми.
За дадена вредност на основниот квантен број n, можни вредности на ℓ се во опсег од 0 до n-1; според тоа, слојот n= 1 поседува само s подслој и може да прими само 2 електрони, n= 2 слојот поседува s, и р подслоeви и може да прими 8 електрони во целост, n= 3 слојот поседува ѕ, р и d подслоеви и има максимум од 18 електрони, и така натаму. Општо земено, максималниот број на електрони во n- нивото на енергија е 2n2. Квантниот број на аголниот момент ℓ, го одредува бројот на рамнински јазли кои минуваат низ јадрото. Во s орбитала, јазли не минуваат низ јадрото, и според тоа соодветниот орбитален квантен број ℓ има вредност 0. Во p орбиталата, еден јазол преминува низ јадрото и затоа ℓ има вредност од 1. L има вредност √2ħ. Во зависност од вредноста на n, постои квантен број на аголниот момент ℓ и следните серии. Наведените бранови должини се за водороден атом:
n= 1, L = 0, Лајманова серија(ултравиолетово) n= 2, L = √2ħ, Балмерова серија(видно достапна) n= 3, L = √6ħ, Пашенова серија (речиси инфрацрвена) n= 4, L = 2√3ħ, Брекетова серија (инфрацрвена со кратка бранова должина) n= 5, L = 2√5ħ, Пфундова серија (инфрацрвена со средна бранова должина).
Собирање на квантни аголни моменти[уреди | уреди извор]
Кај даден вкупен квантен аголен момент кој е збир од два поединечни аголни моменти и ,
магнитудата на квантниот број може да се движи од до каде и се квантни броеви кои одговараат на магнитудите на поединечните аголни моменти.
Вкупниот аголен момент на еден електрон во атомот[уреди | уреди извор]

Како резултат на спин-орбита заемодејството на атомот, орбиталниот аголен момент веќе не е комутативен со Хамилтоновиот оператор, ниту пак со спиновите. Затоа тие се менуваат со текот на времето. Сепак, вкупниот аголен момент J е комутативен со Хамилтоновиот оператор и е констатнтен. J е дефиниран преку
каде L е орбиталниот аголен момент и S се спиновите. Вкупниот аголен момент го задоволува истиот комутативен однос како орбиталниот аголен момент,
:
од кое што следува
:
каде Ji ги заменува Jx, Jy, и Jz.
Квантните броеви кои го опишуваат системот, а се константи во текот на времето, сега се j и mj, дефинирани преку дејството на J за брановата функција
Така што j е поврзан со нормата на вкупниот аголен моментум и mj до својата проекција при одредена оска .
Како и со било кој оператор на аголен момент во квантната механика, проекцијата на J по други оски не може да биде ко-дефинирана со Jz, затоа што тие не се комутативни.
Односот меѓу новите и старите квантните броеви[уреди | уреди извор]
j и mj, заедно со парноста на квантните состојби, ги заменуваат трите квантни броеви ℓ, mℓ и ms (проекцијата на спинот при одредена оска). Претходните квантни броеви можат да се поврзат со овие.
Понатаму, вектори од j, s, mj и парноста, кои се вектори на Хамилтоновиот оператор, се линеарни комбинации на векторите накои исто така се вектори на Хамилтоновиот оператор, се линеарни комбинации на векторите на ℓ, s, mℓ and ms.
Список на квантни броеви за аголен момент[уреди | уреди извор]
- Квантен број за спински аголен момент (спински квантен број)
- Квантен број за орбитален аголен момент
- Магнетен квантен број, поврзан со квантниот број за орбитален момент
- Квантен број за вкупен аголен момент
Историја[уреди | уреди извор]
Орбиталниот квантен број бил пренесен од Боровиот модел на атомот, а бил утврден од страна на Арнолд Зомерфелд.[1] Моделот на Бор бил изведен од спектроскопските анализи на атомот во комбинација со атомскиот модел на Радерфорд. Најниското квантно ниво има аголна динамика нула. Орбити со нула аголен момент биле сметани за осцилирачки полнежи во една димензија и така се опишуваат како "нишало" орбити.[2] Во три димензии орбитите стануваат сферични без јазли кои минуваат низ јадрото, слично (во состојба на најниска енергија) на јаже за скокање кое осцилира во еден голем круг.
Поврзано[уреди | уреди извор]
- Оператор на аголен момент
- Основна квантна механика
- Честичка во сферно симетричен потенцијал
- Квантен број
- Клебш-Горданови коефициенти
Наводи[уреди | уреди извор]
- ↑ Аизберг, Роберт (1974). Квантна физика на Атоми, Молекули, Тврди тела, Јадра, и Честички. Њујорк: Џон Вајли и синови. стр. 114–117. ISBN 978-0-471-23464-7.
- ↑ Р.Б. Линдзи (1927). „Белешки за "нишало" орбитите на атомските модели“. Случувања на Националната академија за наука. 13: 413–419. Bibcode:1927PNAS...13..413L. doi:10.1073/pnas.13.6.413.[мртва врска]
Надворешни врски[уреди | уреди извор]
- Development of the Bohr atom
- Pictures of atomic orbitals Архивирано на 21 април 2012 г.
- Detailed explanation of the Orbital Quantum Number l Архивирано на 28 март 2006 г.
- The azimuthal equation explained














![{\displaystyle [J_{i},J_{j}]=i\hbar \epsilon _{ijk}J_{k}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1c774fd99fb91eb8937cbaaa6b6af2eaf88e7ad6)
![{\displaystyle \left[J_{i},J^{2}\right]=0}](https://wikimedia.org/api/rest_v1/media/math/render/svg/df773fc4aa955999fbf21070fb2d56ae4252b0ef)

