Фациоскапулохумерална мускулна дистрофија
| Фациоскапулохумерална мускулна дистрофија | |
|---|---|
 | |
| Дијаграмот ги прикажува мускулите кои се најчесто погодени од ФСХД | |
| Специјалност | Неурологија, неуромускуларна медицина |
| Симптоми | слабост и атрофија на мускулите |
| Компликации | Хронична болка, сколиоза Ретко: респираторна инсуфициенција, губење на слухот |
| Вообичаена појава | Околу 15 до 30-тата година |
| Времетраење | цел живот |
| Видови | ФСХД 1, ФСХД 2 |
| Причинители | Генетска (наследна или нова мутација) |
| Дијагностички метод | според испитувања на серумска креатинкиназа, електромиограм, генетското тестирање |
| Лекови | Лек не постои , но се користат други третмани и лекови за намлување на прогресот на болеста |
| Прогноза | Прогресивен, непроменет животен век |
| Честота | 4/100.000 |
Фациоскапулохумерална мускулна дистрофија ( ФСХД, Facioscapulohumeral Muscular Dystrophy MКБ 10:G71.02 преваленца/распространетост: 4/100.000 ) е ретко, генетско, прогресивно, мускулно нарушување кај кое најзасегнати се мускулите на лицето, лопатките и надлактиците. Името на оваа болест доаѓа од facies (латински збор и медицински термин за лице); scapula (латински збор и анатомски термин за лопатката на рамото) и humerus (латински збор за надлактицата и анатомски термин за коска што се наоѓа меѓу рамото и лактот). Терминот мускулна дистрофија означува прогресивна мускулна дегенерација (пропаѓање) проследена со слабост и атрофија на мускулите.Слабоста најпрво и најсериозно ги зафаќа лицето, рамената и надлактиците, но болеста обично предизвикува слабост и на другите мускули. Оваа дистрофија е третиот најчест тип на мускулна дистрофија, по мускулните дистрофии на Душен и Бекер и миотоничната дистрофија.
Речиси секој скелетен мускул може да биде засегнат при тешка форма на болеста. Ненормално позиционирани или крилести лопатки се вообичаени, како и неможноста да се подигне стапалото. Двете страни на телото често се погодени асиметрично. Слабоста обично се манифестира на возраст од 15-30 години. ФСХД, исто така, може да предизвика губење на слухот и абнормалности на крвните садови во задниот дел на окото .
ФСХД е предизвикана од генетска мутација што доведува до дерегулација на генот DUX4 . Нормално, генската експресија на DUX4 (е вклучен) во клетките на јајниците уште во раниот човечки развој, а станува потиснат (или исклучен) во моментот кога ембрионот е стар неколку дена. Во ФСХД, DUX4 е несоодветно потиснат, што овозможува спорадично изразување во текот на животот. Бришењето на ДНК во регионот што го опкружува DUX4 е предизвикувачката мутација во 95% од случаите, наречена „ контракција на D4Z4 “ и дефинирање на ФСХД тип 1 . А друга мутациа е ФСХД тип 2 . За да се развие болеста, потребен е и алел 4qA, што е вообичаена варијација во ДНК до DUX4 . Шансите D4Z4 контракција со 4qA алел да се пренесе на дете се 50% ( автосомно доминантна ); Мутациите на ФСХД предизвикуваат несоодветна репресија на DUX4 со еукромахин на ДНК околу DUX4, што го прави пристапен за копирање во информациска РНК (mRNA). Алелот 4qA ја стабилизира оваа DUX4 mRNA, овозможувајќи му да се користи за производство на белковина DUX4. Белковината DUX4 е модулатор на стотици други гени, од кои многу се вклучени во мускулната функција. Сè уште не е разјаснето како оваа генетска модулација предизвикува оштетување на мускулите.
Знаците, симптомите, семејната историја и дијагностички тестови може да помогнат во дијаностицирањето на ФСХД; а генетското тестирање може да обезбеди конечна дијагноза. Превенцијата од различни компликации и интервенции се постигнува преку скринингот. Симптомите може да се решат со физикална терапија и реконструктивна хирургија како што е хируршка фиксација на лопатката на градниот кош. Прогнозата е променлива. Иако дел од пациентите (во 20% од случаите) има потреба од инвалидска количка или скутер голем дел од останатите пациенти се непопречени во секојдневниот живот. Животниот век не зависи од болеста, ретко има случаи во кои доаѓа до смрт поради респираторна инсуфициенција предизвикана од ФСХД. ФСХД за прв пат била истакната како болест во 1870-тите и 1880-тите кога француските лекари Луј Теофил Жозеф Ландузи и Џозеф Жил Дежерин се интересирале со семејство погодено од болеста, па затоа и првичното име кое го добила болеста била Ландузи-Дежерин мускулна дистрофија . Значењето на D4Z4 контракцијата на хромозомот 4 беше утврдено во 1990-тите. Генот DUX4 бил откриен во 1999 година, а во 2007 бил посочен како токсичен , а во 2010 година бил разјаснет неговиот генетскиот механизам. Во 2012 година, бил идентификуван генот кој најчесто мутира во ФСХД 2. Во 2019 година, првиот лек кои имал тенденција да се спротивстави на експресијата на DUX4 започнал со клинички испитувања.
Знаци и симптоми[уреди | уреди извор]
Кај околу 90% од пациентите, симптомите обично започнуваат пред 20-тата година во животот, со појава на слабост и атрофија на мускулите околу очите и устата, рамената, стомачните мускули, горниот дел од рацете и долниот дел на нозете, обично со асиметрично зафаќање. Повеќето лица забележуваат некои проблеми до 20-тата година од животот, иако слабоста на некои мускули може да започне уште во детството и до 50-тите години. Кај некои лица, болеста може да биде толку блага што не се забележуваат никакви симптоми. Во овие случаи, болеста може да се дијагностицира само откако друг, позасегнат член од семејството ќе побара медицинска помош.
Некои експерти ја делат оваа дистрофија на две форми: со почеток кај возрасни лица и инфантилна форма – со почеток кај доенчиња. Почетокот кај возрасните лица обично започнува во адолесценцијата и оваа форма е многу почеста. Кај секоја форма на ФСХД, слабоста на мускулите на лицето може да започне во детството. Засегнатите лица често не одат на доктор додека не им бидат зафатени мускулите на рамото или ногата и не доживеат потешкотии да ја дофатат главата со рацете или да се качат и спуштат по скали. Кога внимателно ќе бидат испрашани, лицата можат да се сетат дека имале симптоми уште во детството, како „заглавени“ лопатки или проблеми со фрлање на топка.Многу често, луѓето велат дека никогаш не можеле да свиркаат со уста или да надуваат балон или дека имале проблеми со пиење со сламка, но можеби овие проблеми не ги поврзувале со мускулна дистрофија. ФСХД со почеток кај доенчиња генерално има поизразен тек во однос на мускулната слабост, а понекогаш и влијае на слухот и видот. Прелиминарните докази сугерираат дека формата со почеток кај доенчиња е поврзана со поголем дефект во ДНК.
Распределбата и степенот на мускулна слабост е исклучително променлив, дури и помеѓу идентични близнаци.[1] Мускулно-скелетната болка е многу честа, најчесто во вратот, рамената, долниот дел на грбот и задниот дел на коленото.[2] Заморот е исто така чест. Мускулната слабост обично станува забележлива на едната страна од телото пред другата, што е одлика на болеста. Мускулите на десното рамо и раката се почесто засегнати од мускулите на левиот горен екстремитет. :139 Инаку, ниту една страна од телото не е изложена на поголем ризик. Класично, симптомите се појавуваат кај оние на возраст од 15 до 30 години, иако се јавуваат и инфантилен почеток, почеток на возрасни и отсуство на симптоми и покрај тоа што имаат причинска генетика.[3] ФСХД 1 со многу големо бришење на D4Z4 ( <i id="mwoQ">Eco</i> RI 10–11 kb ) е посилно поврзано со инфантилен почеток и посериозна слабост. Во просек, ФСХД 2 се појавува 10 години подоцна од типот 1. Инаку, ФСХД 1 и ФСХД 2 не се разликуваат по основ на слабост. Прогресијата на болеста е бавна, а долгите статични фази, во кои не е очигледна прогресија, не се невообичаени. Поретко, индивидуалните мускули брзо се влошуваат во текот на неколку месеци.
Лице[уреди | уреди извор]
Слабост на мускулите на лицето е најпрепознатливиот знак на ФСХД.[3] Тоа е типично најраниот знак, иако ретко е првична причина поради која се бара медицинска помош.[3] Иако блага, слабоста на лицето може да се најде кај 90% или повеќе , од случаите.[4][5] Еден од најчестите недостатоци е неможноста да се затворат очните капаци, што може да резултира со спиење со отворени и суви очи.[3] Имплицираниот мускул е орбикуларниот окул мускул.[3] Друг вообичаен дефицит е неможноста да се стискаат усните, што предизвикува неспособност за свиркање или дување балон.[3] Имплицираниот мускул е мускулот орбикуларис орис .[3] Трет вообичаен дефицит е неможноста да се подигнат аглите на устата, што предизвикува „хоризонтална насмевка“.[3] Одговорен е зигоматичниот главен мускул.[3]
Слабоста на различните мускули на лицето придонесува за тешко изговарање на буквите М, Б и П. Лицето може да делува арогантно, мрзливо или уморно.[3] Мускулите што се користат за џвакање и движење на очите не се засегнати.[5][6] Тешкотиите при голтање не се типични, иако може да се појават во посериозни случаи.[7][8] ФСХД е генерално прогресивен, но не е утврдено дали слабоста на лицето е прогресивна или стабилна во текот на животот.[9]
Рамо, гради и раце[уреди | уреди извор]

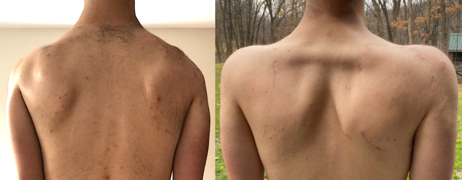
По слабоста на лицето, слабоста обично се развива во мускулите на градниот кош и оние што се протегаат од лопатките до градниот кош. Симптомите кои го вклучуваат рамото, како што е отежнатото работење со рацете над главата, се првичните поплаки во 80% од случаите.[5][6] Претежно, се засегнати предните сератусни и средните и долните трапезести мускули ;[3] горниот трапезен мускул често е помалку засегнат.[6] Слабоста на трапезиусот предизвикува скапулата да се ротира надолу , што резултира со крилести лопатки(скелетна медицинска состојба во која лопатките излегува/стрчат од грбот посебно видливи во абнормална положби.) , хоризонтални клавикули и свиткани раменици. Слабостите на сerratus-от(назабен преден мускул) ја нарушуваат флексијата на раката, а влошувањето на положбата на крилата може да се покаже кога се турка на ѕид , како на сликата. Мускулите што се протегаат од скапулата до раката генерално се поштедени[3][10][11]
Слабоста на мускулите може да ги направи коските многу видливи, карактеристичен пример е знакот „поли-рид“ кој може да се забележи кога ќе се подигне на раката.[3] Првиот „планина“ или испакнатина е горниот агол на скапулата што е поставена нагоре над реброто. Втората испакнатина е AC спој, кој се забележува помеѓу горениот трапезиус и горениот делтоид. Третата испакнатина е долниот делтоиден, што може да се разликува помеѓу горен делтоиден и залудените мускули на хумерусот.[3] Слабоста и болката во рамото може да доведат до нестабилност на рамото, како што е повторлива дислокација, сублуксација или надолно преведување на главата на хумерусот .
Зафатени се и градниот кош, особено деловите на големиот пекторален мускул што се поврзуваат со градната коска и ребрата. Поретко е засегнат делот што се поврзува со клучната коска. Оваа слабост на мускулите може да придонесе за истакнато хоризонтално предно аксиларно превиткување . Надвор од оваа точка, болеста не напредува понатаму во 30% од познатите случаи. По слабоста на горниот дел од торзото, слабоста може да се „спушти“ до надлактиците ( бицепсниот мускул и, особено, трицепсниот мускул ). Подлактиците обично не се зафатени што резултира со изглед што некои го споредуваат со измислениот лик Попај, иако кога подлактиците се погодени во потешка форма на болеста, екстензорите на зглобот се почесто засегнати.
Долниот дел од телото и трупот[уреди | уреди извор]
По горниот дел од телото, слабоста може да се појави или во карлицата, или да ја „прескокне“ карлицата и да го зафати предниот тибијалис (шин мускул), предизвикувајќи пад на стапалото . Еден автор сметал дека мускулите на карлицата и бутовите се последната засегната група. Слабоста на карличните мускули може да се манифестира како искривување на карлицата, предизвикувајќи колковите да се држат во мала флексија. Слабоста на карлицата може да предизвика и знак Тренделенбург. Слабост на мускулот на задниот дел на бутот (е почеста од слабоста на предниот дел на бутот (квадрицепс).
Слабост може да се појави и во стомачните мускули и параспиналните мускули, што може да се манифестира како испакнат абдомен и лумбална хиперлордоза. Абдоминалната слабост може да предизвика неможност да се свртите од една на друга страна додека лежите на грб. Од ректусниот абдоминис мускул, преференцијално е засегнат долниот дел, кој се манифестира како позитивен Биворов знак. Во напредни случаи, слабоста на екстензорите на вратот може да предизвика главата да се наведне кон градниот кош, наречен пад на главата.
Немускулести[уреди | уреди извор]

Најчеста не-мускулно-скелетна манифестација на ФСХД е абнормалност во малите артерии ( артериоли ) во мрежницата . Тортуозноста на артериолите е забележана кај околу 50% од оние со ФСХД. Поретки артериоли абнормалности вклучуваат телеангиектазии и микроаневризми .[12][13] Овие абнормалности на артериолите обично не влијаат на видот или здравјето, иако тешката форма е иста со она што се среќава кај Коатовата болест, состојба која се среќава во околу 1% од случаите и често е поврзана со големи бришења на 4q35. Високофреквентно губење на слухот може да се појави кај оние со големи бришења на 4q35, но во спротивно не е почеста во споредба со општата популација. Големото бришење 4q35 може да доведе до разни други ретки манифестации.[14]
Сколиозата исто така се среќава и се смета дека е резултат на слабост на стомачните мускули, екстензорите на колкот и мускулите на ’рбетот. Спротивно на тоа, сколиозата може да се гледа како компензаторен механизам за слабост. Дишењето може да биде засегнато, поврзано со кифосколиозата која се забележува кај една третина од пациентите кои користат инвалидска количка. Сепак, поддршка од вентилатор (навечер или преку ден) потребно е само во 1% од случаите. И покрај тоа што постојат извештаи за зголемен ризик од срцеви аритмии, општ консензус е дека срцето не е засегнато.
Причина[уреди | уреди извор]
Оваа болест може да се наследи автосомно-доминантнo, преку таткото или мајката, или може да се појави без семејна историја кај околу 30% од лицата. Најверојатната причина е генетска грешка (мутација) која доведува до несоодветна експресија на генот double homeobox protein 4 (DUX4) на хромозомот 4, во регионот D4Z4.Сегментот не е дел од некој посебен ген, но сепак се чини дека се меша во правилната обработка на генетскиот материјал. Научниците досега опишале два типа на ФСХД: Тип 1 и Тип 2. Двата типа обично имаат исти знаци и симптоми и се разликуваат по нивната генетска причина. ФСХД1 е предизвикан од промени во регионот на хромозомот 4 наречен D4Z4 што резултира со абнормална активација на генот DUX4. Мутациите во генот наречен SMCHD1 се основната причина за ФСХД2.

Генетиката на ФСХД е сложена. ФСХД и миотоничните дистрофии имаат уникатни генетски механизми кои значително се разликуваат од останатите генетски миопатии. Генот DUX4 е фокусна точка на ФСХД генетиката. Нормално, DUX4 се изразува за време на ембриогенезата, а подоцна се потиснува во сите ткива освен тестисите . Кај ФСХД, постои неуспех на репресијата на DUX4 и континуирано производство на белковина DUX4, кој е токсичен за мускулите. Механизмот на неуспешна репресија на DUX4 е хипометилација на DUX4 и неговата околна ДНК на врвот на хромозомот 4 (4q35), што овозможува транскрипција на DUX4 во информациската РНК (mRNA). Неколку мутации може да резултираат со болест, по која болеста се подкласифицира во ФСХД тип 1 (FSHD1) и ФСХД тип 2 (FSHD2). Болеста може да резултира само кога е присутна мутација во комбинација со избрани, најчесто пронајдени варијации на 4q35, наречени хаплотипски полиморфизми . Постојат најмалку 17 4q35 хаплотип полиморфизми, грубо поделени во групите 4qA и 4qB. Полиморфизам на хаплотип 4qA, честопати познат како алел 4qA, е неопходен за болеста, бидејќи содржи полиаденилација низа која овозможува DUX4 mRNA да се спротивстави на деградацијата доволно долго за да се транслатира во DUX4 белковина.
DUX4 и низата за повторување D4Z4[уреди | уреди извор]

| CEN | центромерен крај | TEL | теломерен крај |
| NDE кутија | неизбришан елемент | PAS | полиаденилација |
| триаголник | повторување на D4Z4 | трапезоид | делумно повторување на D4Z4 |
| бела кутија | pLAM | сиви кутии | DUX4 егзони 1, 2, 3 |
| стрелки | |||
| ќош | промотори | прави | РНК транскрипти |
| црни | смисленост | црвени | антисмисленост |
| сини | DBE-T | цртички | места за коцки |
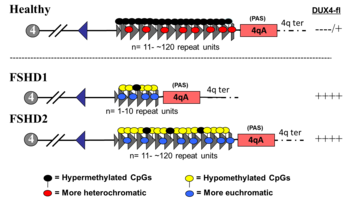
DUX4 се наоѓа во низата за повторување на макросателитот D4Z4, серија од тандемски повторени ДНК сегменти во субтеломерниот регион (4q35) на хромозомот 4 .[15] Секое повторување на D4Z4 е долго 3,3 килобазни парови (kb) и е место на епигенетска регулација, што ги содржи и хетерохроматинските и еухроматинските структури. Во ФСХД, структурата на хетерохроматин се губи, станувајќи еухроматин.
Субтеломерниот регион на хромозомот 10q содржи тандем-повторлива структура високо хомологна (99% идентична) со 4q35, која содржи повторувања „како D4Z4“ со региони за кодирање на белковини идентични со DUX4 (D10Z10 повторувања и DUX4L10, соодветно). Бидејќи на 10q обично му недостасува низа на полиаденилација, тој обично не е поврзан со болеста. Сепак, хромозомските преуредувања може да се случат помеѓу низи од 4q и 10q, а вклученоста во болеста е можна ако сигналот за повторување 4q D4Z4 и полиаденилација се префрли на 10q, или ако преуредувањето предизвикува ФСХД1.
DUX4 се состои од три егзони . Егзоните 1 и 2 се во секое повторување. Егзон 3 е во plAM регионот теломерен до последното делумно повторување. Повеќекратни транскрипти на РНК се произведуваат од низата за повторување D4Z4, и смисленост и антисмисленост. Некои транскрипти може да се деградираат во области за да се произведат мали РНК. Некои транскрипти кои потекнуваат од центромерна низа за повторување на D4Z4 кај неизбришаниот елемент (NDE), наречени транскрипти на регулаторни елементи D4Z4 (DBE-T), може да играат улога во дерепресијата на DUX4. Еден предложен механизам е дека DBE-T води до регрутирање на белковината Ash1L од групата триторакс, зголемување на метилацијата на H3K36me2 и на крајот дерепресија на гените 4q35.
ФСХД 1[уреди | уреди извор]
ФСХД што вклучува бришење на повторувањата на D4Z4 (наречен „D4Z4 контракција“) на 4q е класифициран како ФСХД 1, што претставува 95% од случаите на болеста. Типично, хромозомот 4 вклучува помеѓу 11 и 150 D4Z4 повторувања. Во типот 1, има 1-10 D4Z4 повторувања. Бројот на повторувања е приближно обратно поврзан со тежината на болеста. Имено, оние со 8 - 10 повторувања имаат тенденција да имаат најблаги форми на болеста, понекогаш без симптоми; оние со 4 - 7 повторувања имаат умерена сериозност која е многу променлива; а оние со 1 - 3 повторувања имаат поголема веројатност да имаат тешка форма, атипична и ран почеток на болеста. Бришењето на целата низа за повторување на D4Z4 не резултира со ФСХД бидејќи тогаш нема да се изразат целосни копии на DUX4, иако резултираат други вродени дефекти.[16] Една договорена D4Z4 повторувачка низа со соседен алел 4qA е доволна за да предизвика болест, така што наследувањето е автосомно доминантно . De novo (нови) мутации се вмешани во 10-30% од случаите, од кои 50% покажуваат соматски мозаицизам .
ФСХД 1 е подложен на антиципација, тренд првенствено поврзан со нарушувања на повторувањето на тринуклеотид во кои манифестацијата на болеста се влошува со секоја следна генерација.
ФСХД 2[уреди | уреди извор]
ФСХД без D4Z4 контракција е класифициран како ФСХД 2, што сочинува 5% од случаите на ФСХД. Различни мутации предизвикуваат го предизвикуваат типот 2, сите гени за модификатори на хроматин кои резултираат со хипометилација на D4Z4, при што генетскиот механизам се конвергира со ФСХД 1. Приближно 80% од случаите на ФСХД 2 се должат на деактивирачки мутации во генот SMCHD1 на хромозомот 18 . SMCHD1 е одговорен за метилација на ДНК, а неговото деактивирање резултира со хипометилација на низата за повторување D4Z4. Друга причина за ФСХД 2 е мутацијата на DNMT3B (ДНК метилтрансфераза 3B), која исто така игра улога во метилацијата на ДНК. Почнувајќи од 2020 година, раните докази покажуваат дека третата причина за ФСХД 2 е мутација во двете копии на генот LRIF1, кој го кодира факторот 1 за интеракција на јадрениот рецептор зависен од белковинскиот лиганд (LRIF1). Познато е дека LRIF1 комуницира со белковината SMCHD1. Од 2019 година, веројатно има дополнителни мутации на други неидентификувани генетски локации кои можат да предизвикаат ФСХД 2.
Мутацијата на еден алел на SMCHD1 или DNMT3B може да предизвика болест. Привремено се покажало дека мутацијата на двете копии LRIF1 предизвикува болест кај едно лице од 2020 година. Како и кај ФСХД 1, алелот 4qA мора да биде присутен за да се појави болеста. Сепак, за разлика од низата D4Z4, гените вмешани во ФСХД 2 не се во близина со алелот 4qA и затоа се наследени независно од алелот 4qA, што резултира со дигена шема на наследување. На пример, едниот родител без ФСХД може да пренесе SMCHD1 мутација, а другиот родител, исто така без ФСХД, може да помине на алел 4qA, што резултира со дете со ФСХД 2.
Два краја на спектарот на болеста[уреди | уреди извор]
Првично, двата типа биле опишани како две посебни генетски причинители на истата болест. Сепак, на нив може да се гледа не како различни причинители, туку како фактори на ризик. Не ретко и двете придонесуваат за болеста кај иста личност.
Кај оние со ФСХД 2, иако немаат алел 4qA со D4Z4 повторен број помал од 11, тие сепак често имаат еден помал од 17 (релативно краток во споредба со општата популација), што сугерира дека голем број повторувања на D4Z4 може да спречат ефектите на SMCHD1 мутација. Потребно е да се направат дополнителни студии за да се одреди горната граница на повторувањата на D4Z4 во која може да се појави ФСХД 2.
Кај оние со 4qA алел и 10 или помалку повторувања, дополнителна SMCHD1 мутација се покажало дека ја влошуваат болеста, класифицувајќи ги и како ФСХД 1 и ФСХД 2. Кај овие поединци ФСХД 1/ФСХД 2, шемата на метилација на низата за повторување D4Z4 наликува на онаа што се забележува во типот 2. Оваа комбинирана презентација на двата типа е најчеста кај оние со 9 - 10 повторувања и ретко се среќава кај оние со 8 или помалку повторувања. Релативното изобилство на SMCHD1 мутации во групата со 9-10 повторувања е веројатно затоа што значителен дел од општата популација има 9-10 повторувања без никаква болест, но сепак со адитивниот ефект на SMCHD1 мутација, симптомите се развиваат и се поставува дијагноза. Кај оние со 8 или помалку повторувања, симптомите се поверојатни отколку кај оние со 9-10 повторувања, што доведува до дијагноза без оглед на дополнителна SMCHD1 мутација.
Очигледната фреквенција на случаите ФСХД 1/ФСХД 2 во опсегот од 9 - 10 повторувања, комбинирана со шемата на метилација слична на типот 2, сугерира дека големината на повторување од 9 - 10 е зона на преклопување помеѓу двата типа.
Патофизиологија[уреди | уреди извор]
Молекуларна[уреди | уреди извор]

Од 2020 година, постои консензус дека аберантното изразување на DUX4 во мускулите е причина за ФСХД.[17] DUX4 се изразува во екстремно мали количини, откриени во 1 од секои 1000 незрели мускулни клетки (миобласт), што делува дека се зголемува по созревањето на миобластот, делумно поради тоа што клетките се спојуваат додека созреваат, а едно јадро кое изразува DUX4 може да обезбеди DUX4 белковина до соседните јадра од споените клетки.[18]
Сепак активно се истражува како белковината DUX4 предизвикува оштетување на мускулите.[19] DUX4 белковината е фактор на транскрипција кој регулира многу други гени. Некои од овие гени се вклучени во апоптозата, како што се p53, p21, MYC и β-катенин, и изгледа дека белковината DUX4 ги прави мускулните клетки посклони кон апоптоза. Други гени регулирани со белковината DUX4 се вклучени во оксидативниот стрес, и експресијата на DUX4 ја намалува толеранцијата на мускулните клетки на оксидативниот стрес. Варијацијата во способноста на поединечните мускули да се справат со оксидативниот стрес може делумно да ги објасни шемите на вклучување на мускулите на ФСХД. DUX4 белковината намалува многу гени вклучени во развојот на мускулите, вклучително и MyoD, myogenin, desmin и PAX7, а експресијата на DUX4 ја намалува пролиферацијата, диференцијацијата и соединувањето на мускулните клетки . DUX4 белковината регулира неколку гени кои се вклучени во контролата на квалитетот на РНК, и се покажало дека експресијата на DUX4 предизвикува акумулација на РНК со последователна апоптоза.[17] Естрогенот игра улога во менувањето на ефектите на белковината DUX4 врз мускулната диференцијација, што објаснува зошто женките се помалку погодени од мажјаците.
Одговорот на клеточната хипоксија е разгледуван во една студија како главен двигател на смртта на мускулните клетки предизвикани од DUX4 белковината. Факторите кои предизвикуваат хипоксија (HIFs) се нагоре регулирани од белковината DUX4, што веројатно предизвикува патолошка сигнализација која води до клеточна смрт.[20]
Друга студија покажала дека експресијата на DUX4 во мускулните клетки доведело до регрутирање и промена на влакнести / масни прогениторни клетки, што помага да се објасни зошто мускулите се заменуваат со масно и фиброзно ткиво .[18]
Една студија го вклучила и RIPK3 во клеточна смрт посредувана од DUX4.[21]
Мускулна хистологија[уреди | уреди извор]

За разлика од другите мускулни дистрофии, раните мускулни биопсии покажувале само благ степени на фиброза, хипертрофија на мускулните влакна и поместување на јадрата од периферијата на миофибер (централно нуклеација). Почесто се среќава воспаление. Може да има ендомизијално воспаление, првенствено составено од ЦД8+ Т-клетки, иако се чини дека овие клетки не директно предизвикуваат смрт на мускулните влакна. Ендомизијалните крвни садови можат да бидат опкружени со воспаление, кое е релативно уникатно за ФСХД, а ова воспаление содржи ЦД4+ Т-клетки. Воспалението е проследено со таложење на маснотии (масна инфилтрација), потоа фиброза. Индивидуалните мускулни влакна може да изгледаат заоблени, изедено и, особено, лобулирани.
Шема на зафатеност на мускулите[уреди | уреди извор]
Зошто одредени мускули се преференцијално засегнати кај ФСХД останува непознато. Мускулите на десното рамо и раката почесто се засегнати од мускулите на левиот горен екстремитет, шаблон што се гледа и кај синдромот на Полска и наследна невралгична амиотрофија ; ова може да одразува генетски, развојен/анатомски или функционален механизам.[5][9][22]
Медицинските слики (копјутерска томографија и магнетна резонанца) покажале дека вклученоста на мускулите не е лесно видлива.[10] Заклучоци:
- Една студија со МРИ покажала дека големиот кос мускул (musculus teres major) е најчесто засегнат.[11]
- Полумембранозниот мускул(musculus semimembranosus) најчесто е засегнат,[22][23][24] што според еден автор се смета за „најчесто и најсилно погодениот мускул“.[25]
- Од квадрицепсните мускули, преференцијално е засегнат ректус феморис [23]
- Од гастрокемиусот, преференцијално е засегнат медијалниот дел;[23][24]
- Илиопсоасот, флексорниот мускул, многу често останува незасегнат.[24][25]
Ретинопатија[уреди | уреди извор]
Извртување на ретиналните артериоли, а поретко микроаневризми и телеангиектазии, најчесто се наоѓаат кај ФСХД.[12] Абнормалности на капиларите и венулите не се забележува.[12] Една теорија за тоа зошто артериолите се селективно засегнати е дека тие содржат мазни мускулно тквио .[12] Степенот на D4Z4 контракција е во корелација со сериозноста на тортуозноста на артериолите.[12] Се претпоставува дека ретинопатија се должи на DUX4-белковински поттикната модулација на CXCR4 - SDF1 оската, која има улога во клеточната морфологија на врвот на ендотелијата и васкуларното разгранување.[12]
Дијагноза[уреди | уреди извор]

За поставување на дијагноза, важни се симптомите и резултатите од следниве испитувања: серумска креатинкиназа, електромиограм, но генетското тестирање се користи за потврда на дијагнозата. Самата дијагноза може да се претпостави врз основа на знаци, симптоми и/или негенетски медицински тестови.[3] Во отсуство на утврдена семејна историја на ФСХД, дијагнозата може да биде тешка поради варијабилноста во тоа како се манифестира болеста.
Генетско тестирање[уреди | уреди извор]
Генетското тестирање е најсигурен начин за дијагностицирање на ФСХД. Најчесто, ФСХД 1 прво се тестира. Скратена должина на низата D4Z4 (должина Eco RI од 10 kb до 38 kb) со соседен алел 4qA соодвестуваат на типот 1. Ако типот 1 не е присутен, најчесто ФСХД 2 се тестира следно со проценка на метилацијата на 4q35. Ниска метилација (помалку од 20%) во контекст на алел 4qA е доволна за дијагноза. Специфичната мутација, обично една од различните SMCHD1 мутации, може да се идентификува со секвенционирање на следната генерација.[26]
Проценка на должината на D4Z4[уреди | уреди извор]
Мерењето на должината на D4Z4 е технички предизвик поради низата за повторување D4Z4 која се состои од долги, повторувачки елементи. На пример, секвенционирањето на следната генерација не може да се користи за проценка на должината на D4Z4, бидејќи ја разложува ДНК на фрагменти пред да ги прочита, и не е јасно од кое повторување D4Z4 доаѓа секој секвенциониран фрагмент. Во 2020 година, оптичкото мапирање станало достапно за мерење на должината на низата D4Z4, што е попрецизно и помалку трудоинтензивно од јужниот дел. Достапно е и молекуларно чешлање за проценка на должината на низата D4Z4. Овие методи, кои физички ја мерат големината на низата за повторување D4Z4, бараат специјално подготвена висококвалитетна и висока молекуларна геномска ДНК (gDNA) од серумот, зголемување на цената и намалување на пристапноста до тестирање.

Анализата на полиморфизмот со должина на рестриктивен фрагмент бил првиот генетски тест развиен и сè уште се користи од 2020 година, иако постепено престанува да се користи со доаѓањето на понови методи. Вклучува сецкање на ДНК на рестрикциони ензими и сортирање на добиените рестриктивни фрагменти по големина . Најчесто се користат рестриктивните ензими Eco RI и Bln I. Eco RI ги изолира низите за повторување 4q и 10q, а Bln I ја сече низата од 10q на мали парчиња, овозможувајќи да се разликува 4q. Фрагментот за рестрикција на Eco RI е составен од три дела: 1) проксимален дел од 5,7 kb, 2) централен со променлива големина D4Z4 повторувачка низа и 3) дистален дел, обично 1,25 kb. Проксималниот дел има низа од ДНК што може да се обојува со сондата p13E-11, која вообичаено се користи за визуелизација на фрагментот EcoRI . Името „p13E-11“ одразува дека тоа е субклон на ДНК секвенца означена како космид 13E за време на проектот за човечки геном. Имајќи предвид дека секое повторување на D4Z4 е 3,3 kb, а фрагментот Eco RI содржи 6,9 kb ДНК што не е дел од низата за повторување D4Z4, може да се пресмета бројот на D4Z4 единици.
- D4Z4 повторува = ( Eco RI должина - 6,9) / 3,3
Понекогаш 4q или 10q ќе имаат комбинација од повторувања слични на D4Z4 и D4Z4 поради размена на ДНК помеѓу 4q и 10q, што може да даде погрешни резултати, па потоа бара подетална обработка. Понекогаш D4Z4 повторувачките бришења на низата може да го вклучат местото за врзување p13E-11, што гарантира употреба на алтернативни сонди.
Проценка на статусот на метилација[уреди | уреди извор]
Статусот на метилација на 4q35 традиционално се оценува откако тестирањето за типот 1 е негативно. Дигестијата со рестриктивен ензим сензитивен за метилација (MSRE) што покажува хипометилација долго време се смета за дијагностика на типот 2. Други метилациски анализи се предложени или користени во истражувачки услови, вклучително имунопреципитација на метилирана ДНК и секвенционирање на бисулфит, но не се рутински користени во клиничката пракса.
Помошно тестирање[уреди | уреди извор]

Други тестови можат да ја потврдат дијагнозата на ФСХД, иако сите тие се помалку чувствителни и помалку специфични од генетското тестирање. Сепак, тие можат да исклучат слични состојби.
- Нивото на креатин киназа во крвта често се препорачува кога постои сомневање за оштетување на мускулите. Креатин киназа е ензим кој се наоѓа во мускулите, кој истекува во крвта кога мускулите ќе се оштетат. Кај ФСХД, нивото на креатин киназа е нормален до благо покачено, никогаш не надминува пет пати повеќе од горната граница на нормалата.
- Електромиограмот (ЕМГ) ја мери електричната активност во мускулите. ЕМГ може да покаже неспецифични знаци на мускулно оштетување или раздразливост.
- Брзината на нервната спроводливост ја мери брзината на движење на сигналите по нервот. Нервните сигнали се мерат со површински електроди (слични на оние што се користат за електрокардиограм) или иглени електроди.
- Мускулна биопсија е хируршко отстранување и испитување на мало парче мускул, обично од раката или ногата. За испитување се користат микроскопија и различни биохемиски тестови. Наодите во ФСХД се неспецифични, како што се присуство на бели крвни зрнца или варијација во големината на мускулните влакна. Овој тест е ретко индициран.
- Мускулната магнетна резонанца е чувствителна за откривање на оштетување на мускулите, дури и во благи случаи. Поради посебните модели на вклучување на мускулите на ФСХД, снимките може да помогнат да се разликува ФСХД од другите мускулни болести, насочувајќи го генетското тестирање.
Диференцијална дијагноза[уреди | уреди извор]
Диференцијалната дијагноза на ФСХД се мускулната дистрофија на екстремитетите (особено калпаинопатија ), миопатија на скапопулоронеална, митохондријална миопатија, Помпеова болест, и полимиозитис . Калпаинопатија и скапулоперонеална миопатија, како ФСХД, се манифестираат со крилја на лопатките. Одлики кои укажуваат на ФСХД се слабост на лицето, асиметрична слабост и недостаток на корист од лековите за имуносупресија. Одлики кои сугерираат алтернативна дијагноза се контрактури, респираторна инсуфициенција, слабост на мускулите кои го контролираат движењето на очите и слабост на јазикот или грлото(булпарна парализа) .
Третман[уреди | уреди извор]
До сега, за фациоскапулохумералната мускулна дистрофија не постои лек, но се користат лекови и третмани со цел менаџирање на некои симптоми и потенцијално забавување на прогресијата на болеста.Физикална терапија може да помогне во задржување на мускулнатасила ифункција, подобрување на мобилноста и превенција од паѓање. Нестероидни антиинфламаторни лекови често се препишуваат за подобрување на комфорот и мобилноста. Професионална и говорна терапија може да помогне во одржување на секојдневните животни вештини. Употребата на лубриканти може да помогне да се спречи сушење на очите кај лица чија мускулна слабост предизвикува делумно отворени очи за време на спиење. Масажа исто така може да помогне при непријатности поврзани со ФСХД. Ортозите за глужд/стапало можат да ја подобрат подвижноста и да спречат паѓање. Потпирачи за грб, корсети, појаси и специјални градници за овие лица можат да ја компензираат слабоста на мускулите во горниот и долниот дел на грбот. Хируршка фиксација на скапулата за ѕидот на градниот кош може да го подобри опсег на движење во рацете. Но и покрај ова досега ниту една интервенција не покажала значително забавување во прогресијата на болеста или дејстување врз слабоста во мускулите како и подобрување на силата.[25][27]
Скрининг и следење на компликациите[уреди | уреди извор]
Американската академија за неврологија препорачaла неколку медицински тестови за откривање на компликации.[28] Се препорачувало детален очен преглед за да се откријат евентуални абнормалности на мрежницата кај новодијагностицирани ФСХД; за оние со големи бришења на D4Z4, годишно се препорачува евалуација од специјалист.[29] Тест на слухот се препорачувало за индивидуи со ран почеток на ФСХД пред да тргнат на училиште, или за кој било друг поединец погоден од ФСХД со симптоми на губење на слухот. Тестирањето на белодробната функција се препорачувало кај новодијагностицираните за да се воспостави основната пулмонална функција и рекурентно за оние со симптоми или ризици на пулмонална инсуфициенција. Рутинскиот скрининг за срцеви заболувања, како што е електрокардиограм (ЕКГ) или ехокардиограм (ехо), се сметало за непотребен кај оние без симптоми на срцеви заболувања.[29][30]
Физикална терапија и вежби[уреди | уреди извор]
За аеробикот се смета дека го намалува хроничниот замор и ја забавуваат масната инфилтрација на мускулите кај ФСХД.[28] Американската акамедија за неврологија препорачувала луѓето со ФСХД да прават аеробни вежби, не многу интензивни за да го подобрат нивото на енергија, здравјето на мускулите и здравјето на коските.[31] Тренинзите кои вклучуваат поголем или умерен интензитет не му штетат на пациентите, но не се покажал и некој значаен ефект. При физикалната терапија се спроведува терапија за одредени пројавени симптоми бидејќи не постои стандардизиран протокол за ФСХД.[32] Анегдотските извештаи сугерираат дека соодветно применетата кинезиолошка лента може да ја намали болката.[28][28]
Протезите често се користат за решавање на мускулната слабост. Зацврстувањето на скапулата може да ja подобри функцијата на рамото, иако често се смета за неефективно или непрактично[33]. Ортозите на глужд-стапалото може да го подобрат одењето, рамнотежата и квалитетот на животот.[34]
Фармаколошки третман[уреди | уреди извор]
Ниеден фармацевтски препарат не е дефинитивно докажан како ефикасен за менување на текот на болеста.[27] Иако неколку фармацевтски препарати покажале подобрена мускулна маса во ограничени аспекти, тие не го подобриле квалитетот на животот и не се докажана препорака за користење против ФСХД.[27]
Операција[уреди | уреди извор]
Крилјата лопатки (искривување на лопатките) може да се фиксираат со помош на хируршка корекција. Скапуларната фиксација е ограничување и стабилизирање на положбата на скапулата(лопатките), ставајќи ја во поблиска поставеност на градниот кош и намалувајќи ја искривеноста. Најчесто се пријавува апсолутно ограничување на движењето на скапулата со фиксирање на скапулата на ребрата. Оваа процедура често вклучува поттикнување на коскено соединување, наречена артродеза, помеѓу скапулата и ребрата. Имињата за ова вклучуваат скапулоторакално соединување, скапуларно соединување и скапулодеза. Оваа процедура го зголемува активниот опсег на движење на раката, ја подобрува функцијата на раката, ја намалува болката и го подобрува изгледот.[35] Со други зборови, пациентот добива способност полека да ги крева рацете до 90+ степени, но не и цели 180 степени.[36][37] Американската академија наведува дека фиксацијата на скапулата може да се примени претпазливо на селектираните пациенти откако ќе се разгледаат ридобивките со негативните последици од операцијата и продолжената имобилизација.[38] Друга начин на операција на скапулата е скапулопексија. „Scapulo-“ се однесува на коската на скапулата, а „-pexy“ е изведен од грчкиот збор „да се врзува“. Некои верзии на скапулопексија го постигнуваат суштински истиот резултат како и скапулаторакалното соединување, но наместо да се поттикнува коскено соединување, скапулата е прицврстена на ребрата само со жица, тетивни графтови или друго. Некои верзии на скапулопексија не го ограничуваат целосно движењето на скапулата, примери како врзување на скапулата со ребрата, пршлените или друга скапула. Скапулопексијата се смета за поконзервативна од скапулоторакалното соединување, со намалено време на опоравување и помал ефект врз дишењето.[35] Сепак, тие исто така изгледаат поподложни на долгорочен неуспех. Друга форма на фиксација на скапулата, иако вообичаено не се прави во ФСХД, е трансфер на тетива, што вклучува хируршко преуредување на прицврстувањата на мускулите на коската.[38] Примерите вклучуваат префрлање на големиот пекторалис и процедурата Еден-Ланж.[39] Постојат и и разни други хируршки интервенции.[40] Златни импланти за горниот очен капак се користат за оние кои не можат да ги затворат очите. Испуштената долна усна е решена со пластична хирургија.[41] Одредени случаи на паѓање на стапалото може хируршки да се коригираат со трансфер на тетива, при што задниот тибијален мускул се пренаменува како тибијален преден мускул, верзија на ова се нарекува процедура Bridle.[42][43][44] Тешката сколиоза предизвикана од ФСХД може да се коригира со ’рбетно соединување; сепак, бидејќи сколиозата е компензаторна промена како одговор на мускулната слабост, корекција на усогласеноста на ’рбетниот столб може да резултира со дополнително нарушена мускулна функција.
- Scapular winging management
-
Kinesiology tape applied across the scapulas.
-
A cloth brace to hold the scapulas in retraction to reduce shoulder symptoms, such as collarbone pain.
-
Scapula-to-scapula scapulopexy, pre- and post-operation. The scapulas are tethered together into a retracted position with an Achilles tendon graft, which, in this case, rendered the rhomboid major muscles distinguishable.
Прогноза[уреди | уреди извор]
Генетиката делумно ја предвидува прогнозата.[27] Оние со големи повторувачки бришења на D4Z4 (со преостаната големина на низата за повторување на D4Z4 од 10-20 kbp, или 1-4 повторувања) имаат поголема веројатност да имаат тешка и рана болест, како и не-мускулни симптоми.[27] Оние кои имаат генетски мутации и на ФСХД 1 и ФСХД 2 имаат поголема веројатност да имаат потешка форма на болеста.[45] Исто така, забележано е дека манифестацијата на болеста е поблага кога е присутна истакната семејна историја, наспроти нова мутација.[се бара извор] Во некои големи семејства, 30% од оние со мутација не покажуваат симптоми, а 30% од оние со симптоми не напредувале надвор од слабоста на лицето и рамената.[се бара извор] Жените се со помала веројатност да бидат симптоматски, а ако се симптоматски имаат помалку сериозни манифестации.[се бара извор]
Останатите варијации во текот на болеста се припишуваат на непознати фактори на животната средина. Една студија покажала дека текот на болеста не се влошува со пушење тутун или консумирање алкохол, заеднички фактори на ризик за други болести.[46]
Бременост[уреди | уреди извор]
Резултатите од бременоста се генерално добри кај мајките со ФСХД; нема разлика во стапката на предвремено породување, стапката на спонтан абортус и исходите врз доенчињата.[47] Сепак, слабоста која се јавува како последица на болеста може да ја зголеми потребата за асистирано породување.[47]
Еден преглед покажал дека слабоста се влошува, без закрепнување, кај 12% од мајките со ФСХД за време на бременоста, иако тоа може да се должи на зголемување на телесната тежина или декондиционирање.[47]
Епидемиологија[уреди | уреди извор]
Преваленцата на ФСХД се движи од 1 во 8.333 до 1 во 15.000.[39] Холандија известува за преваленца од 1 на 8.333, откако се биле пресметани и недијагностицираните. Преваленцата во Соединетите Држави обично се смета за 1 на 15.000.[48]
Откако генетското тестирање станало возможно во 1992 година, било откриено дека просечната преваленца е околу 1 на 20.000, што претставува голем пораст во споредба со пред 1992 година.[5][49][50] Сепак, 1 од 20.000 не е релевантен податок , бидејќи многумина со ФСХД имаат благи симптоми и никогаш не се дијагностицирани, или тие се браќа и сестри на заболени лица и никогаш не барале конечна дијагноза.[50] Според други проценки распространетоста може да биде и 4 на 100 000.
Нема податоци дека расата и етничката припадност влијаат врз инциденцата или сериозноста на болеста.[51]
Иако наследувањето не покажало склоност кон пол, болеста се манифестира поретко кај жените, па дури и кога се манифестира кај жените, тие во просек се помалку сериозно погодени од заболените мажи.[48] Ова се објаснува преку естрогенот како заштитен фактор што го предизвикува несовпаѓање. Една студија покажала дека естрогенот ја намалува активноста на DUX4. Сепак, друга студија не открила поврзаност помеѓу тежината на болеста и изложеноста на естроген во текот на животот кај жените.[52] Истата студија покажала дека прогресијата на болеста не се разликува низ периодите на хормонални промени, како што се менарха, бременост и менопауза.[53]
Историја[уреди | уреди извор]
Првиот опис на лице со ФСХД во медицинската литература се појавил во извештајот од обдукцијата на Жан Крувеилје во 1852 г. Прво во 1874 година, потоа со почесто цитирана публикација во 1884 година, и повторно со слики во 1885 година, француските лекари Луј Ландузи и Џозеф Дежерин објавиле детали за болеста, препознавајќи ја како посебен клинички ентитет, и затоа ФСХД понекогаш се нарекува како болест Ландузи Дежерин. Во својот труд од 1886 година, Ландузи и Дежерин го привлекле вниманието споменувајќи дека четири генерации биле заболени со ФСХД во семејството кое тие го истражувале. Формалното клиничките одлики на ФСХД не биле дефинирани се до 1952 година кога било проучувано големо семејство во Јута. Почнувајќи од околу 1980 година, зголемениот интерес за ФСХД довел до зголемено разбирање на големата варијабилност во болеста и растечко разбирање на генетските и патофизиолошките комплексности. До крајот на 1990-тите, истражувачите конечно почнале да ги разбираат регионите на хромозомот 4 поврзани со ФСХД.
Од објавувањето на обединувачката теорија во 2010 година, истражувачите продолжиле да ги усовршуваат своите разбирања за DUX4 . Со зголемена доверба во работата, истражувачите го предложиле првиот консензуален поглед во 2014 година за патофизиологијата на болеста и потенцијалните пристапи кон терапевтската интервенција врз основа на тој модел.
Алтернативните и историските имиња за ФСХД се:
- фациоскапулохумерална болест
- фациохмероскапуларен[се бара извор]
- Ландузи Дежерин болест (или „синдром“ или „тип на мускулна дистрофија“ )
- синдром Ерб-Ландузи-Дежерин[се бара извор]
Хронологија на важни генетски истражувања поврзани со ФСХД[уреди | уреди извор]
| 1861 |  |
| 1884 | Ландузи и Дежерин опишувале форма на детска прогресивна мускулна атрофија со карактеристична зафатеност на мускулите на лицето и различна од псевдохипертрофичната (Душенова д-р) и спиналната мускулна атрофија кај возрасните.[54] |
Двајца браќа со ФСХД следени од Ландузи и Дежерин Фотографија на едениот брат на 21-годишна возраст. Десната лопатка е издолжена, надолу ротирана и странично поместена. Цртеж на другиот брат на 17 години. Видлива е лумбална хиперлордоза. Надлактицата и пекторалните мускули изгледаат атрофирани. | |
|---|---|
| 1886 | Ландузи и Дежерин ја опишуваат прогресивната мускулна атрофија од типот скапуло-хумерус.[55] |
| 1950 | Тајлер и Стивенс проучувале 1249 индивидуи кои биле во сродство со ФСХД наврајќајќи се и до нивните предци и опишале типичен модел наМенделово наследство со целосна пенетрација и многу променлива експресија. Воведен бил терминот фациоскапулохумерална дистрофија.[56] |
| 1982 | Падберг ги овозможил првите студии поврзани со одредување на генетски локус за ФСХД во неговата семинална теза „Фациоскапулохумерална болест." |
| 1987 | Целосната секвенца на генот Дистрофин (Душен MD) била одредена.[57] |
| 1991 | Генетското пореметување кое настанува кај ФСХД било поврзани со регионот (4q35) во близина на хромозомот 4.[58] |
| 1992 | Утврдено било дека ФСХД, и во фамилијарните и во de novo случаите е поврзан с0 рекомбинацијаta што ја намалува големината на 4q EcoR1 фрагмент до <28 kb (50–300 kb нормално). |
| 1993 | 4q EcoР1 Откриено е дека фрагментите содржат тандемски распоред на повеќе единици од 3,3 kb (D4Z4), а ФСХД е поврзана со присуство на < 11 D4Z4 единици.
Студија со седум семејства со ФСХД открила докази за генетска хетерогеност во ФСХД.[59] |
| 1994 | хетерохроматска структура на 4q35 била препознаена како фактор што може да влијае на изразувањето на болеста, можеби преку разновидност на ефектот на позиција.
Секвенционирањето на ДНК во единиците D4Z4 покажало дека тие содржат отворена рамка за читање што одговара на два домени хомеобокс, но истражувачите заклучиле дека D4Z4 најверојатно нема да кодира за функционален препис. |
| 1995 | Термините ФСХД1A и ФСХД1B биле воведени за да се опишат 4q-поврзани и не-4q-поврзани форми на болеста.[60] |
| 1996 | ФСХД регионот Ген1 (FRG1) бил откриен 100 kb проксимално до D4Z4.[61] |
| 1998 | Биле разгледувани монозиготни близнаци со многу различна клиничка експресија на ФСХД. |
| 1999 | Целосното секвенционирање на 4q35 D4Z4 единици открило промоторски регион сместен на 149 bp 5' од отворената рамка за читање за двата домени хомеобокси, што укажувало на ген кој кодира белковина од 391 аминокиселински белковина (подоцна коригиран на 424 аа |
| 2001 | Истражувачите ја процениле состојбата метилација (хетерохроматин повисоко метилиран од ехроматин) на ДНК во 4q35 D4Z4. Испитувањето на SmaI, MluI, SacII и EagI рестриктивен фрагмент од повеќе типови клетки, вклучително и скелетни мускули, не откриле докази за хипометилација во клетките од пациенти со ФСХД1 во однос на D4Z4 од незасегнати контролни клетки или во однос на хомологните места на D4Z4 на хромозом 10. Меѓутоа, во сите случаи, D4Z4 од спермата била хипометилиран во однос на D4Z4 од соматски ткива.[62] |
| 2002 | Полиморфен сегмент од 10 kb директно дистално од D4Z4 бил пронајден дека постои во две алелни форми, означени како 4qA и 4qB. ФСХД1 е поврзан само со алелот 4qA.[63]
Трите гени (FRG1, FRG2, ANT1) сместени во регионот само центромерот до D4Z4 на хромозомот 4 бил пронајден во изолирани мускулни клетки од индивидуи со ФСХД на нивоа 10 до 60 пати поголемо од нормалното, покажувајќи поврзаност помеѓу контракциите на D4Z4 и изменетата експресија на гените 4q35.[64] |
| 2003 | Понатамошното испитување на метилацијата на ДНК во различни фрагменти за ограничување 4q35 D4Z4 (BsaAI и FseI) покажало значајна хипометилација на двете места за индивидуи со ФСХД1, носители на гени кои не покажуваат ФСХД и индивидуи со фенотипски ФСХД во однос на незасегнатите контроли.[65] |
| 2004 | Контракцијата на регионот D4Z4 на алелот 4qB до <38 kb не предизвикува ФСХД.[66] |
| 2006 | Се покажало дека трансгенските глувци кои прекумерно изразуваат FRG1 развиваат тешка миопатија.[67] |
| 2007 | Откриле дека рамка за читање DUX4 била зачувана во геномот на приматите повеќе од 100 милиони години, што ја поддржало веројатноста дека таа го кодира потребната белковина.[68]
Истражувачите идентификувале DUX4 mRNA во примарните ФСХД миобласти и идентификувале во D4Z4-трансфектирани клетки белковина DUX4, чија прекумерна експресија предизвикува клеточна смрт. Пријавено било дека DUX4 мРНК и белковинската експресија се зголемуваат кај миобластите кај пациенти со ФСХД, во споредба со незасегнатите контроли. Стабилната DUX4 мРНК се транскрибира само од најоддалечената единица D4Z4, која користи интрон и полиаденилација сигнал обезбедени од страничниот pLAM регион. DUX4 белковината бил идентификуван како фактор на транскрипција, а доказите сугерирале дека прекумерната експресија на DUX4 е поврзана со зголемување на целниот спарена транскрипција на хомеодомен фактор 1(PITX1).[69] |
| 2009 | Термините ФСХД1 и ФСХД2 биле воведени за да се опишат генетските форми поврзани со бришење D4Z4 и не-D4Z4 , соодветно. Во типот 1, хипометилацијата е ограничена на краткиот 4q алел, додека типот 2 се одликува со хипометилација и на 4q и на двата 10q алели.[70]
Спојувањето и оделувањето кај (повеќето теломери) 4q D4Z4 DUX4 транскрипт кај примарни миобласти и фибробласти од пациенти со ФСХД било откриено дека резултира со генерирање на повеќе РНК, вклучувајќи мала некодирачка РНК како нов кандидат за патофизиологија на ФСХД.[71] |
| 2010 | Се создава генетски модел на ФСХД: контракциите на D4Z4 предизвикувале ФСХД само кога се во алел 4qA поради стабилизирање на транскриптот на DUX4 РНК, што овозможува изразување на DUX4. (See FSHD Society).
Д-р Френсис Колинс, кој го надгледувал првото секвенционирање на Човечкиот геном со Националните институти за здравје изјавил:
Даниел Перес, ко-основачот на здружението ФСХД, ги поздравил новите наоди велејќи:[се бара извор]
МДА изјавил:[се бара извор]
Еден од соавторите на извештајот, Силвер ван дер Маарел од Универзитетот во Лајден, изјавил;[се бара извор]
DUX4 бил пронајден активно транскрибиран во биопсиите на скелетните мускули и примарните миобласти. Клетките погодени од ФСХД произведуваат транскрипт со целосна должина, DUX4-fl, додека алтернативното спојување кај незасегнати индивидуи резултира со производство на пократок, 3'-скратен транскрипт (DUX4-s). Ниската севкупна експресија на двата транскрипта во мускулите се припишува на релативно високата експресија во мал број јадра (~ 1 во 1000). Повисоките нивоа на DUX4 изразување во човечки тестис (~ 100 пати повисоки од скелетните мускули) укажуваат на развојна улога на DUX4 во човечкиот развој. Повисоките нивоа на DUX4-s (наспроти DUX4-fl) се покажале дека корелираат со поголем степен на DUX-4 H3K9me3-метилација. |
| 2012 | Некои примери на ФСХД2 биле поврзани со мутации во генот SMCHD1 на хромозомот 18 и се воспоставило генетско/механистичко разделување на ФСХД1 и ФСХД2.
Преваленцата на D4Z4 бришења слични на ФСХД на попустливи алели била значително повисока од преваленцата на ФСХД кај општата популација, предизвикувајќи ги критериумите за молекуларна дијагноза на ФСХД.[72] Кога се изразувале во примарните миобласти, DUX4-fl делувал како транскрипциски активатор, создавајќи > 3-кратна промена во изразувањето на 710 гени.[73] Последователна студија со користење на поголем број примероци ја идентификувала експресијата на DUX4-fl во миогените клетки и мускулното ткиво од незасегнати роднини на пациенти со ФСХД, што не било доволно за да предизвика патологија, и дополнителните модификатори биле детерминанти на прогресијата на болеста.[74] Бил предложен механизам на DBE-T (препис на регулаторниот елемент D4Z4) што довело до дерепресија на гените 4q35. |
| 2013 | Се покажа дека мутациите на SMCHD1 ја зголемуваат сериозноста на болеста тип 1.
Трансгенските глувци кои носат низи D4Z4 од алел ФСХД1 (со 2,5 D4Z4 единици), иако немале очигледен фенотип на скелетните мускули сличен на ФСХД, било откриено дека рекапитулираат важни шеми на генетска експресија и епигенетски одлики на ФСХД.[75] |
| 2014 | DUX4-fl и низводно целните гени биле изразени во биопсиите на скелетните мускули и клетките добиени од биопсија на фетуси со низи D4Z4 слични на ФСХД, што покажало дека молекуларните маркери на ФСХД се веќе изразени за време на феталниот развој.[76]
Истражувачите „прегледуваат како придонесите од многу лаборатории во текот на многу години довеле до разбирање на фундаментално нов механизам на човечка болест“ и артикулираат како обединувачкиот генетски модел и последователните истражувања претставуваат „стожерна точка во истражувањето на ФСХД, транзиција на полето од откритието - ориентирани студии кон преведувачки студии насочени кон развој на терапии засновани на здрав модел на патофизиологија на болеста“. Тие го опишуваат консензусниот механизам на патофизиологијата за ФСХД како „неефикасна епигенетска репресија со посредство на повторување на макросателитната низа за повторување D4Z4 на хромозомот 4, што резултира со разновидната експресија на ретрогенот DUX4, кодирајќи фактор на транскрипција со двоен хомеобокс. во скелетните мускули." |
Фармацевтски развој[уреди | уреди извор]
Раните испитувања на лекови, пред да се открие патогенезата што го вклучува DUX4, биле нецелосни и главно неуспешни. Cohen, Justin; DeSimone, Alec; Lek, Monkol; Lek, Angela (October 2020). „Therapeutic Approaches in Facioscapulohumeral Muscular Dystrophy“. Trends in Molecular Medicine. 27 (2): 123–137. doi:10.1016/j.molmed.2020.09.008. PMC 8048701 Проверете ја вредноста |pmc= (help). PMID 33092966 Проверете ја вредноста |pmid= (help).</ref> Соединенијата биле тестирани со цел да се зголеми мускулната маса, да се намали воспалението. Следниве лекови не покажале ефикасност:
- Преднизон, стероид, базиран на неговите антиинфламаторни својства и терапевтски ефект кај мускулната дистрофија на Душен.[77]
- Орален албутерол, β2 агонист, врз основа на неговите анаболни својства. Иако ја подобрувал мускулната маса и силата кај оние со ФСХД, не ја подобрил глобалната сила или функција.[78][79][80] Интересно, подоцна се покажало дека β2 агонистите ја намалувале експресијата на DUX4.
- Дилтиазем, блокатор на калциумови канали, врз основа на анегдотски извештаи за употреба и теоријата дека дисрегулацијата на калциум одиграла улога во смртта на мускулните клетки.[81]
- MYO-029 (Stamulumab), антитело што го инхибира миостатинот, бил развие за да го промовира растот на мускулите. Миостатинот е белковина која го инхибира растот на мускулното ткиво.[82]
- ACE-083, TGF-β инхибитор, бил развиен за да го промогне растот на мускулите.[83]
Општество и култура[уреди | уреди извор]
Медиуми[уреди | уреди извор]
- Во серијата Мажот во високиот замок (The Man in the High Castle ) , Обергруппенфирер синот на Џон Смит, е со дијагностициран Ландузи-Дежерин синдром.[84]
- Во биографијата Стјуарт: Живот наназад (Stuart: A Life Backwards) , протагонистот бил погоден од мускулна дистрофија, веројатно ФСХД.[85]
Пациенти и истражувачки организации[уреди | уреди извор]
- Здружението ФСХД било основано во 1991 година од две лица со ФСХД, Даниел Перес и Стивен Јакобсен.[86][87] Здружението тврди дека се залагало за стандардизација на името на болеста фациоскапулохумерална мускулна дистрофија и нејзината кратенка ФСХД.[88] Исто така се залагало за истражувања за болеста и го ко-напишале Законот за MD-CARE од 2001 година, кој обезбедил федерално финансирање за сите мускулни дистрофии. Здружението ФСХД прерасна во најголемата светска организација која се залага за едукација на пациентите и научни и медицински истражувања. Еден значаен портпарол на здружението е Макс Адлер, актер во ТВ серијата Glee[89][90].
- Пријатели на ФСХД истражувања е непрофитна организација ориентирана кон истражување, основана во 2004 година од Тери и Рик Колела од Киркланд, Вашингтон, откако на нивниот син му беше дијагностицирана ФСХД.[91][92]
- Фондацијата за глобално истражување на ФСХД била основана во 2007 година од Бил Мос во Австралија, поранешен извршен директор на банката Мекквари кој заболел од ФСХД. Во моментов е управувано од ќерката на Мос. Фондацијата била прогласена за австралиска добротворна организација на годината за 2017 година и најголем финансиер на медицинските истражувања на ФСХД надвор од Соединетите држави од 2018 година.[93]
- ФСХД ЕВРОПА била основана во 2010 година.[94]
Забележителни случаи[уреди | уреди извор]
- Чип Вилсон е канадски милијардер и основач на Лулулемон. Тој ветил 100 милиони кандиски долари за истражување преку „Реши го ФСХД (Solve FSHD)“.
- Крис Карино е радио гласот на Бруклин Нетс. Тој ја основал „Фондацијата Крис Карино за ФСХД“, ориентирана кон финансирање на истражувања.
- Морган Хофман е американски професионален играч на голф. Ја основал фондацијата Морган Хофман, ориентирана кон финансирање на истражувања.
Истражувачки насоки[уреди | уреди извор]
Фармацевтски развој[уреди | уреди извор]
По постигнувањето на консензус за патофизиологијата на ФСХД во 2014 година, истражувачите предложиле четири пристапи за терапевтска интервенција:[96]
- подобрување на епигенетската репресија на D4Z4
- таргетирајте ја DUX4 mRNA, вклучително и менување на спојување или полиаденилација;
- блокирање на активноста на белковината DUX4
- инхибирање на процесот или процесите поттикнати од DUX4 што доведуваат до патологија.
Лекови со мали молекули
Повеќето лекови кои се користат во медицината се „лекови со мали молекули“, за разлика од биолошки медицински производи кои вклучуваат белковини, вакцини и нуклеински киселини. Лековите со мали молекули обично може да се земаат со голтање, наместо со инјектирање.
- Лосмапимод, селективен инхибитор на p38α/β митоген-активираните белковински кинази, бил идентификуван од Фулкрум терапевтика како моќен супресор на DUX4 in vitro.[97] Резултатите од клиничкото испитување фаза IIb, открини во јуни 2021 година, покажале статистички значајно забавување на влошувањето на мускулната функција. Се чекаат понатамошни судења.[98][99]
- Инхибицијата на казеин киназа 1 (CK1) е идентификувана од Фацио терапи, холандска фармацевтска компанија, за да ја потисне експресијата на DUX4 и е во претклинички развој. Фацио терапи тврди дека CK1 инхибицијата го остава соединувањето на миотубите недопрено, за разлика од BET инхибиторите, p38 MAPK инхибиторите и β2 агонистите.[100][101]
Генска терапија
Генската терапија е администрација на нуклеотиди за лекување на болеста. Повеќе видови на генска терапија се во претклиничка фаза на развој за третман на болеста.
- Антисенс терапијата користи антисенс олигонуклеотиди кои се врзуваат за DUX4 информациска РНК, поттикнувајќи ја неговата деградација и спречувајќи производство на DUX4 белковина. Фосфородијамидат морфолинос, олигонуклеотид модифициран за да ја зголеми неговата стабилност, се покажало дека селективно го намалува DUX4 и неговите ефекти; сепак, овие антисенс нуклеотиди имаат слаба способност да навлезат во мускулите.[39]
- МикроРНК (миРНК) насочени против DUX4, испорачани од вирусни вектори, покажале дека го намалуваат DUX4, штитат од патологија на мускулите и спречуваат губење на силата на стисокот кај моделите FSHD на глувци.[39] Arrowhead Pharmaceuticals развива терапевтски лек за интерференција на РНК против DUX4, наречен ARO-DUX4, и има намера да поднесе барање за регулаторно одобрение во третиот квартал од 2021 година за да започне клинички испитувања.[102][103][104]
- Се истражува уредувањето на геномот, трајната промена на генетскиот код. Една студија се обидела да го искористи CRISPER-Cas9 за да го исфрли сигналот за полиаденилација во моделите на лабораториски чинии, но не покажал терапевтски резултати.[105]
Потенцијални цели на лековите
- Инхибицијата на патеката на хијалуронска киселина (ХА) е потенцијална терапија. Една студија покажала дека многу молекуларни патологии поттикнати од DUX4 се посредувани од HA сигнализација, а инхибицијата на биосинтезата на HA со 4-метилумбелиферон ги спречила овие молекуларни патологии.[106]
- Се покажало дека инхибицијата на P300 ги инхибира штетните ефекти на DUX4[107]
- Се покажало дека BET инхибиторите ја намалуваат експресијата на DUX4.[108]
- Антиоксидансите потенцијално би можеле да ги намалат ефектите на ФСХД. Едно истражување покажало дека витаминот Ц, витаминот Е, цинк гликонат и селенометионин ја зголемуваат издржливоста и силата на квадрицепсите, но немаат значителна корист од перформансите на одење.[109] Се чека на понатамошно истражување.[25]
Мерки за исход[уреди | уреди извор]
Начините за мерење на болеста се важни за проучување на прогресијата на болеста и проценка на ефикасноста на лековите во клиничките испитувања.
- Квалитетот на животот може да се одредува преку прашалници, како што е ФСХД здравствениот индекс (FSHD Health Index).[39]
- Како болеста влијае на секојдневните активности може да се одредува преку прашалници, како што е скалата за вкупна попреченост изградена од FSHD-Rasch (FSHD-RODS)[110] или ФСХД композитна исходна мерка (FSHD-COM).[111]
- Миографијата со електрична импеданса се проучува како начин за мерење на оштетувањето на мускулите.[39]
- Магнетната резонанца на мускулите е корисна за проверка на сите мускули во телото. Мускулите може да се бодираат врз основа на степенот на инфилтрација на маснотии.[39]
Наводи[уреди | уреди извор]
- ↑ Tawil, R; Storvick, D; Feasby, TE; Weiffenbach, B; Griggs, RC (February 1993). „Extreme variability of expression in monozygotic twins with FSH muscular dystrophy“. Neurology. 43 (2): 345–8. doi:10.1212/wnl.43.2.345. PMID 8094896.
- ↑ Pandya, Shree; Eichinger, Kate. „Physical Therapy for Facioscapulohumeral Muscular Dystrophy“ (PDF). FSHD Society. Архивирано од изворникот (PDF) на 14 April 2020. Посетено на 14 April 2020.
- ↑ 3,00 3,01 3,02 3,03 3,04 3,05 3,06 3,07 3,08 3,09 3,10 3,11 3,12 3,13 3,14 Mul, Karlien; Lassche, Saskia; Voermans, Nicol C; Padberg, George W; Horlings, Corinne GC; van Engelen, Baziel GM (June 2016). „What's in a name? The clinical features of facioscapulohumeral muscular dystrophy“. Practical Neurology. 16 (3): 201–207. doi:10.1136/practneurol-2015-001353. PMID 26862222.
- ↑ Upadhyaya, Meena; Cooper, David, уред. (March 2004). FSHD Facioscapulohumeral Muscular Dystrophy : Clinical Medicine and Molecular Cell Biology. BIOS Scientific Publishers. ISBN 0203483677.
- ↑ 5,0 5,1 5,2 5,3 5,4 Padberg, George W. (2004). „Facioscapulohumeral muscular dystrophy: a clinician's experience“. Во Upadhyaya, Meena; Cooper, David N. (уред.). FSHD Facioscapulohumeral Muscular Dystrophy: Clinical Medicine and Molecular Cell Biology. BIOS Scientific Publishers. ISBN 1-85996-244-0.
- ↑ 6,0 6,1 6,2 Tawil, R; Van Der Maarel, SM (July 2006). „Facioscapulohumeral muscular dystrophy“ (PDF). Muscle & Nerve. 34 (1): 1–15. doi:10.1002/mus.20522. PMID 16508966.
- ↑ Wohlgemuth, M; de Swart, BJ; Kalf, JG; Joosten, FB; Van der Vliet, AM; Padberg, GW (27 June 2006). „Dysphagia in facioscapulohumeral muscular dystrophy“. Neurology. 66 (12): 1926–8. doi:10.1212/01.wnl.0000219760.76441.f8. PMID 16801662.
- ↑ Mul, K; Berggren, KN; Sills, MY; McCalley, A; van Engelen, BGM; Johnson, NE; Statland, JM (26 February 2019). „Effects of weakness of orofacial muscles on swallowing and communication in FSHD“. Neurology. 92 (9): e957–e963. doi:10.1212/WNL.0000000000007013. PMC 6404471. PMID 30804066.
- ↑ 9,0 9,1 „A giant of FSHD research shares his "regrets"“. FSHD Society. Way Back Machine. 30 September 2020. Архивирано од изворникот на 24 October 2020. Посетено на 11 March 2021.
Another striking aspect of FSHD is that muscles weakness seems to vary so much from patient to patient. Nonetheless, "there is a highly characteristic pattern of muscle weakness, otherwise we would never have been able to recognize FSHD as a specific disease," Padberg said. "Strong deltoid muscle does not occur in any other condition that involves weakness of scapular stabilizers. No other muscle disease with shoulder girdle involvement has this pattern." Unfortunately, "an explanation is beyond our grasp as we don't know how muscle are laid down" during the early stages of human gestation.
- ↑ 10,0 10,1 Tasca, G; Monforte, M; Iannaccone, E; Laschena, F; Ottaviani, P; Leoncini, E; Boccia, S; Galluzzi, G; Pelliccioni, M (2014). „Upper girdle imaging in facioscapulohumeral muscular dystrophy“. PLOS ONE. 9 (6): e100292. Bibcode:2014PLoSO...9j0292T. doi:10.1371/journal.pone.0100292. PMC 4059711. PMID 24932477.
- ↑ 11,0 11,1 Gerevini, S; Scarlato, M; Maggi, L; Cava, M; Caliendo, G; Pasanisi, B; Falini, A; Previtali, SC; Morandi, L (March 2016). „Muscle MRI findings in facioscapulohumeral muscular dystrophy“. European Radiology. 26 (3): 693–705. doi:10.1007/s00330-015-3890-1. PMID 26115655.
- ↑ 12,0 12,1 12,2 12,3 12,4 12,5 Goselink, RJM; Schreur, V; van Kernebeek, CR; Padberg, GW; van der Maarel, SM; van Engelen, BGM; Erasmus, CE; Theelen, T (2019). „Ophthalmological findings in facioscapulohumeral dystrophy“. Brain Communications. 1 (1): fcz023. doi:10.1093/braincomms/fcz023. PMC 7425335. PMID 32954265.
- ↑ Padberg, G. W.; Brouwer, O. F.; de Keizer, R. J. W.; Dijkman, G.; Wijmenga, C.; Grote, J. J.; Frants, R. R. (1995). „On the significance of retinal vascular disease and hearing loss in facioscapulohumeral muscular dystrophy“. Muscle & Nerve. 18 (S13): S73–S80. doi:10.1002/mus.880181314.
|hdl-access=бара|hdl=(help) - ↑ Trevisan, CP; Pastorello, E; Tomelleri, G; Vercelli, L; Bruno, C; Scapolan, S; Siciliano, G; Comacchio, F (December 2008). „Facioscapulohumeral muscular dystrophy: hearing loss and other atypical features of patients with large 4q35 deletions“. European Journal of Neurology. 15 (12): 1353–8. doi:10.1111/j.1468-1331.2008.02314.x. PMID 19049553.
- ↑ The name "D4Z4" is derived from an obsolete nomenclature system used for DNA segments of unknown significance during the human genome project: D for DNA, 4 for chromosome 4, Z indicates it is a repetitive sequence, and 4 is a serial number assigned based on the order of submission.
- ↑ Tupler, R; Berardinelli, A; Barbierato, L; Frants, R; Hewitt, JE; Lanzi, G; Maraschio, P; Tiepolo, L (May 1996). „Monosomy of distal 4q does not cause facioscapulohumeral muscular dystrophy“. Journal of Medical Genetics. 33 (5): 366–70. doi:10.1136/jmg.33.5.366. PMC 1050603. PMID 8733044.
- ↑ 17,0 17,1 Lim, KRQ; Nguyen, Q; Yokota, T (22 January 2020). „DUX4 Signalling in the Pathogenesis of Facioscapulohumeral Muscular Dystrophy“. International Journal of Molecular Sciences. 21 (3): 729. doi:10.3390/ijms21030729. PMC 7037115. PMID 31979100.
- ↑ 18,0 18,1 Bosnakovski, Darko; Shams, Ahmed S.; Yuan, Ce; da Silva, Meiricris T.; Ener, Elizabeth T.; Baumann, Cory W.; Lindsay, Angus J.; Verma, Mayank; Asakura, Atsushi (6 April 2020). „Transcriptional and cytopathological hallmarks of FSHD in chronic DUX4-expressing mice“. Journal of Clinical Investigation. 130 (5): 2465–2477. doi:10.1172/JCI133303. PMC 7190912. PMID 32250341.
- ↑ Mocciaro, Emanuele; Runfola, Valeria; Ghezzi, Paola; Pannese, Maria; Gabellini, Davide (26 November 2021). „DUX4 Role in Normal Physiology and in FSHD Muscular Dystrophy“. Cells. 10 (12): 3322. doi:10.3390/cells10123322. PMC 8699294 Проверете ја вредноста
|pmc=(help). PMID 34943834 Проверете ја вредноста|pmid=(help). - ↑ Lek, Angela; Zhang, Yuanfan; Woodman, Keryn G.; Huang, Shushu; DeSimone, Alec M.; Cohen, Justin; Ho, Vincent; Conner, James; Mead, Lillian (25 March 2020). „Applying genome-wide CRISPR-Cas9 screens for therapeutic discovery in facioscapulohumeral muscular dystrophy“. Science Translational Medicine. 12 (536): eaay0271. doi:10.1126/scitranslmed.aay0271. PMC 7304480. PMID 32213627.
- ↑ Mariot, Virginie; Joubert, Romain; Le Gall, Laura; Sidlauskaite, Eva; Hourde, Christophe; Duddy, William; Voit, Thomas; Bencze, Maximilien; Dumonceaux, Julie (22 October 2021). „RIPK3‐mediated cell death is involved in DUX4‐mediated toxicity in facioscapulohumeral dystrophy“. Journal of Cachexia, Sarcopenia and Muscle. 12 (6): 2079–2090. doi:10.1002/jcsm.12813. PMC 8718031 Проверете ја вредноста
|pmc=(help). PMID 34687171 Проверете ја вредноста|pmid=(help). - ↑ 22,0 22,1 Rijken, NH; van der Kooi, EL; Hendriks, JC; van Asseldonk, RJ; Padberg, GW; Geurts, AC; van Engelen, BG (December 2014). „Skeletal muscle imaging in facioscapulohumeral muscular dystrophy, pattern and asymmetry of individual muscle involvement“. Neuromuscular Disorders. 24 (12): 1087–96. doi:10.1016/j.nmd.2014.05.012. PMID 25176503.
- ↑ 23,0 23,1 23,2 Mair, D; Huegens-Penzel, M; Kress, W; Roth, C; Ferbert, A (2017). „Leg Muscle Involvement in Facioscapulohumeral Muscular Dystrophy: Comparison between Facioscapulohumeral Muscular Dystrophy Types 1 and 2“. European Neurology. 77 (1–2): 32–39. doi:10.1159/000452763. PMID 27855411.
- ↑ 24,0 24,1 24,2 Olsen, DB; Gideon, P; Jeppesen, TD; Vissing, J (November 2006). „Leg muscle involvement in facioscapulohumeral muscular dystrophy assessed by MRI“. Journal of Neurology. 253 (11): 1437–41. doi:10.1007/s00415-006-0230-z. PMID 16773269.
- ↑ 25,0 25,1 25,2 25,3 Wagner, Kathryn R. (December 2019). „Facioscapulohumeral Muscular Dystrophies“. CONTINUUM: Lifelong Learning in Neurology. 25 (6): 1662–1681. doi:10.1212/CON.0000000000000801. PMID 31794465.
- ↑ Strafella, Claudia; Caputo, Valerio; Galota, Rosaria Maria; Campoli, Giulia; Bax, Cristina; Colantoni, Luca; Minozzi, Giulietta; Orsini, Chiara; Politano, Luisa (1 December 2019). „The variability of SMCHD1 gene in FSHD patients: evidence of new mutations“. Human Molecular Genetics. 28 (23): 3912–3920. doi:10.1093/hmg/ddz239. PMC 6969370. PMID 31600781.
- ↑ 27,0 27,1 27,2 27,3 27,4 Tawil, R; Kissel, JT; Heatwole, C; Pandya, S; Gronseth, G; Benatar, M; Guideline Development, Dissemination, and Implementation Subcommittee of the American Academy of, Neurology.; Practice Issues Review Panel of the American Association of Neuromuscular & Electrodiagnostic, Medicine. (28 July 2015). „Evidence-based guideline summary: Evaluation, diagnosis, and management of facioscapulohumeral muscular dystrophy: Report of the Guideline Development, Dissemination, and Implementation Subcommittee of the American Academy of Neurology and the Practice Issues Review Panel of the American Association of Neuromuscular & Electrodiagnostic Medicine“. Neurology. 85 (4): 357–64. doi:10.1212/WNL.0000000000001783. PMC 4520817. PMID 26215877.CS1-одржување: повеќе имиња: список на автори (link)
- ↑ 28,0 28,1 28,2 28,3 Voet, N; Bleijenberg, G; Hendriks, J; de Groot, I; Padberg, G; van Engelen, B; Geurts, A (18 November 2014). „Both aerobic exercise and cognitive-behavioral therapy reduce chronic fatigue in FSHD: an RCT“. Neurology. 83 (21): 1914–22. doi:10.1212/WNL.0000000000001008. PMID 25339206. S2CID 25382403.
- ↑ 29,0 29,1 Tawil, R; Kissel, JT; Heatwole, C; Pandya, S; Gronseth, G; Benatar, M; Guideline Development, Dissemination, and Implementation Subcommittee of the American Academy of, Neurology.; Practice Issues Review Panel of the American Association of Neuromuscular & Electrodiagnostic, Medicine. (28 July 2015). „Evidence-based guideline summary: Evaluation, diagnosis, and management of facioscapulohumeral muscular dystrophy: Report of the Guideline Development, Dissemination, and Implementation Subcommittee of the American Academy of Neurology and the Practice Issues Review Panel of the American Association of Neuromuscular & Electrodiagnostic Medicine“. Neurology. 85 (4): 357–64. doi:10.1212/WNL.0000000000001783. PMC 4520817. PMID 26215877.CS1-одржување: повеќе имиња: список на автори (link)
- ↑ Tawil, R; van der Maarel, S; Padberg, GW; van Engelen, BG (July 2010). „171st ENMC international workshop: Standards of care and management of facioscapulohumeral muscular dystrophy“. Neuromuscular Disorders. 20 (7): 471–5. doi:10.1016/j.nmd.2010.04.007. PMID 20554202. S2CID 18448196.
- ↑ Tawil, R; Mah, JK; Baker, S; Wagner, KR; Ryan, MM; Sydney Workshop, Participants. (July 2016). „Clinical practice considerations in facioscapulohumeral muscular dystrophy Sydney, Australia, 21 September 2015“. Neuromuscular Disorders. 26 (7): 462–71. doi:10.1016/j.nmd.2016.03.007. PMID 27185458.
- ↑ Janssen, B; Voet, N; Geurts, A; van Engelen, B; Heerschap, A (3 May 2016). „Quantitative MRI reveals decelerated fatty infiltration in muscles of active FSHD patients“. Neurology. 86 (18): 1700–7. doi:10.1212/WNL.0000000000002640. PMID 27037227. S2CID 11617226.
- ↑ „Information for Patients and Families - The Richard Fields Center for FSH Dystrophy (FSHD) & Neuromuscular Research - University of Rochester Medical Center“. www.urmc.rochester.edu. Архивирано од изворникот на 14 November 2019. Посетено на 14 April 2020.
- ↑ Aprile, I; Bordieri, C; Gilardi, A; Lainieri Milazzo, M; Russo, G; De Santis, F; Frusciante, R; Iannaccone, E; Erra, C; Ricci, E; Padua, L (April 2013). „Balance and walking involvement in facioscapulohumeral dystrophy: a pilot study on the effects of custom lower limb orthoses“. European Journal of Physical and Rehabilitation Medicine. 49 (2): 169–78. PMID 23138679.
- ↑ 35,0 35,1 Orrell, Richard W; Copeland, Stephen; Rose, Michael R (20 January 2010). „Scapular fixation in muscular dystrophy“. Cochrane Database of Systematic Reviews. 2010 (1): CD003278. doi:10.1002/14651858.CD003278.pub2. PMC 7144827. PMID 20091543.
- ↑ Demirhan, Mehmet; Uysal, Ozgur; Atalar, Ata Can; Kilicoglu, Onder; Serdaroglu, Piraye (31 March 2009). „Scapulothoracic Arthrodesis in Facioscapulohumeral Dystrophy with Multifilament Cable“. Clinical Orthopaedics and Related Research. 467 (8): 2090–2097. doi:10.1007/s11999-009-0815-9. PMC 2706357. PMID 19333668.
- ↑ Eren, İlker; Birsel, Olgar; Öztop Çakmak, Özgür; Aslanger, Ayça; Gürsoy Özdemir, Yasemin; Eraslan, Serpil; Kayserili, Hülya; Oflazer, Piraye; Demirhan, Mehmet (May 2020). „A novel shoulder disability staging system for scapulothoracic arthrodesis in patients with facioscapulohumeral dystrophy“. Orthopaedics & Traumatology: Surgery & Research. 106 (4): 701–707. doi:10.1016/j.otsr.2020.03.002. PMID 32430271.
- ↑ 38,0 38,1 Upadhyaya, Meena; Cooper, David N. (2004). „Introduction and overview of FSHD“. Во Upadhyaya, Meena; Cooper, David N. (уред.). FSHD Facioscapulohumeral Muscular Dystrophy: Clinical Medicine and Molecular Cell Biology. BIOS Scientific Publishers. ISBN 1-85996-244-0.
- ↑ 39,0 39,1 39,2 39,3 39,4 39,5 39,6 Wagner, Kathryn R. (December 2019). „Facioscapulohumeral Muscular Dystrophies“. CONTINUUM: Lifelong Learning in Neurology. 25 (6): 1662–1681. doi:10.1212/CON.0000000000000801. PMID 31794465. S2CID 208531681.
- ↑ Sansone, V; Boynton, J; Palenski, C (June 1997). „Use of gold weights to correct lagophthalmos in neuromuscular disease“. Neurology. 48 (6): 1500–3. doi:10.1212/wnl.48.6.1500. hdl:2434/210652. PMID 9191754. S2CID 16251273.
- ↑ Matsumoto, M; Onoda, S; Uehara, H; Miura, Y; Katayama, Y; Kimata, Y (September 2016). „Correction of the Lower Lip With a Cartilage Graft and Lip Resection in Patients With Facioscapulohumeral Muscular Dystrophy“. The Journal of Craniofacial Surgery. 27 (6): 1427–9. doi:10.1097/SCS.0000000000002720. PMID 27300465. S2CID 16343571.
- ↑ Krishnamurthy, S; Ibrahim, M (January 2019). „Tendon Transfers in Foot Drop“. Indian Journal of Plastic Surgery. 52 (1): 100–108. doi:10.1055/s-0039-1688105. PMC 6664842. PMID 31456618.
- ↑ Chiodo, Chris; Bluman, Eric M. (2011-10-21). Tendon transfers in the foot and ankle. Saunders. стр. 421. ISBN 9781455709243. Посетено на 1 January 2020.
- ↑ Tawil, R; Mah, JK; Baker, S; Wagner, KR; Ryan, MM; Sydney Workshop, Participants. (July 2016). „Clinical practice considerations in facioscapulohumeral muscular dystrophy Sydney, Australia, 21 September 2015“. Neuromuscular Disorders. 26 (7): 462–71. doi:10.1016/j.nmd.2016.03.007. PMID 27185458.
- ↑ Sacconi, S; Lemmers, RJ; Balog, J; и др. (Oct 3, 2013). „The FSHD2 gene SMCHD1 is a modifier of disease severity in families affected by FSHD1“. The American Journal of Human Genetics. 93 (4): 744–751. doi:10.1016/j.ajhg.2013.08.004. PMC 3791262. PMID 24075187.
- ↑ Vincenten, Sanne C.C.; Mul, Karlien; Schreuder, Tim H.A.; Voermans, Nicol C.; Horlings, Corinne G.C.; van Engelen, Baziel G.M. (July 2021). „nnExploring the influence of smoking and alcohol consumption on clinical severity in patients with facioscapulohumeral muscular dystrophy“. Neuromuscular Disorders. 31 (9): 824–828. doi:10.1016/j.nmd.2021.07.005. ISSN 0960-8966. PMID 34407911 Проверете ја вредноста
|pmid=(help). - ↑ 47,0 47,1 47,2 Massey, JM; Gable, KL (1 February 2022). „Neuromuscular Disorders and Pregnancy“. Continuum (Minneapolis, Minn.). 28 (1): 55–71. doi:10.1212/CON.0000000000001069. PMID 35133311 Проверете ја вредноста
|pmid=(help). S2CID 246651681 Проверете ја вредноста|s2cid=(help). - ↑ 48,0 48,1 Statland, JM; Tawil, R (December 2016). „Facioscapulohumeral Muscular Dystrophy“. Continuum (Minneapolis, Minn.). 22 (6, Muscle and Neuromuscular Junction Disorders): 1916–1931. doi:10.1212/CON.0000000000000399. PMC 5898965. PMID 27922500.
- ↑ Deenen, JC; Horlings, CG; Verschuuren, JJ; Verbeek, AL; van Engelen, BG (2015). „The Epidemiology of Neuromuscular Disorders: A Comprehensive Overview of the Literature“. Journal of Neuromuscular Diseases. 2 (1): 73–85. doi:10.3233/JND-140045. PMID 28198707.
- ↑ 50,0 50,1 „Population-based incidence and prevalence of facioscapulohumeral dystrophy“. Neurology. 83 (12): 1056–9. 2014. doi:10.1212/WNL.0000000000000797. PMC 4166358. PMID 25122204.
- ↑ Statland, JM; Tawil, R (December 2016). „Facioscapulohumeral Muscular Dystrophy“. Continuum (Minneapolis, Minn.). 22 (6, Muscle and Neuromuscular Junction Disorders): 1916–1931. doi:10.1212/CON.0000000000000399. PMC 5898965. PMID 27922500.
- ↑ Teveroni, E; Pellegrino, M; Sacconi, S; Calandra, P; Cascino, I; Farioli-Vecchioli, S; Puma, A; Garibaldi, M; Morosetti, R; Tasca, G; Ricci, E; Trevisan, CP; Galluzzi, G; Pontecorvi, A; Crescenzi, M; Deidda, G; Moretti, F (3 April 2017). „Estrogens enhance myoblast differentiation in facioscapulohumeral muscular dystrophy by antagonizing DUX4 activity“. The Journal of Clinical Investigation. 127 (4): 1531–1545. doi:10.1172/JCI89401. PMC 5373881. PMID 28263188.
- ↑ Mul, K; Horlings, CGC; Voermans, NC; Schreuder, THA; van Engelen, BGM (June 2018). „Lifetime endogenous estrogen exposure and disease severity in female patients with facioscapulohumeral muscular dystrophy“. Neuromuscular Disorders. 28 (6): 508–511. doi:10.1016/j.nmd.2018.02.012. PMID 29655530.
- ↑ Landouzy; Dejerine (1884). „De la myopathie atrophique progressive (myopathie héréditaire, débutant dans l'enfance par la face, sans altération du système nerveux)“. Comptes Rendus de l'Académie des Sciences. 98: 53–55.
- ↑ Landouzy; Dejerine (1886). „Contribution à l'étude de la myopathie atrophique progressive (myopathie atrophique progressive, à type scapulo-huméral)“. Comptes Rendus des Séances de la Société de Biologie. 38: 478–481.
- ↑ Tyler, Frank; Stephens, FE (April 1950). „Studies in disorders of muscle. II Clinical manifestations and inheritance of facioscapulohumeral dystrophy in a large family“. Annals of Internal Medicine. 32 (4): 640–660. doi:10.7326/0003-4819-32-4-640. PMID 15411118.
- ↑ Koenig, M; Hoffman, EP; Bertelson, CJ; Monaco, AP; Feener, C; Kunkel, LM (Jul 31, 1987). „Complete cloning of the Duchenne muscular dystrophy (DMD) cDNA and preliminary genomic organization of the DMD gene in normal and affected individuals“. Cell. 50 (3): 509–517. doi:10.1016/0092-8674(87)90504-6. PMID 3607877. S2CID 35668717.
- ↑ Wijmenga, C; Padberg, GW; Moerer, P; и др. (April 1991). „Mapping of facioscapulohumeral muscular dystrophy gene to chromosome 4q35-qter by multipoint linkage analysis and in situ hybridization“. Genomics. 9 (4): 570–575. doi:10.1016/0888-7543(91)90348-I. PMID 2037288.
- ↑ Gilbert, JR; Stajich, JM; Wall, S; и др. (Aug 1993). „Evidence for heterogeneity in facioscapulohumeral muscular dystrophy (FSHD)“. American Journal of Human Genetics. 53 (2): 401–408. PMC 1682358. PMID 8328457.
- ↑ Gilbert, JR; Speer, MC; Stajich, J; и др. (Oct 1995). „Exclusion mapping of chromosomal regions which cross hybridise to FSHD1A associated markers in FSHD1B“. Journal of Medical Genetics. 32 (10): 770–773. doi:10.1136/jmg.32.10.770. PMC 1051697. PMID 8558552.
- ↑ van Deutekom, JC; Lemmers, RJ; Grewal, PK; и др. (May 1996). „Identification of the first gene (FRG1) from the FSHD region on human chromosome 4q35“. Human Molecular Genetics. 5 (5): 581–590. doi:10.1093/hmg/5.5.581. PMID 8733123.
- ↑ Tsien, F; Sun, B; Hopkins, NE; и др. (Nov 2001). „Methylation of the FSHD syndrome-linked subtelomeric repeat in normal and FSHD cell cultures and tissues“. Molecular Genetics and Metabolism. 74 (3): 322–331. doi:10.1006/mgme.2001.3219. PMID 11708861.
- ↑ Lemmers, RJ; de Kievit, P; Sandkuijl, L; и др. (Oct 2002). „Facioscapulohumeral muscular dystrophy is uniquely associated with one of the two variants of the 4q subtelomere“. Nature Genetics. 32 (2): 235–236. doi:10.1038/ng999. PMID 12355084. S2CID 28107557.
- ↑ Gabellini, D; Green, MR; Tupler, R (Aug 9, 2002). „Inappropriate gene activation in FSHD: a repressor complex binds a chromosomal repeat deleted in dystrophic muscle“. Cell. 110 (3): 339–348. doi:10.1016/S0092-8674(02)00826-7. PMID 12176321. S2CID 16396883.
- ↑ van Overveld, PG; Lemmers, RJ; Sandkuijl, LA; и др. (Dec 2003). „Hypomethylation of D4Z4 in 4q-linked and non-4q-linked facioscapulohumeral muscular dystrophy“. Nature Genetics. 35 (4): 315–317. doi:10.1038/ng1262. PMID 14634647. S2CID 28696708.
- ↑ Lemmers, RJ; Wohlgemuth, M; Frants, RR; Padberg, GW; Morava, E; van der Maarel, SM (Dec 2004). „Contractions of D4Z4 on 4qB subtelomeres do not cause facioscapulohumeral muscular dystrophy“. The American Journal of Human Genetics. 75 (6): 1124–1130. doi:10.1086/426035. PMC 1182148. PMID 15467981.
- ↑ Gabellini, D; D'Antona, G; Moggio, M; и др. (Feb 23, 2006). „Facioscapulohumeral muscular dystrophy in mice overexpressing FRG1“. Nature. 439 (7079): 973–977. Bibcode:2006Natur.439..973G. doi:10.1038/nature04422. PMID 16341202. S2CID 4427465.
- ↑ Clapp, J; Mitchell, LM; Bolland, DJ; и др. (Aug 2007). „Evolutionary conservation of a coding function for D4Z4, the tandem DNA repeat mutated in facioscapulohumeral muscular dystrophy“. The American Journal of Human Genetics. 81 (2): 264–279. doi:10.1086/519311. PMC 1950813. PMID 17668377.
- ↑ Dixit, M; Ansseau, E; Tassin, A; и др. (Nov 13, 2007). „DUX4, a candidate gene of facioscapulohumeral muscular dystrophy, encodes a transcriptional activator of PITX1“. Proceedings of the National Academy of Sciences of the USA. 104 (46): 18157–18162. Bibcode:2007PNAS..10418157D. doi:10.1073/pnas.0708659104. PMC 2084313. PMID 17984056.
- ↑ de Greef, JC; Lemmers, RJ; van Engelen, BG; и др. (Oct 2009). „Common epigenetic changes of D4Z4 in contraction-dependent and contraction-independent FSHD“. Human Mutation. 30 (10): 1449–1459. CiteSeerX 10.1.1.325.8388. doi:10.1002/humu.21091. PMID 19728363. S2CID 14517505.
- ↑ Snider, L; Asawachaicharn, A; Tyler, AE; и др. (Jul 1, 2009). „RNA transcripts, miRNA-sized fragments and proteins produced from D4Z4 units: new candidates for the pathophysiology of facioscapulohumeral dystrophy“. Human Molecular Genetics. 18 (13): 2414–2430. doi:10.1093/hmg/ddp180. PMC 2694690. PMID 19359275.
- ↑ Scionti, I; Greco, F; Ricci, G; и др. (Apr 6, 2012). „Large-scale population analysis challenges the current criteria for the molecular diagnosis of fascioscapulohumeral muscular dystrophy“. The American Journal of Human Genetics. 90 (4): 628–635. doi:10.1016/j.ajhg.2012.02.019. PMC 3322229. PMID 22482803.
- ↑ Geng, LN; Yao, Z; Snider, L; и др. (Jan 17, 2012). „DUX4 activates germline genes, retroelements, and immune mediators: implications for facioscapulohumeral dystrophy“. Developmental Cell. 22 (1): 38–51. doi:10.1016/j.devcel.2011.11.013. PMC 3264808. PMID 22209328.
- ↑ Jones, TI; Chen, JC; Rahimov, F; и др. (Oct 15, 2012). „Facioscapulohumeral muscular dystrophy family studies of DUX4 expression: evidence for disease modifiers and a quantitative model of pathogenesis“. Human Molecular Genetics. 21 (20): 4419–4430. doi:10.1093/hmg/dds284. PMC 3459465. PMID 22798623.
- ↑ Krom, YD; Thijssen, PE; Young, JM; и др. (Apr 2013). „Intrinsic Epigenetic Regulation of the D4Z4 Macrosatellite Repeat in a Transgenic Mouse Model for FSHD“. PLOS Genetics. 9 (4): e1003415. doi:10.1371/journal.pgen.1003415. PMC 3616921. PMID 23593020.
- ↑ Ferreboeuf, M; Mariot, V; Bessieres, B; и др. (Jan 1, 2014). „DUX4 and DUX4 downstream target genes are expressed in fetal FSHD muscles“. Human Molecular Genetics. 23 (1): 171–181. doi:10.1093/hmg/ddt409. PMID 23966205.
- ↑ Tawil, R; McDermott, MP; Pandya, S; King, W; Kissel, J; Mendell, JR; Griggs, RC (January 1997). „A pilot trial of prednisone in facioscapulohumeral muscular dystrophy. FSH-DY Group“. Neurology. 48 (1): 46–9. doi:10.1212/wnl.48.1.46. PMID 9008492. S2CID 729275.
- ↑ Kissel, JT; McDermott, MP; Natarajan, R; Mendell, JR; Pandya, S; King, WM; Griggs, RC; Tawil, R (May 1998). „Pilot trial of albuterol in facioscapulohumeral muscular dystrophy. FSH-DY Group“. Neurology. 50 (5): 1402–6. doi:10.1212/wnl.50.5.1402. PMID 9595995. S2CID 24848310.
- ↑ Kissel, JT; McDermott, MP; Mendell, JR; King, WM; Pandya, S; Griggs, RC; Tawil, R; FSH-DY, Group. (23 October 2001). „Randomized, double-blind, placebo-controlled trial of albuterol in facioscapulohumeral dystrophy“. Neurology. 57 (8): 1434–40. doi:10.1212/wnl.57.8.1434. PMID 11673585. S2CID 28093111.
- ↑ van der Kooi, EL; Vogels, OJ; van Asseldonk, RJ; Lindeman, E; Hendriks, JC; Wohlgemuth, M; van der Maarel, SM; Padberg, GW (24 August 2004). „Strength training and albuterol in facioscapulohumeral muscular dystrophy“. Neurology. 63 (4): 702–8. doi:10.1212/01.wnl.0000134660.30793.1f. PMID 15326246. S2CID 22778327.
- ↑ Elsheikh, BH; Bollman, E; Peruggia, M; King, W; Galloway, G; Kissel, JT (24 April 2007). „Pilot trial of diltiazem in facioscapulohumeral muscular dystrophy“. Neurology. 68 (17): 1428–9. doi:10.1212/01.wnl.0000264017.08217.39. PMID 17452589. S2CID 361422.
- ↑ Wyeth Initiates Clinical Trial with Investigational Muscular Dystrophy Therapy MYO-029
- ↑ Malcolm, Emily (18 June 2019). „ACE-083“. Muscular Dystrophy News. Посетено на 19 December 2019.
- ↑ Landouzy-Dejerine syndrome, whonamedit.com, date accessed March 11, 2007
- ↑ Cohen, Justin; DeSimone, Alec; Lek, Monkol; Lek, Angela (October 2020). „Therapeutic Approaches in Facioscapulohumeral Muscular Dystrophy“. Trends in Molecular Medicine. 27 (2): 123–137. doi:10.1016/j.molmed.2020.09.008. PMC 8048701 Проверете ја вредноста
|pmc=(help). PMID 33092966 Проверете ја вредноста|pmid=(help). - ↑ „Our History“. FSHD Society. Архивирано од изворникот на 27 February 2022.
- ↑ Bartlett, Jessica (19 August 2014). Boston Business Journal https://web.archive.org/web/20220412220102/https://www.bizjournals.com/boston/blog/health-care/2014/08/dan-perez-living-with-and-fighting-against-a.html. Архивирано од изворникот на 12 April 2022. Посетено на 12 April 2022. Отсутно или празно
|title=(help) - ↑ „FSHD Society“. NORD (National Organization for Rare Disorders). Архивирано од изворникот на 2022-05-13. Посетено на 2023-01-28.
- ↑ „This Is FSHD“. HuffPost (англиски). 16 July 2014. Архивирано од изворникот на 2 August 2019. Посетено на 12 April 2022.
- ↑ „About Us :: Friends of FSH Research“. Friends of FSH Research. Архивирано од изворникот на 17 February 2020. Посетено на 9 April 2022.
- ↑ Krummey, Catherine (30 March 2017). „Kirkland couple raises $3.2 million for FSH muscular dystrophy research“. Kirkland Reporter. Архивирано од изворникот на 16 June 2017. Посетено на 9 April 2022.
- ↑ AMRA Medical (13 Oct 2021). „AMRA Medical's Whole-body MRI Analysis Used in FSHD Clinical Trial Research Network Study for Biomarker Development“. Cision PR Newswire (англиски). Архивирано од изворникот на 1 November 2021. Посетено на 9 April 2022.
- ↑ Tasker, Sarah-Jane (26 May 2018). „Bill Moss, the single-minded biotech and a search for a cure“. The Australian. Посетено на 9 April 2022.
- ↑ Voermans, NC; Vriens-Munoz Bravo, M; Padberg, GW; Laforêt, P; FSHD European Trial Network workshop study, group. (September 2021). „1st FSHD European Trial Network workshop:Working towards trial readiness across Europe“. Neuromuscular Disorders. 31 (9): 907–918. doi:10.1016/j.nmd.2021.07.013. PMID 34404575 Проверете ја вредноста
|pmid=(help). S2CID 236217036 Проверете ја вредноста|s2cid=(help). - ↑ Rickard, Amanda; Petek, Lisa; Miller, Daniel (August 5, 2015). „Endogenous DUX4 expression in FSHD myotubes is sufficient to cause cell death and disrupts RNA splicing and cell migration pathways“. Hum. Mol. Genet. 24 (20): 5901–14. doi:10.1093/hmg/ddv315. PMC 4581613. PMID 26246499.
- ↑ Tawil, Rabi; van der Maarel, SM; Tapscott, SJ (10 June 2014). „Facioscapulohumeral dystrophy: the path to consensus on pathophysiology“. Skeletal Muscle. 4 (1): 12. doi:10.1186/2044-5040-4-12. PMC 4060068. PMID 24940479.Tawil, Rabi; van der Maarel, SM; Tapscott, SJ (10 June 2014).
- ↑ „ReDUX4 trial result exceeds expectations“. FSHD Society. Wayback Machine. 2021-06-24. Архивирано од изворникот на 26 June 2021. Посетено на 26 June 2021.
- ↑ „Efficacy and Safety of Losmapimod in Subjects With Facioscapulohumeral Muscular Dystrophy (FSHD)“. ClinicalTrials.gov (англиски). United States National Library of Medicine. Посетено на 12 August 2019.
- ↑ „Fulcrum Therapeutics Acquires Global Rights to Losmapimod, a Potential Disease-Modifying Therapy for Facioscapulohumeral Muscular Dystrophy“. BioSpace. Посетено на 12 August 2019.
- ↑ „Facio to present at the World Muscle Society Congress“. Facio Therapies. 30 September 2019. Архивирано од изворникот на 2019-11-09. Посетено на 9 November 2019.
- ↑ „Facio reveals novel mechanism targeting the cause of FSHD“. Facio Therapies. 24 June 2019. Архивирано од изворникот на 2019-11-09. Посетено на 9 November 2019.
- ↑ „Arrowhead Pharmaceuticals announces FSHD drug candidate“. FSHD Society. 15 April 2021. Посетено на 15 April 2021.
- ↑ „Arrowhead Announces ARO-DUX4 as First Muscle Targeted RNAi Candidate Using TRiMTM Platform“. Businesswire (англиски). 15 April 2021. Посетено на 15 April 2021.
- ↑ Saad, Nizar Y.; Al-Kharsan, Mustafa; Garwick-Coppens, Sara E.; Chermahini, Gholamhossein Amini; Harper, Madison A.; Palo, Andrew; Boudreau, Ryan L.; Harper, Scott Q. (December 2021). „Human miRNA miR-675 inhibits DUX4 expression and may be exploited as a potential treatment for Facioscapulohumeral muscular dystrophy“. Nature Communications. 12 (1): 7128. Bibcode:2021NatCo..12.7128S. doi:10.1038/s41467-021-27430-1. PMC 8654987 Проверете ја вредноста
|pmc=(help). PMID 34880230 Проверете ја вредноста|pmid=(help). - ↑ Joubert, R; Mariot, V; Charpentier, M; Concordet, JP; Dumonceaux, J (23 December 2020). „Gene Editing Targeting the DUX4 Polyadenylation Signal: A Therapy for FSHD?“. Journal of Personalized Medicine. 11 (1): 7. doi:10.3390/jpm11010007. PMC 7822190 Проверете ја вредноста
|pmc=(help). PMID 33374516 Проверете ја вредноста|pmid=(help). - ↑ DeSimone, Alec M.; Leszyk, John; Wagner, Kathryn; Emerson, Charles P. (11 December 2019). „Identification of the hyaluronic acid pathway as a therapeutic target for facioscapulohumeral muscular dystrophy“. Science Advances. 5 (12): eaaw7099. Bibcode:2019SciA....5.7099D. doi:10.1126/sciadv.aaw7099. PMC 6905861. PMID 31844661.
- ↑ Bosnakovski, D; da Silva, MT; Sunny, ST; Ener, ET; Toso, EA; Yuan, C; Cui, Z; Walters, MA; Jadhav, A; Kyba, M (September 2019). „A novel P300 inhibitor reverses DUX4-mediated global histone H3 hyperacetylation, target gene expression, and cell death“. Science Advances. 5 (9): eaaw7781. Bibcode:2019SciA....5.7781B. doi:10.1126/sciadv.aaw7781. PMC 6739093. PMID 31535023.
- ↑ Campbell, AE; Oliva, J; Yates, MP; Zhong, JW; Shadle, SC; Snider, L; Singh, N; Tai, S; Hiramuki, Y; Tawil, R; van der Maarel, SM; Tapscott, SJ; Sverdrup, FM (4 September 2017). „BET bromodomain inhibitors and agonists of the beta-2 adrenergic receptor identified in screens for compounds that inhibit DUX4 expression in FSHD muscle cells“. Skeletal Muscle. 7 (1): 16. doi:10.1186/s13395-017-0134-x. PMC 5584331. PMID 28870238.
- ↑ Passerieux, E; Hayot, M; Jaussent, A; Carnac, G; Gouzi, F; Pillard, F; Picot, MC; Böcker, K; Hugon, G; Pincemail, J; Defraigne, JO; Verrips, T; Mercier, J; Laoudj-Chenivesse, D (April 2015). „Effects of vitamin C, vitamin E, zinc gluconate, and selenomethionine supplementation on muscle function and oxidative stress biomarkers in patients with facioscapulohumeral dystrophy: a double-blind randomized controlled clinical trial“ (PDF). Free Radical Biology & Medicine. 81: 158–69. doi:10.1016/j.freeradbiomed.2014.09.014. PMID 25246239. S2CID 10971952.
- ↑ Mul, K; Hamadeh, T; Horlings, CGC; Tawil, R; Statland, JM; Sacconi, S; Corbett, AJ; Voermans, NC; Faber, CG; van Engelen, BGM; Merkies, ISJ (10 April 2021). „The FacioScapuloHumeral muscular Dystrophy Rasch-built Overall Disability Scale (FSHD-RODS)“. European Journal of Neurology. 28 (7): 2339–2348. doi:10.1111/ene.14863. PMC 8251612 Проверете ја вредноста
|pmc=(help). PMID 33838063 Проверете ја вредноста|pmid=(help). - ↑ Eichinger, K; Heatwole, C; Iyadurai, S; King, W; Baker, L; Heininger, S; Bartlett, A; Dilek, N; Martens, WB; Mcdermott, M; Kissel, JT; Tawil, R; Statland, JM (2018-01-30). „Facioscapulohumeral muscular dystrophy functional composite outcome measure“. Muscle & Nerve. 58: 72–78. doi:10.1002/mus.26088. PMC 6066464. PMID 29381807.
Надворешни врски[уреди | уреди извор]
| Класификација | |
|---|---|
| Надворешни извори |