Осмотски притисок

Осмотски притисок ― минималниот притисокот што треба да се нанесе врз растворот за да се спречи внатрешен тек на чистиот растворувач низ полупропустлива мембрана.[1] Исто така, се дефинира како мерка за тенденцијата на растворот да внесува чист растворувач со осмоза. Потенцијалниот осмотски притисок е максималниот осмотски притисок што би можел да се развие во растворот доколку тој се одвои од неговиот чист растворувач со полупропустлива мембрана.
Осмозата се јавува кога два раствори кои содржат различни концентрации на растворена супстанција се одделени со избрано пропустлива мембрана. Молекулите на растворувачот преференцијално минуваат низ мембраната од растворот со ниска концентрација до растворот со поголема концентрација на растворена супстанција. Преносот на молекулите на растворувачите ќе продолжи додека не се постигне рамнотежа.[1][2]
Примени[уреди | уреди извор]
Мерењето на осмотскиот притисок може да се користи за определување на молекуларни тежини.
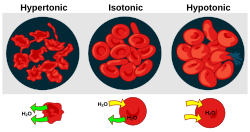
Осмотскиот притисок е важен фактор што влијае на клетките. Осморегулација е хомеостазен механизам на организмот да постигне рамнотежа во осмотскиот притисок.
- Хипертоничност е присуство на раствор што предизвикува намалување на клетките.
- Хипотоничност е присуство на раствор кој предизвикува отекување на клетките.
- Изотоничност е присуство на раствор кој не предизвикува промена во волуменот на клетката.
Кога клетката е во хипотонична средина, внатрешноста на клетката акумулира вода, водата тече низ клеточната мембрана во клетката, предизвикувајќи нејзино проширување. Во растителна клетка, клеточниот ѕид го ограничува ширењето, што резултира со притисок врз клеточниот ѕид одвнатре наречен тургорски притисок. Тургорскиот притисок им овозможува на тревни растенија да стојат исправено. Тоа е исто така одлучувачки фактор за тоа како растенијата ја регулираат отворот на нивните стоми. Во животинските клетки прекумерниот осмотски притисок може да резултира со цитолиза.
Осмотскиот притисок е основата на филтрирањето („обратна осмоза“), постапка која најчесто се користи во прочистување на водата. Водата што треба да се прочисти се става во комора и се става под притисок поголем од осмотскиот притисок што го врши водата и растворените материи растворени во неа. Дел од комората се отвора кон диференцијално пропустлива мембрана која ги пропушта молекулите на водата, но не и честичките на растворената супстанција. Осмотскиот притисок на океанската вода е околу 27 атм. Обратна осмоза отсолува свежа вода од морска вода.
Морсова релација[уреди | уреди извор]
Осмотскиот притисок Π на идеален раствор може да се пресмета според Морсовата релација (наречена по Хармон Нортроп Морс):[3]
- ,
каде
- i е бездимензионален Вант Хофов фактор
- M е моларноста
- R=0.0821 L atm K-1 mol-1 е гасна константа
- T е термодинамичка температура
Поврзано[уреди | уреди извор]
Наводи[уреди | уреди извор]
- ↑ 1,0 1,1 Voet, Donald; Judith Aadil; Charlotte W. Pratt (2001). Fundamentals of Biochemistry (Rev.. изд.). Њујорк: Wiley. стр. 30. ISBN 978-0-471-41759-0.
- ↑ Atkins, Peter W.; de Paula, Julio (2010). „Section 5.5 (e)“. Physical Chemistry (9. изд.). Oxford University Press. ISBN 978-0-19-954337-3.
- ↑ Mansoor M. Amiji, Beverly J. Sandmann (2002). Applied Physical Pharmacy. McGraw-Hill Professional. стр. 54–57. ISBN 0071350764.
Надворешни врски[уреди | уреди извор]
| Оваа статија од областа на биологијата е никулец. Можете да помогнете со тоа што ќе ја проширите. |

