Ацил хлорид

Во органската хемија, ацил хлорид (познат и како киселински хлорид) е органско соединение кое претставува реакционен дериват на карбоксилна киселина. Како дел од својата молекулска структура, секој ацил хлорид поседува реакциона функционална група од типот -CO-Cl. Ацил хлоридот ја има општата формула RCOCl, каде R е органска радикална група.
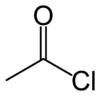
ацетил хлорид
Ацил хлоридите се подгрупа на ацил халидите и подлежат на повеќето реакции во кои стапуваат ацил халидите. Специфичен пример на ацил хлорид е ацетил хлорид (МСЧПХ име: етаноил хлорид) CH3COCl.
Хемиски реакции[уреди | уреди извор]
Ацил хлоридите се многу реактивни и не настануваат во природата. Тие се корисни реагенси за лабораториска синтеза на естери и амиди. Присуството на хлорот до карбонилниот јаглерод ги прави добри електрофили, бидејќи и кислородот и хлорот се силни електрон акцептори, притоа давајќи му на јаглеродот голем делумен позитивен полнеж. Ова значи дека дури и слаб нуклеофил може да го нападне јаглеродот. Бидејќи хлоридниот јон е добра заминувачка група, тој брзо ќе биде заменет со нуклеофилот. Ацил хлоридите можат да се користат за подготовка на било кој дериват на карбоксилните киселини: ацил анхидрид, естер или амид, преку хемиска реакција на ацил хлоридите со: сол на карбоксилна киселина, алкохол или амин, соодветно. Ацил хлоридите исто така ќе реагираат со вода или Џилманов реагенс (литиум диорганобакарно соединение). Во повеќето од овие реакции, HCl (хлороводородна киселина) се образува како спореден производ.
Со јаглеродни нуклеофили, како што се Грињаровите реагенси, ацил хлоридите обично прво реагираат со кетонот, а потоа со вториот еквивалент на терциерниот алкохол. Важен исклучок е реакцијата на ацил халидите со одредени органокадмиумски реагенси кои ја запираат кетонската фаза. Ацил хлоридите на ароматичните киселини се обично помалку реактивни отколку тие на алкил киселините и како резултат на ова се потребни поригорозни услови за да настапи реакција.
Несакани последици[уреди | уреди извор]
Бидејќи ацил хлоридите се токсични, треба да се преземат посебни мерки додека се ракува со нив. Тие делуваат иритирачки на очите и нивните пареи се многу штетни.
Синтеза[уреди | уреди извор]
Често ацил хлоридите се подготвуваат со реакција на карбоксилна киселина со тионил хлорид:
- R-COOH + SOCl2 → R-COCl + SO2 + HCl
Ацил хлоридите може исто така што се подготват со фосфор хлорид реагенси како што се фосфор трихлорид или фосфор пентахлорид:
- R-COOH + PCl5 → R-COCl + POCl3 + HCl
|
