Ензим за расцепување на страничниот синџир на холестерол
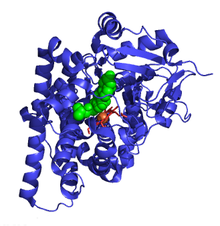
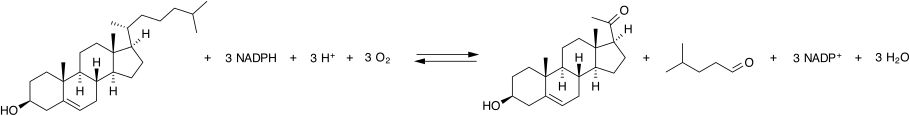
Ензимот за расцепување со страничен синџир на холестерол најчесто се нарекува P450scc, каде што „scc“ е акроним за расцепување со страничен синџир. P450scc е митохондријален ензим кој ја катализира конверзијата на холестеролот во прегненолон. Ова е прва реакција во процесот на стероидогенеза во сите ткива на цицачи кои се специјализирани за производство на различни стероидни хормони.[1]
|
P450scc е член на суперфамилијата на ензими на цитохром P450 (фамилија 11, подфамилија А, полипептид 1) и е кодирана од генот CYP11A1.[2]
Номенклатура[уреди | уреди извор]
-
Прегненолон
Системското име на оваа класа на ензими е холестерол, редуцирана надбубрежна-феродоксин: кислородна оксидоредуктаза (расцепување на страничен синџир). Други имиња вклучуваат:
|
| Ензим за расцепување на страничниот синџир на холестерол | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Назнаки | |||||||||
| EC-број | 1.14.15.6 | ||||||||
| Бази на податоци | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA entry | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | KEGG entry | ||||||||
| MetaCyc | metabolic pathway | ||||||||
| PRIAM | profile | ||||||||
| PDB структури | RCSB PDB PDBj PDBe PDBsum | ||||||||
| |||||||||
Ткиво и интрацелуларна локализација[уреди | уреди извор]
Највисокото ниво на системот за расцепување на страничниот синџир на холестерол се наоѓа во кората на надбубрежните жлезди и жолтото тело.[1] Системот е исто така изразен на високи нивоа во стероидогените тека клетки во јајниците и Лајдиговите клетки во тестисот.[1] За време на бременоста, плацентата исто така изразува значајни нивоа на овој ензимски систем.[3] P450scc е исто така присутен на многу пониски нивоа во неколку други видови ткива, вклучувајќи го и мозокот.[4] Во кората на надбубрежните жлезди, концентрацијата на адренодоксин е слична на онаа на P450scc, но адренодоксин редуктазата е изразена на пониски нивоа.[5]
Студиите за имунофлуоресценција со користење на специфични антитела против ензимите на системот P450scc покажале дека протеините се наоѓаат исклучиво во митохондриите.[6][7] P450scc е поврзан со внатрешната митохондријална мембрана, свртена кон внатрешноста (матрица).[8][9] Адренодоксин и адренодоксин редуктаза се растворливи периферни мембрански протеини сместени во внатрешноста на митохондријалната матрица кои се чини дека се поврзуваат едни со други првенствено преку електростатските интеракции.[10]
Механизам на дејство[уреди | уреди извор]
P450scc ја катализира конверзијата на холестеролот во прегненолон во три реакции на монооксигеназа. Тие вклучуваат 2 хидроксилации на страничниот синџир на холестерол, кои генерираат, прво, 22R-хидроксихолестерол, а потоа 20 алфа,22R-дихидроксихолестерол. Последниот чекор ја раскинува врската помеѓу јаглеродот т 20 и 22, што резултира со производство на прегненолон и изокапроичен алдехид.
Секој чекор на монооксигеназа бара 2 електрони ( редукциони еквиваленти ). Почетниот извор на електроните е NADPH.[11] Електроните се пренесуваат од NADPH до P450scc преку два протеини за пренос на електрони: адренодоксин редуктаза[12] и адренодоксин.[13][14] Сите три протеини заедно го сочинуваат комплексот на расцепување на страничниот синџир на холестерол.
Вклучувањето на три протеини во реакцијата на расцепување на страничниот синџир на холестерол го покренува прашањето дали трите протеини функционираат како троен комплекс како редуктаза:адренодоксин:Р450. И спектроскопските студии за врзување на адренодоксин за P450scc и кинетичките студии во присуство на различни концентрации на адренодоксин редуктаза покажале дека редуктазата се натпреварува со P450scc за врзување со адренодоксин. Овие резултати покажале дека формирањето на функционален тринарен комплекс не е возможно.[13] Од овие студии, било заклучено дека местата за врзување на адренодоксинот за неговата редуктаза и за P450 се преклопуваат и, како последица на тоа, адренодоксинот функционира како мобилен електронски шатл помеѓу редуктазата и P450.[13] Овие заклучоци се потврдени со структурна анализа на адренодоксин и комплексот P450.[15]
Процесот на пренос на електрони од NADPH до P450scc не е цврсто поврзан; односно, за време на преносот на електрони од адренодоксин редуктаза преку адренодоксин до P450scc, одреден дел од електроните истекуваат надвор од синџирот и реагираат со O2, генерирајќи супероксидни радикали.[16] Стероидогените клетки вклучуваат разновидна низа на антиоксидантни системи за да се справат со радикалите генерирани од стероидогените ензими.[17]
Регулатива[уреди | уреди извор]
Во секоја стероидогена клетка, изразувањето на протеините на системот P450scc е регулирано од трофичниот хормонски систем специфичен за типот на клетката.[1] Во клетките на надбубрежниот кортекс од zona fasciculata, експресијата на mRNA кои ги кодираат сите три протеини P450scc е индуцирана од кортикотропин (ACTH).[7][18] Трофичните хормони ја зголемуваат генска експресијата CYP11A1 преку факторите на транскрипција како што е стероидогениот фактор 1 (SF-1), преку α изоформата на активирачкиот протеин 2 (AP-2) кај човекот и многу други.[18][19] Производството на овој ензим е инхибирано особено од нуклеарниот рецептор DAX-1.[18]
P450scc е секогаш активен, но неговата активност е ограничена од снабдувањето со холестерол во внатрешната мембрана. Снабдувањето со холестерол до оваа мембрана (од надворешната митохондријална мембрана ) се смета за вистински чекор што ја ограничува стапката во производството на стероиди. Овој чекор е посредуван првенствено од стероидогениот акутен регулаторен протеин (StAR или STARD1). По стимулација на клетката да направи стероид, количината на StAR достапна за преноц на холестерол во внатрешната мембрана го ограничува колку брзо може да оди реакцијата (акутната фаза). Со продолжена (хронична) стимулација, се смета дека снабдувањето со холестерол повеќе не станува проблем и дека капацитетот на системот да произведува стероиди (т.е. нивото на P450scc во митохондриите) сега е поважен.
Кортикотропин (ACTH) е хормон кој се ослободува од предниот дел на хипофизата како одговор на стресни ситуации. Студијата за стероидогениот капацитет на надбубрежниот кортекс кај доенчиња со акутна респираторна болест покажало дека навистина за време на болеста постои специфично зголемување на стероидогениот капацитет за синтеза на глукокортикоидниот кортизол, но не и за минералокортикоидот алдостерон или андроген DHEAS што се лачат. од други зони на надбубрежниот кортекс.[20]
Патологија[уреди | уреди извор]
Мутациите во генот CYP11A1 резултираат со дефицит на стероиден хормон, предизвикувајќи мал број на случаи на ретката и потенцијално фатална состојба липоидна конгенитална адренална хиперплазија.[21][22][23] Недостатокот на CYP11A1 може да резултира и со хиперпигментација, хипогликемија и рекурентни инфекции.[24]
Инхибитори[уреди | уреди извор]
Инхибиторите на ензимите за расцепување на страничниот синџир на холестерол вклучуваат аминоглутетимид, кетоконазол и митотан, меѓу другите.[25][26][27]
Поврзано[уреди | уреди извор]
- Стероидоген ензим
- Цитохром P450 оксидаза
Наводи[уреди | уреди извор]
|
Понатамошно читање[уреди | уреди извор]
- ↑ 1,0 1,1 1,2 1,3 „Steroidogenic enzymes: structure, function, and role in regulation of steroid hormone biosynthesis“. The Journal of Steroid Biochemistry and Molecular Biology. 43 (8): 779–804. December 1992. doi:10.1016/0960-0760(92)90307-5. PMID 22217824.
- ↑ „Entrez Gene: CYP11A1 cytochrome P450, family 11, subfamily A, polypeptide 1“.
- ↑ „Placental steroid hormone synthesis: unique features and unanswered questions“. Biology of Reproduction. 54 (2): 303–311. February 1996. doi:10.1095/biolreprod54.2.303. PMID 8788180.
- ↑ „Neurosteroid metabolism in the human brain“. European Journal of Endocrinology. 145 (6): 669–679. December 2001. doi:10.1530/eje.0.1450669. PMID 11720889.
- ↑ „Stoichiometry of mitochondrial cytochromes P-450, adrenodoxin and adrenodoxin reductase in adrenal cortex and corpus luteum. Implications for membrane organization and gene regulation“. European Journal of Biochemistry. 157 (1): 27–31. May 1986. doi:10.1111/j.1432-1033.1986.tb09633.x. PMID 3011431.
- ↑ „Induction and mitochondrial localization of cytochrome P450scc system enzymes in normal and transformed ovarian granulosa cells“. The Journal of Cell Biology. 111 (4): 1373–1381. October 1990. doi:10.1083/jcb.111.4.1373. PMC 2116250. PMID 2170421.
- ↑ 7,0 7,1 „Mechanism of corticotropin and cAMP induction of mitochondrial cytochrome P450 system enzymes in adrenal cortex cells“. The Journal of Biological Chemistry. 265 (33): 20602–20608. November 1990. doi:10.1016/S0021-9258(17)30545-8. PMID 2173715.
- ↑ Topological studies of cytochromes P-450scc and P-45011 beta in bovine adrenocortical inner mitochondrial membranes.
- ↑ „Preparation of antiserum to rat cytochrome P-450 cholesterol side chain cleavage, and its use for ultrastructural localization of the immunoreactive enzyme by protein A-gold technique“. Endocrinology. 118 (4): 1353–1365. April 1986. doi:10.1210/endo-118-4-1353. PMID 3948785.
- ↑ „Mechanisms of ionic activation of adrenal mitochondrial cytochromes P-450scc and P-45011 beta“. The Journal of Biological Chemistry. 256 (9): 4329–4335. May 1981. doi:10.1016/S0021-9258(19)69437-8. PMID 6783659.
- ↑ „Routes and regulation of NADPH production in steroidogenic mitochondria“. Endocrine Research. 21 (1–2): 231–241. 1995. doi:10.3109/07435809509030439. PMID 7588385.
- ↑ „Isolation of a cDNA for adrenodoxin reductase (ferredoxin-NADP+ reductase). Implications for mitochondrial cytochrome P-450 systems“. European Journal of Biochemistry. 169 (3): 449–455. December 1987. doi:10.1111/j.1432-1033.1987.tb13632.x. PMID 3691502.
- ↑ 13,0 13,1 13,2 „Mitochondrial cytochrome P-450scc. Mechanism of electron transport by adrenodoxin“. The Journal of Biological Chemistry. 255 (7): 3057–3061. April 1980. doi:10.1016/S0021-9258(19)85851-9. PMID 6766943.
- ↑ „Adrenal mitochondrial cytochrome P-450scc. Cholesterol and adrenodoxin interactions at equilibrium and during turnover“. The Journal of Biological Chemistry. 256 (9): 4321–4328. May 1981. doi:10.1016/S0021-9258(19)69436-6. PMID 7217084.
- ↑ „Structural basis for pregnenolone biosynthesis by the mitochondrial monooxygenase system“. Proceedings of the National Academy of Sciences of the United States of America. 108 (25): 10139–10143. June 2011. Bibcode:2011PNAS..10810139S. doi:10.1073/pnas.1019441108. PMC 3121847. PMID 21636783.
- ↑ „Electron leakage from the mitochondrial NADPH-adrenodoxin reductase-adrenodoxin-P450scc (cholesterol side chain cleavage) system“. Archives of Biochemistry and Biophysics. 305 (2): 489–498. September 1993. doi:10.1006/abbi.1993.1452. PMID 8396893.
- ↑ „Antioxidant protective mechanisms against reactive oxygen species (ROS) generated by mitochondrial P450 systems in steroidogenic cells“. Drug Metabolism Reviews. 38 (1–2): 171–196. 2006. doi:10.1080/03602530600570040. PMID 16684656.
- ↑ 18,0 18,1 18,2 „Transcriptional regulation of steroidogenic genes: STARD1, CYP11A1 and HSD3B“. Experimental Biology and Medicine. 234 (8): 880–907. August 2009. doi:10.3181/0903-MR-97. PMID 19491374.
- ↑ „Transcriptional regulation of human CYP11A1 in gonads and adrenals“. Journal of Biomedical Science. 14 (4): 509–515. July 2007. doi:10.1007/s11373-007-9177-z. PMID 17594537.
- ↑ „Selective increases in adrenal steroidogenic capacity during acute respiratory disease in infants“. European Journal of Endocrinology. 133 (5): 552–556. November 1995. doi:10.1530/eje.0.1330552. PMID 7581984.
- ↑ „Phenotypic variations in lipoid congenital adrenal hyperplasia“. Pediatric Endocrinology Reviews. 3 (3): 258–271. March 2006. PMID 16639391.
- ↑ „Homozygous mutation of P450 side-chain cleavage enzyme gene (CYP11A1) in 46, XY patient with adrenal insufficiency, complete sex reversal, and agenesis of corpus callosum“. The Journal of Clinical Endocrinology and Metabolism. 91 (8): 2821–2826. August 2006. doi:10.1210/jc.2005-2230. PMID 16705068.
- ↑ „Severe combined adrenal and gonadal deficiency caused by novel mutations in the cholesterol side chain cleavage enzyme, P450scc“. The Journal of Clinical Endocrinology and Metabolism. 93 (3): 696–702. March 2008. doi:10.1210/jc.2007-2330. PMC 2266942. PMID 18182448.
- ↑ „Primary adrenal insufficiency: New genetic causes and their long-term consequences“. Clinical Endocrinology. 92 (1): 11–20. 2020. doi:10.1111/cen.14109. PMC 6916405. PMID 31610036.
- ↑ Becker KL (2001). Principles and Practice of Endocrinology and Metabolism. Lippincott Williams & Wilkins. стр. 735–. ISBN 978-0-7817-1750-2.
- ↑ Jameson JL, De Groot LJ (18 May 2010). Endocrinology - E-Book: Adult and Pediatric. Elsevier Health Sciences. стр. 301–302. ISBN 978-1-4557-1126-0.
- ↑ Ortiz de Montellano PR (13 March 2015). Cytochrome P450: Structure, Mechanism, and Biochemistry. Springer. стр. 851–879. ISBN 978-3-319-12108-6.
Синтеза на стероидни хормони[уреди | уреди извор]


Дополнителни слики[уреди | уреди извор]
Надворешни врски[уреди | уреди извор]
- Цитохром+P450scc во Националната медицинска библиотека на САД, медицински предметни наслови (MeSH)