Боров модел
На оваа страница е потребен превод на македонски. Оваа страница (или пасус) не е напишана на јазик којшто е македонски. Ако е наменета за читателите од тој јазик, треба да биде преместена на јазичното издание на Википедија на тој јазик. Видете го целосниот список на јазични изданија. Ако страницата (или пасусот) не е преведена на македонски во рок од една седмица, содржината која е на друг јазик ќе биде избришана. |
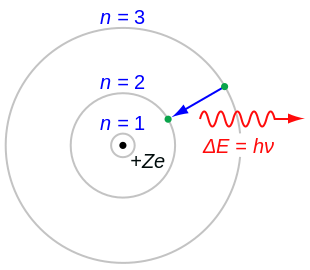
Во атомската физика, Ратерфорд–Боровиот модел или Боровиот модел, го прикажува атомот како мало, позитивно наелектризирано јадро опкружен со електрони што патуваат во округли орбити околу јадрото—слично како во сончевиот Систем. Според кубниот модел (1902), Томсоновиот модел (1904), the Сатуранскиот модел (1904), и Радерфордовиот модел (1911) доаѓа Ратерфорд-Боровиот модел или скратено само Боровиот модел(1913).Подобрувањето на Радерфордовиот модел е повеќе само квантно физичко претставување на моделот.
Успехот на моделот лежи во објаснувањето на Рајдерберговата формула за спектрално зрачење од атомскиот водород. Додека Рајдерберговата формула била практично позната, немала теоретско објаснување сè додека не бил претставен Боровиот модел. Не само што Боровиот модел ја објаснил причината за структурата на Рајдерберговата формула, туку исто така снабди и оправдување за емперискиот резултат во фундаменталната физичка константа.
Боровиот модел е релативно примитевен модел на водородно јадро, споредено со валентниот атом. Како теорија може да се проследи преку првото предвидување на водородниот атом користејки многу по прецизна квантна механика и поради тоа може да се смета како застарена научна теорија. Сепак, поради едноставноста и точноста за некои селектирани системи, Боровиот модел сè уште се предава на некои студенти за да се запознаат со квантна механика пред да се премине на покомплицирани но попрецизни валентни атоми.
Потекло[уреди | уреди извор]

Во почетокот на 20 век, експериментите од Ернест Ратерфорд потврдиле дека атомите се состојат од облак од негативно наелктризирани електрони кои обкружуваат мало, позитивно наелектризирано јадро.[2] Со оглед на тоа дека податоците од овој експеримент, Ратерфорд размислувал за планетарен модел на атомот - модел каде што електроните орбитираат соларено јадро - сепак планетарниот модел има техничка не исправност. Законите на класичната механика предвидуваат дека електронот испушта електромагнетно зрачење додека го орбитира јадрото.Бидејќи електронот би губел енергирја, тој би колабирал во јадрото за време од околу 16 пикосекунди.[3] Овој модел на атомот е неточен бидејќи предвидува дека атомот е не стабилен.[4]
Исто така, додека електронот колабира зрачењето брзо ќе се зголемува во честота додека орбитата се смалува. Сепак при крајот на 19 век експериментите со електрично испуштањеhпокажале дека атомите би зрачеле светлоaсамо на одредена честота.
За да се надмине оваа потешкотија, Нилс Борpго предложил rмоделот на атомот денеска познат како Боров модела на атомот. Тој предложол дека електронит еможат да имаат одредени движења:
- Електрони во орбитата на атомското јадро.
- Електроните можат да орбитираат стабилно, без зрачење само во одредени орбитали, во одредени оддалечености од јадрото. Овие орбитали се поврзани со дефинитивна енергија и се исто така наречени енергетски школки или енергетски нивоа. Во овие орбитали, електронското забрзување не резултира во зрачење и губење на енергија како што се бара според класичната електромагнетност.
- Електроните можат само да добијат и да испуштат енергија скокајќи од една орбитала во друга, со тоа што апсорбираат и зрачат електромагнетно зрачење со честота v одредена од разликата на енергијата помеѓу орбиталите одредена одПленковата релација:
каде што h е Пленковата константа. Честота од емитуваното зрачење во орбита во одреден период T е како што би била во класичната механика::
Значајноста на Боровиот модел е законот за класична механика применета во движењето на електронот околу јадродто само кога е ограничено од квантното правило. Иако Праволото 3 не е комплетно дефинирано во малите орбитали, бидејќи процесот на зралење вклучува две орбитали со два различни периода, Бор можел да ја одреди енергетската разлика помеѓу нивоата користејки го Правилото 3 и да се стигне до точно квантно правило:
Каде n = 1, 2, 3, ... се вика принципот на квантен број, и ħ = h/2π. Најмалата вредност на n е 1; ова дава најмал можен орбитален полупречник од 0.0529 nm познато како Боров полупречник. Откако електронот е во најмалата орбитала, не може да дојде поблиску до протонот. Почнувајќи од аголниот момент квантно правило, Бор можел само да ја пресмета енергијата на дозволените орбиталиoна водородниот атом, и на другите атоми слични на водородот.
Боровиот кондицијал, дека аголниот момент е број помножен со ħ подоцна бил преиспитан во 1924 како стоечкиот бранов кондиција: електронот е опишан како бран и цел број од бранови должини мора да се соберат на обемот на орбитата на електронот:
Заменувајќи ја Броглиевата бранова должина од λ = h/p се репродуцира Боровото правило. Во 1913 брановото однесување на материјата како што е електронот не се очекувало.
Во 1925 нов вид механика бил предложен, квантна механика, во која Боровиот модел на електронот патувајќи во квантна орбитала бил издолжен во попрецизен моделна електронот во движење. Новата теорија била предложена од Вернер Хајзенберг. Друг вид од истата теорија, бранова механика, била откриена од Австрискиот физичар Ервин Шредингер не зависно и со друго разбирање.
Електронски нивоа на енергија[уреди | уреди извор]
Боровиот модел дава скоро точен резултат само во систем каде две наелектризирани точки кружат околу себе со брзина многу помала од брзината на светлината. Ова не само што вклучува системи со еден електрони како што се водородниот атом, едно јонизираниот хелиум, двојонизираниот литиум, исто така вклучува и Рајдерберговата состојба на секој атом каде што еден електрон е далеку од се друго. Може да се користи за K-линијата X-реј транзициони пресметки ако други претпоставки се додадат. Во високо енергетската физика, може да се користи за пресметување на масата на тешки кварк месони.
За пресметување на орбиталите потребни се две претпоставки.
- Класична механика
- Електронот е ограничен во кружна орбитала од електростатичка атракција. Центрипеталната сила е еднаква на Коломбовиот сила.
- каде me е електронската маса, e е полнежот на електронот, ke е Коломбовата константа и Z е атомскиот број. Се претпоставува тука дека масата на јадрото е многу поголема од таа на електронот. Оваа равенка ја одредува брзината на електронот во секој полупречник:
- Исто така ја одредува целосната енергија на електронот во секој полупречник:
- Целосната енергија е негативна и инверзно пропорционална на r. Ова значи дека презема енергија за да го привлече електронот што кружи околу протонот. Џа бесконечни вредности на r, енергијата е нула, соодветни на бездвижен електрон бесконечно далеку од протон. Целосната енергија е пола од потенцијалната енергија.
- Квантно правило
- Аголниот моментум L = mevr е број помножен со ħ:
| Потеклно на равенката: |
|---|
| Ако електрон во атом не се движи на орбитала со период T, класнично електромагнетното зрачење ќе се повторува секој орбитален период. Ако спојувањето на електромагнетното поле е слабо, со тоа што орбитата не се распаќа многу во еден циклус, зрачењето ќе се емитува во узорец што се повторува секој период, со тоа што Фориеровите трансформации ќе имаат честоти што се само множители од 1/T. Ова е класичниот закон за зралење: честотите емитувани се цели броеви множители на 1/T.
Во квантната механика, емитувањето мора да биде во квант од светло, од честоти содржани од цели броеви множители од 1/T, со тоа класичната механика е приближен опис на големи квантни броеви. Ова значи дека нивоата на енергија се соодветни со класнична орбитала со период од 1/T мора да има близу енергетски нивоа кои се разликуваат во енергија спрема h/T, и треба да се еднакво оддалечени од тоа ниво, Бор бил загрижен дали енергетскиот простор 1/T треба да биде калкулиран со период од енергетската состојба , or . Бор размислувал за кружни орбитали. Класично, овие орбитали морало да се распаѓаат на помали кругови каде фотони се емитувани. Нивото на оддалеченост помеѓу кружните орбитали може да се пресмета со соодветната формула. За водородниот атом. класичните орбитали имаат период одлучен од Кемплеровиот трет законtза да се земе со размер од r3/2. Енергетската скала како 1/r, со тоа што просторната формула има износ од Можно е да се утврди енергетското ниво со рекурзивно спуштање орбитала по орбитала, но има скратен пат. Аголниот момент L од кружната орбиталана скала како √r.
Претпоставувајќи со Бор дека квантинизирана вредност од L се еднаквно оддалечени, оддалеченоста помеѓу блиските енергии е Аголниот момент треба да биде цел број множител на ħ, Вака стигнал Бор до неговиот модел. |
- Заменувајќи го изразот за брзина ни дава равенка за r во однос на n:
- дозволениот орбитален полупречник за секој n е:
- Најмалата можна вредност на r во водородниот атом (Z=1) се нарекува Боров полупречник и е еднаков на
- Енергијата на n-тото ниво за секој атом се одлучува според полупречникот и квантниот број:
Електронот во најмалото енергетско ниво (n = 1) од таму има околу 13.6 eV помалце енергејиа него бездвижен електрон бесконечно далеку од јадрото. Следното енергетско ниво (n = 2) е −3.4 eV. Третото (n = 3) is −1.51 eV, итн. За поголемите вредности на n, овие се исто така сврзните енергии за високо возбуден атом со еден електрон во голема кружна орбитала околу атомот.
Водородната формула исто така се совпаѓа со Валисовиот продукт.[5]
Комбинацијата од природни константи во формулата за енергија се нарекува Рајдербергова енергија(RE):
Овој израз е разјаснет преку интерпретација на изразот во комбинации од природни единици:
- е смирена масна енергија на електронот (511 keV)
- е структурна константа
Бидејќи оваа деривација е претпоставката дека околу јадрото орбитира еден електро, можеме да го генерализираме резултатот допуштајќи го јадрото да има полнеж q = Z e каде Z е атомскиот број. Ова ќе ни го даде нивото на енергија за водородните атоми, што можат да послужат како груби целни-големини приближување на вистинското ниво на енергија:
Вистинското ниво на енергија Може да се реши со анализа на повеќе од еден електрон, бидејќи електроните не примаат влијание само од јадротоbтуку исто така и од Колумбовата сила.
Кога Z = 1/α (Z ≈ 137), движењетос станува високо релевантно, и Z2 го прекинува α2 во R; Орбиталаната енергија е споредлива со мирната енергија. Доволно големи јадра, ако се стабилни, би ја редуцирале својата промена создавајќи еден затворен електрон од вакуумот, исфрлајќи го позитронот во бесконечност. Ова е теоретскиот феномен на електромагнетниот полнеж кој предвидува максимален јадрен полнеж. Емитувањето на такви позитрони било посматрано во високи јони за да се создаваат привремено супер тешки јадра.[се бара извор]
Боровата формула правилно ги користи редуцираните масиoна електронот и протон во сите ситуации, наместо масата на електронот,
Рајдберговата формула[уреди | уреди извор]
Рајдберговата формула, која била позната емпириски пред Боровата формула, се смета во Боровата теорија како опис на енергиите на транзиција на квантни скоковиbпомеѓу едно орбитално енргетско ниво. Боровата формула ја дава бројната вредност на веќе познатите и измерените Рајдбергови константи, но во однос на по фундаментални константи на природата, вклучувајќи го и електронскиот полнеж и Планковата константа.
Кога електронот ќе се помести од неговото оригинално енергетско ниво во повисоко нив, тогаш скока назад секое ниво додека не стигне до оригиналната позиција, што резултира во фотон. Користејќи ја формулата за различни енергетски нивоа на водоред може да се најде брановата должина на светлото еметувано од водороден атом.
Енергијата на фотон емитуван од водороден атом е дадена преку разликата на два енергетски нивоа на водород.:
каде nf е финалното енергетско ниво и ni е првичното енергетско ниво.
Бидејќи енергијата на фотонот е
Брановата должина на фотон е:
Ова е познато како Рајдбергова формула и Рајдбергова константа R е RE/hc, или RE/2π во природни броеви. Оваа формула била позната во 19 век за научници кои изучувале спектроскопија, но немало теоретско објаснување за оваа форма или теоретска претпоставка за вредноста на R, сè до Бор.
За да се аплицира за атоми со повеќе од еден атом, Рајдберговата формула може да се модифицира заменувајќи Z со Z−b или n со n−b каде b е константа претставувајќи скрининг ефект поради внатрешната школка и други електрони. Ова било заклучено емпериски пред Бор да го презентира својот модел.
Модел на школка на потешки атоми[уреди | уреди извор]
Бор го проширил моделот од водор за да даде приближен модел за потешките атоми. Ова дало физичка слика што репродуцирала многу познати атомски својства за првпат.
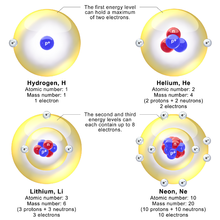
Потешките атоми имаат повеќе протони во јадрото, и повеќе електрони за да се изедначи полнежот. Боровата идеја била дека секоја дискретна орбитала може да задржи само одреден број на електрони. Откако таа орбитала ќе се напуни, следното ниво мора да се користи. Ова му дава на атомот структура на школка, во која секоја школка одговара на секоја Борова орбитала.
Овој модел е уште поприближен него моделот на водород, бидејќи ги третира електроните во секоја школка како не-интерактивни. Електроните во крајните орбитали не само што го орбитираат јадрото, туку тие исто така ги движат внатрешните електрони, така делотворниот Z полнеж што го осеќаат е намален од бројот на електрони во внатрешните орбитали.
Пример атомот на литиум има електрони во најдолната 1s орбитала. Секој електрон го следи јадрениот полнеж од Z=3 минус ефектот на скрининг од другите, што грубо го намалува јадрениот полнеж за една единица. Ова значи дека највнатрешните електронски орбитала е приближно 1/4 од боровиот полупречник. Најнадворешниот електрон во литиумската орбитала на е грубо Z=1, бидејќи двата внатрешни електрони го намалуваат јадрениот полнеж за 2. Овој надворешен треба да биде на еден Боров полупречник од јадрото. Бидејќо електроните силно се одвратаат, описот на делотворниот полнеж е многу приближен. Но Моселиевиот закон експериментно ги сонди највнатрешниот пар на електрони, и покажува дека го користат јадрениот полнеж од приближно Z−1.
Во моделот на школка, овој феномен е објаснет од полнењето на школката. Последователните атоми стануваат помали бидејќи тие исполнуваат орбитали од иста големина, сè додека не се исполни орбиталата, тогаш следниот атом на табелта има слабо ограничен надворешен атом, правејќи го да се проширува. Првата Борова орбитала е исполнета кога има два електрони, што објаснува зошто хелиумот е инертен. Втората орбитала дозволува осум електрони, и кога ќе се исполни атомот е неон, пак инертен. Третата орбитала содржи пак осум, освен тоа што во поточниот Сомерфил третман има екстра "d" електрони. Третата орбитала може да држи екстра 10d електрони, но овие позиции не се исполнети сè додека не се исполнат уште неколку орбитали. Ова нерегуларно пополнување е ефект од реакција помеѓу електроните, што не се сметаат во Боровиот и Сомерфилдовиот модел.
Мослиевиот закон и пресметки на К-алфа X-реј емитувани линии[уреди | уреди извор]
Нилс Бор во 1962 рекол "Може да се види дека Радерфордовата работе не се сфатила сериозно. Не можеме да ја разбереме денес, но не била сфатена сериозно воопште. Вистинската промена дојде од Мослие."
Во 1913 Хенри Моселие пронашол емпириска релација помеѓу најсилните X-реј линии емитувани од атомите под електронско бомбардување, и нивниот атомски број Z. Мослие дошол до неговата емпириска формула преку Рајдберговата и Боровата формула.
Мослие му пишал на Бор, збунет околу неговите резултати, но Бор не можел да му помогне, Во тоа време, тој мислел дека највнатрешната школка "К" треба да има барем четири елктрони, не два што би го објаснило реузлтатот. Така Мослие ги издал своите резултати без теоретско објаснување.
Подоцна луѓето сфатиле дека ефектот бил предизвикан од промената на скрининг, со тоа што внатрешната школка содржела само два електрони. Во експериментот, еден од највнатрешните електрони во атом е изваден, оставајќи празен простор во највнатрешната Борова орбитала, што и останало само еден електрон. Овој празен простор птоа се полни со електрон од следната орбитала, што има n=2. Но n=2 електрони гледаат делотворна промена од Z−1, што е вредноста одговорна за полнежот на јадрото, кога еден електрон останува во највнатрешната Борова орбитала за скрининг на јадрениот полнеж +Z, и го намалува за− 1. Енергијата добиена од спуштањето на електронот од втората школка во првата ни го дава Мослиевиот закон за K-алфа линиите,
или
Недостатоци[уреди | уреди извор]
Боровиот модел ни дава не точна вредност L=ħ за земната состојба орбитален аголен момент. Познато е дека аголниот момент е нула од експериментот. Ова може да се репродуцира само во пософистициран полукласичен третнам како Сомерфилдовиот. Сепак и најсофисцираните полукласични модели не успеваат да го објаснат фактот дека највнатрешната енергетска состојба е сферно симетрлина - не покажува во никоја насока.
И покрај тоа во модерната целосно квантниот третман во фазниот простор, точната деформација на полукласичниот резултат се приспособува на вредноста на аголниот момент во точно делотворниот.
Во модерната квантна механика, електронот во водородот е сферен облак на веројатностtшто се згустува покрај јадрото. Стапката на постојаност на можноста на распаѓање во водородот е еднаква на инверзијата на Боровиот полупречник, но бидејќи Бор работел со кружни орбитали, фактот што овие два броја се согласни се смета за случајност.
Боровиот модел исто така има потешкотии со, или не може да објасни:
- Повеќе за спектралните поголеми атоми. Во најдобар случај може да ги предвиди К-алфа и некои L-алфа X-реј емитувања на поголемите атоми.
- релативната сила на спекралните линии, иако во некои едноставни случају, Боровата формула или некоја модификација од неа, може да даде разумна претпоставка.
- Постоењето на ситна структура и супер ситна структураiво спектралните линии, што е позната како последица на различните релативни и суптилни ефекти, како и компликации од електронското движење.
- Зимановиот ефект – се менува во спектралните линии поради надворешните магнетни полиња; овие се исто така поради компликации во квантниот принцип во интеркација со електронското движење и орбиталните магнетни полиња.
- Моделот исто така го прекршува принципот на несигурностiсо тоа што смета дека електронот има познати орбитали и локации, две работи што не можат да се измерат истовремено.
- Двојки и тројки: Се појавуваат во спектарот на некои атоми: Многу блиски парови од линии. Боровиот модел не може да каже некои нивоа на енергија мора да бидат блиску еден до друг.
- Повеќе-електронски Атоми: немаат нивоа на енергија предвидени од моделот. Не работи за хелиум.
Refinements[уреди | уреди извор]

Several enhancements to the Bohr model were proposed, most notably the Sommerfeld model or Bohr–Sommerfeld model, which suggested that electrons travel in elliptical orbits around a nucleus instead of the Bohr model's circular orbits.[1] This model supplemented the quantized angular momentum condition of the Bohr model with an additional radial quantization condition, the Sommerfeld–Wilson quantization condition[6][7]
where pr is the radial momentum canonically conjugate to the coordinate q which is the radial position and T is one full orbital period. The integral is the action of action-angle coordinates. This condition, suggested by the correspondence principle, is the only one possible, since the quantum numbers are adiabatic invariants.
The Bohr–Sommerfeld model was fundamentally inconsistent and led to many paradoxes. The magnetic quantum number measured the tilt of the orbital plane relative to the xy-plane, and it could only take a few discrete values. This contradicted the obvious fact that an atom could be turned this way and that relative to the coordinates without restriction. The Sommerfeld quantization can be performed in different canonical coordinates and sometimes gives different answers. The incorporation of radiation corrections was difficult, because it required finding action-angle coordinates for a combined radiation/atom system, which is difficult when the radiation is allowed to escape. The whole theory did not extend to non-integrable motions, which meant that many systems could not be treated even in principle. In the end, the model was replaced by the modern quantum mechanical treatment of the hydrogen atom, which was first given by Wolfgang Pauli in 1925, using Heisenberg's matrix mechanics. The current picture of the hydrogen atom is based on the atomic orbitals of wave mechanics which Erwin Schrödinger developed in 1926.
However, this is not to say that the Bohr model was without its successes. Calculations based on the Bohr–Sommerfeld model were able to accurately explain a number of more complex atomic spectral effects. For example, up to first-order perturbations, the Bohr model and quantum mechanics make the same predictions for the spectral line splitting in the Stark effect. At higher-order perturbations, however, the Bohr model and quantum mechanics differ, and measurements of the Stark effect under high field strengths helped confirm the correctness of quantum mechanics over the Bohr model. The prevailing theory behind this difference lies in the shapes of the orbitals of the electrons, which vary according to the energy state of the electron.
The Bohr–Sommerfeld quantization conditions lead to questions in modern mathematics. Consistent semiclassical quantization condition requires a certain type of structure on the phase space, which places topological limitations on the types of symplectic manifolds which can be quantized. In particular, the symplectic form should be the curvature form of a connection of a Hermitian line bundle, which is called a prequantization.
Поврзано[уреди | уреди извор]
|
|
Наводи[уреди | уреди извор]
Footnotes[уреди | уреди извор]
- ↑ 1,0 1,1 Akhlesh Lakhtakia (Ed.); Salpeter, Edwin E. (1996). „Models and Modelers of Hydrogen“. American Journal of Physics. World Scientific. 65 (9): 933. Bibcode:bdchgrifu..65..933L Проверете го
|bibcode=value (help). doi:10.1119/1.18691. ISBN 981-02-2302-1.CS1-одржување: излишен текст: список на автори (link) - ↑ Niels Bohr (1913). „On the Constitution of Atoms and Molecules, Part I“ (PDF). Philosophical Magazine. 26 (151): 1–24. doi:10.1080/14786441308634955.
- ↑ „Olsen and McDonald 2005“ (PDF). Архивирано од изворникот (PDF) на 2019-09-09. Посетено на 2016-04-03.
- ↑ „CK12 – Chemistry Flexbook Second Edition – The Bohr Model of the Atom“. Посетено на 30 September 2014.
- ↑ "Revealing the hidden connection between pi and Bohr's hydrogen model." Physics World (November 17, 2015)
- ↑ A. Sommerfeld (1916). „Zur Quantentheorie der Spektrallinien“. Annalen der Physik. 51 (17): 1. Bibcode:1916AnP...356....1S. doi:10.1002/andp.19163561702.
- ↑ W. Wilson (1915). „The quantum theory of radiation and line spectra“. Philosophical Magazine. 29 (174): 795–802. doi:10.1080/14786440608635362.
Primary sources[уреди | уреди извор]
- Niels Bohr (1913). „On the Constitution of Atoms and Molecules, Part I“ (PDF). Philosophical Magazine. 26 (151): 1–24. doi:10.1080/14786441308634955.
- Niels Bohr (1913). „On the Constitution of Atoms and Molecules, Part II Systems Containing Only a Single Nucleus“ (PDF). Philosophical Magazine. 26 (153): 476–502. doi:10.1080/14786441308634993.
- Niels Bohr (1913). „On the Constitution of Atoms and Molecules, Part III Systems containing several nuclei“. Philosophical Magazine. 26: 857–875. doi:10.1080/14786441308635031.
- Niels Bohr (1914). „The spectra of helium and hydrogen“. Nature. 92 (2295): 231–232. Bibcode:1913Natur..92..231B. doi:10.1038/092231d0.
- Niels Bohr (1921). „Atomic Structure“. Nature. 107 (2682): 104–107. Bibcode:1921Natur.107..104B. doi:10.1038/107104a0.
- A. Einstein (1917). „Zum Quantensatz von Sommerfeld und Epstein“. Verhandlungen der Deutschen Physikalischen Gesellschaft. 19: 82–92. Reprinted in The Collected Papers of Albert Einstein, A. Engel translator, (1997) Princeton University Press, Princeton. 6 p. 434. (provides an elegant reformulation of the Bohr–Sommerfeld quantization conditions, as well as an important insight into the quantization of non-integrable (chaotic) dynamical systems.)
Further reading[уреди | уреди извор]
- Linus Carl Pauling (1970). General Chemistry. Chapter 5-1 (3. изд.). San Francisco: W.H. Freeman & Co.
- Reprint: Linus Pauling (1988). General Chemistry. New York: Dover Publications. ISBN 0-486-65622-5.
- George Gamow (1985). Thirty Years That Shook Physics. Chapter 2. Dover Publications.
- Walter J. Lehmann (1972). Atomic and Molecular Structure: the development of our concepts. Chapter 18. John Wiley and Sons.
- Paul Tipler and Ralph Llewellyn (2002). Modern Physics (4. изд.). W. H. Freeman. ISBN 0-7167-4345-0.
- Klaus Hentschel : Elektronenbahnen, Quantensprünge und Spektren, in: Charlotte Bigg & Jochen Hennig (eds.) Atombilder. Ikonografien des Atoms in Wissenschaft und Öffentlichkeit des 20. Jahrhunderts, Göttingen: Wallstein-Verlag 2009, pp. 51–61
- Steven and Susan Zumdahl (2010). Chemistry. Chapter 7.4 (8. изд.). Brooks/Cole. ISBN 978-0-495-82992-8.
- Helge Kragh (2011). „Conceptual objections to the Bohr atomic theory — do electrons have a "free will" ?“. European Physical Journal H. 36 (3): 327. Bibcode:2011EPJH...36..327K. doi:10.1140/epjh/e2011-20031-x.
Надворешни врски[уреди | уреди извор]
- Standing waves in Bohr’s atomic model An interactive simulation to intuitively explain the quantization condition of standing waves in Bohr's atomic model
| „Боров модел“ на Ризницата ? |































