Хепарин
 | |
 | |
| Систематско (IUPAC) | |
|---|---|
| Клинички податоци | |
| Бременосна категорија |
|
| Начин на издавање |
|
| Начин на примена | i.v., s.c. |
| Фармакокинетички податоци | |
| Биорасположливост | nil |
| Метаболизам | hepatic |
| Полувреме на елиминација | 1.5 hrs |
| Екскреција | ? |
| Назнака | |
| CAS-број | 9005-49-6 |
| ATC код | B01AB01 C05 S01 |
| DrugBank | APRD00056 |
| ChemSpider | 17216115 |
| UNII | T2410KM04A |
| ChEMBL | CHEMBL526514 |
| Хемиски податоци | |
| Формула | C12H19NO20S3 |
| Моларна маса | 12000–15000 g/mol |
| |
| (провери) | |
Под поимот хепарин (од старогрчки ηπαρ (hepar), црн дроб) се подразбира група на ендогени полисахариди исто така познати под името нефракциониран хепарин, кои делуваат инхибиторно на коагулационата каскада и затоа се користат во терапевски цели како средство за спречување на згрутчувањето на крвта, т.е. како антикоагулантни средства (антикоагуланси). Хепаринот се користи пред сè во спречувањето и лекувањето на тромбоза и емболија.
Антикоагулантниот ефект на хепарините се заснова на засилување на дејството на антитромбин III, ензим што циркулира во крвта и е инхибитор на активирани фактори на коагулацијата. Со врзување на хепарин за антитромбин III доаѓа до засилување на неговата активност за околу 1000 пати.
Хепаринот не се апсорбира преку гастроинтестиналниот тракт и затоа се администрира парентерално, т.е. како инјекција или како континуирана инфузија, во зависност од областа на апликација. За надворешна употреба, хепаринските препарати се нудат како гел или маст за поддршка на третман на акутен оток по тапи повреди (модринки)[1], и покрај тоа што хепаринот, поради неговите физичко-хемиски својства, не може да се докаже дека продира во кожата и затоа не може ефикасно да се апсорбира.[2]
Дозата на хепарин не се дава во грамови, туку во меѓународни единици (IU): Една единица спречува згрутчување на 1 ml цитратна плазма по додавање на CaCl2 на 37 °C за еден час.
Фракционирана верзија на хепаринот, позната како нискомолекуларен хепарин е исто така достапна.[3]
Структура[уреди | уреди извор]
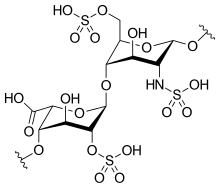
Хепарините се гликозаминогликани, кои се состојат од наизменични секвенци на D-гликозамин и уронска киселина (D-гликуронска киселина или L-идуронска киселина).[4] Многу од мономерните единици содржат сулфатни групи поврзани со атоми на кислород и азот.
Почнувајќи од должина на синџир од пет моносахариди (три D-гликозамини и две уронски киселини), гликозаминогликаните покажуваат антикоагулантно дејство. Во зависност од градежните единци на синџирот, тие имаат многу негативни полнежи, преку кои се врзуваат за антитромбин III. Нативниот хепарин е познат и како нефракциониран хепарин (англиски: unfractionated heparin, UFH), додека деполимеризираните хепарини со просечна релативна моларна маса под 8000 (со најмалку 80% од хепарините под 8000)[5] се познати како хепарини со ниска молекуларна тежина (англиски: low molecular weight heparins, LMWH) или нискомолекуларни хепарини.
Нефракционираниот хепарин во медицинска употреба (исто така наречен стандарден хепарин) има моларна маса од 6000 до 30.000 далтони (Da). Преку хемиско или ензимско фракционирање (расцепување) се добиваат нискомолекуларни, терапевтски корисни хепарини со просечна моларна маса од околу 5000 далтони: цертопарин (5400 Da), далтепарин (6100 Da), еноксапарин (4500 Da), парнапарин (50) , надропарин (4300 Da). ), ревипарин (4400 Da) и тинзапарин (6500 Da).[6]
Биосинтеза[уреди | уреди извор]
Во телото, хепаринот се продуцира од страна на мастоцитите и базофилните гранулоцити во различни органи (на пример, белите дробови, цревата, тимусот и слезината).[7]
Механизам на дејство[уреди | уреди извор]
Хепаринот се врзува за антитромбин III, ензим кој циркулира во крвта и е протеазен инхибитор на следниве фактори на коагулација: тромбин (фактор IIa) и активиран фактор X, во помала мера активираните фактори IX, XI and XII, како и активираниот фактор VII во мала мера.[8] Исто така, комлексот хепарин-антитромбин III ја инхибира активираната серин протеаза каликреин. Врзувањето за антитромбин III предизвикува конформациска промена во неговиот активен центар што резултира со негово активирање. Стапката на инактивација на факторите на коагулација од страна на антитромбин може да се зголеми до 1000 пати поради врзувањето на хепаринот.
Конформациската промена на антитромбин при врзувањето за хепарин ја засилува неговата активност во инхибиција на факторот Xa. За разлика од тоа, за инактивацијата на тромбин е потребно формирањето на троен комплекс помеѓу антитромбин, тромбин и хепарин. Поради оваа причина, активноста на хепаринот против тромбин зависи неговата големина, при што тројниот комплекс бара големина на хепаринот од најмалку 18 сахаридни единици за да може ефикасно да се формира. Поради ова, нискомолекуларните хепарини го инхибираат претежно само факторот Xa.
Фармакокинетика[уреди | уреди извор]
Хепаринот (UFH) се администрира интравенски или поткожно (супкутано). Поткожната администрација на UFH резултира со 30% биорасположивост. Со интравенска администрација, првично доаѓа до брза елиминација на 40% од инјектираниот UFH (брз процес на заситување; поради многуте негативни полнежи во структурата на UFH, тој се врзува за ендотелот и за макрофагите, како и за плазмените белковини) со полуживот од 5 -15 минути, што потоа се претвора во побавна елиминација со полуживот од 60-90 минути (ренална елиминација преку гломеруларна филтрација и тубуларна секреција). Само откако сите места каде UFH се врзува ќе постанат заситени, односот доза-ефект станува линеарен и се постигнува терапевтски ефективно ниво. UFH не ја преминува плацентата и не поминува во мајчиното млеко, така што може да се користи за време на бременост и доење.
Нискомолекуларните хепарини (LMWH) се администрираат поткожно. Тие имаат помал афинитет за плазмените белковини, васкуларните матрични белковини, макрофагите, тромбоцитите и ендотелните клетки. Ова ја објаснува подобрата биорасположивост, подолгиот полуживот на елиминација и исклучиво реналниот клиренс на LMWH. По поткожната инјекција се постигнува над 90% биорасположивост. Ако функцијата на бубрезите е нарушена, дозата можеби ќе треба да се намали. LMWH не ја преминува плацентата и не е познато дека преминува во мајчиното млеко.
Медицинска употреба[уреди | уреди извор]
Нефракционираниот хепарин (UFH) е индициран, меѓу другото, за:
- профилакса на периоперативна и постоперативна тромбоза
- терапија на длабока венска тромбоза и белодробна емболија
- терапија на артериска емболија
- како антикоагулант во екстракорпорална циркулација (на пр. дијализа)
- под посебни аспекти:
- за терапија на DIC (= дисеминирана интраваскуларна коагулација)
- за дополнителна терапија на тромболиза
- за третман на акутен миокарден инфаркт.
Нискомолекуларниот хепарин (LMWH) е индициран, меѓу другото за:
- за пери- и постоперативна профилакса на венска тромбоза
- терапија на длабока венска тромбоза
- терапија на немасивна (нормотензивна) белодробна емболија
- профилакса на тромбоза кај нестабилна ангина пекторис и делумно кај акутен коронарен синдром
- како антикоагулант во хемодијализа.
За повеќето од нискомолекуларните хепарини сè уште може да нема одобрение за користење за секоја од овие индикации.
Споредба - нефракциониран хепарин и нискомолекуларни хепарини[уреди | уреди извор]
Предности на нефракционираниот хепарин (UFH)[уреди | уреди извор]
- достапен е антидот - протамин за целосно антагонизирање на дејството. Кај нискомолекуларните хепарини, протамин покажува само делумен ефект.
- за разлика од нискомолекуларните хепарини, нефракционираниот хепарин може да се администрира и во случај на ренална инсуфициенција (GFR < 30ml/min)
Предности на нискомолекуларните хепарини (LMWH)[уреди | уреди извор]
- помало неспецифично врзување за плазмени белковини и клетки
- подобра биорасположливост (90% наспроти 30%)
- помалку несакани ефекти, значително помала стапка на хепарин индуцирана тромбоцитопенија тип II (HIT II)
- околу двапати подолг полуживот од нефракционираниот хепарин
- константен сооднос на доза-дејство, најчесто не се потребни лабораториски контроли
- исклучиво елиминација преку бубрезите
- речиси целосна биорасположливост по субкутана инјекција
- помала интеракција со тромбоцитите, не доаѓа до неутрализација од страна на тромбоциниот фактор 4 (PF-4)
Контраиндикации и ограничувања во употребата[уреди | уреди извор]
Хепарините не смеат да се користат ако постои сомнителна или постоечка наклонетост кон крварење, гастроинтестинални улкуси и доколку постои веројатност за спонтан абортус. Неопходна е критична анализа на придобивките и ризиците од терапијата со хепарин како и внимателно лабораториско следење на пациентот во случај на:
- артериска хипертензија (висок крвен притисок) отпорна на третман и хипертензивна ретинопатија
- заболувања на црниот дроб и бубрезите со нарушена функција, акутен панкреатит
- тешки метаболички болести како што е дијабетес мелитус
- напреднат малигнитет
- напредна возраст (со зголемен морбидитет)
- преосетливост или претходен HIT II (хепарин индуцирана тромбоцитопенија тип 2)
високо дозиран хепарин:
- постоечко крварење или зголемена можност за внатрешно крварење
- пункција на артерии и паренхиматозни органи, интрамускулни инјекции (<7 дена)
- свежи операции (во зависност од времетраењето и видот на интервенцијата)
- бактериски ендокардитис
- дефекти на митралниот залисток на срцето со атријална фибрилација.
Во случај на процедури за регионална анестезија блиску до ’рбетниот мозок (спинална анестезија или епидурална анестезија), нефракционираниот хепарин (UFH) треба да се прекине четири до шест часа претходно и повторно да се дава не порано од еден час по интервенцијата. Во случај на LMWH профилакса, активната супстанција треба да се прекине 12 часа претходно, во случај на LMWH терапија 24 часа претходно и да се дава повторно дури четири часа по процедурата.[9][10]
Несакани дејства[уреди | уреди извор]
Главниот несакан ефект на хепаринот е крварење. Ризикот зависи од дозата и се зголемува со истовремена употреба на други антикоагулантни лекови. Како противотров може да се администрира протамин интравенски. Хепаринот може да доведе до т.н. хепарин индуцирана тромбоцитопенија. Противтелата против хепарин можат да доведат до крварење опасно по животот и формирање на тромби. Третманот подолг од четири недели може да предизвика мерливо намалување на густината на коските. До 2-3% од пациентите на долготраен третман со хепарин страдаат од остеопоротични вертебрални фрактури. Реверзибилно зголемување на трансаминазите е исто така вообичаено. Хепарините со ниска молекуларна тежина покажуваат помала фреквенција на овие несакани ефекти. Сепак, тие имаат понизок терапевтски ефект од хепаринот со подолг ланец поради нивниот помал ефект врз деактивирањето на тромбин.[9]
Контрола[уреди | уреди извор]
Кај пациентите кои добиваат нефракциониран хепарин (UFH), потребни се лабораториски контроли со мерење на парцијално тромбопластинско време (partial thromboplastin time, PTT) со цел да не се дава ниту преголема доза (ризик од крварење) ниту премала доза (ризик од тромбоза) на хепарин.
За нискомолекуларните хепарини обично не е потребна лабораториска контрола. Меѓутоа, доколку е потребно, точната доза може да се одреди со мерење на анти-Xa активноста. Мерењето мора да се изврши четири часа по супкутаната инјекција со цел за создавање на стандардизирани услови.[6]
Наводи[уреди | уреди извор]
- ↑ „Gebrauchsinformation Heparin AL Gel 30.000. (Memento vom 21. März 2014 im Internet Archive) (PDF; 43 kB) Aliud Pharma, April 2010“ (PDF). Архивирано од изворникот на 2014-03-21. Посетено на 2023-01-04.CS1-одржување: бот: непознат статус на изворната URL (link)
- ↑ „Heinz Lüllmann, Klaus Mohr: Pharmakologie und Toxikologie. Arzneimittelwirkungen verstehen – Medikamente gezielt einsetzen. 17. Auflage. Georg Thieme Verlag, 2010, ISBN 978-3-13-368517-7, S. 198“. Отсутно или празно
|url=(help) - ↑ Rietschel, Robert L.; Fowler, Joseph F.; Fisher, Alexander A. (2008). Fisher's Contact Dermatitis (англиски). PMPH-USA. стр. 142. ISBN 9781550093780. Архивирано од изворникот на 2017-09-10.
- ↑ „Heparin“. www.spektrum.de (германски). Посетено на 2023-01-04.
- ↑ „European Pharmacopoeia Commission (Hrsg.): European Pharmacopoeia 9.0. 2016, S. 2194 f.“. Наводот journal бара
|journal=(help) - ↑ 6,0 6,1 Mutschler, Ernst (2013). Mutschler Arzneimittelwirkungen : Lehrbuch der Pharmakologie und Toxikologie ; mit einführenden Kapiteln in die Anatomie, Physiologie und Pathophysiologie ; 264 Tabellen (10. Aufl. изд.). Stuttgart: Wiss. Verl.-Ges. ISBN 978-3-8047-2898-1. OCLC 816547684.
- ↑ „Eintrag zu Heparin. In: Pschyrembel Online, abgerufen am 2. Januar 2023“.
- ↑ „8 Inhibitors. Transfus Med Hemother. 2009;36(6):437-448. PMID: 21245974; PMCID: PMC2997298“.
- ↑ 9,0 9,1 Kozek-Langenecker, S. A.; Fries, D.; Gütl, M.; Hofmann, N.; Innerhofer, P.; Kneifl, W.; Neuner, L.; Perger, P.; Pernerstorfer, T. (2005-05). „Lokoregionalanästhesien unter gerinnungshemmender Medikation: Empfehlungen der Arbeitsgruppe Perioperative Gerinnung (AGPG) der Österreichischen Gesellschaft für Anästhesiologie und Intensivmedizin (ÖGARI)“. Der Anaesthesist (германски). 54 (5): 476–484. doi:10.1007/s00101-005-0827-0. ISSN 0003-2417. Проверете ги датумските вредности во:
|date=(help) - ↑ „[No title found]“. AINS - Anästhesiologie · Intensivmedizin · Notfallmedizin · Schmerztherapie (германски). 19 (04). doi:10.1055/s-002-23167. Проверете ја вредноста
|doi=(help). ISSN 0939-2661.
| ||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||
|
