Органометална хемија
Органометалната хемија се занимава со органските соединенија во кои се вклучени врски меѓу јаглероден и метален атом. Ваквите соединенија биле познати и се проучувале околу 200 години, а нивните единствени својства биле нашироко користени за одвивањето на синтетските трансформации. Во зависност од редукцискиот потенцијал на металот, реактивноста на органометалните соединенија значително варира, така што за подготовка и користење на најреактивното соединение требаат ниски до средни температури и инертни услови (атмосфера и растворувачи). Општо, реактивноста е паралелна со јонскиот карактер на јаглерод-метал врската, што може да се процени од преместувањето на протоните и јаглеродните атоми на метилните деривати:
% Јонски карактер на H3C - Метал (CH3)2Hg < (CH3)2Cd < (CH3)2Zn < (CH3)2Mg < CH3Li
Видови на органометални соединенија[уреди | уреди извор]
Првите пријавени органометални соединенија биле подготвени со редуктивна супституција на алкил халидите, како што е покажано во следните три равенки. Сите овие метали имаат силни или средни негативни редукциски потенцијали од кои литиумот и магнезиумот се најреактивни. Халидната реактивност се зголемува по редот: Cl < Br < I. Алкилнатриумовите и калиумовите соединенија не се подготвуваат на овој начин, бидејќи Вурцовото спарување на алкилната половина (давајќи R-R) претендира да предоминира. Ова може да биде проблем кога алил или бензил халидите се претвораат во Грињарови или литиумови реагенси.
- (алкил цинков реагенс), 1849, Е. Франкланд
- (Грињаров реагенс), 1900, Виктор Грињар
- (алкил литиумов реагенс), К. Циглер
Едноставните алкил деривати на сите три вида се пирофорни (спонтано горат на воздух) и реагираат со водата при што го даваат соодветниот алкан (RH); но, цинковите соединенија се помалку реактивни во друг поглед. Диетилцинкот може да се подготви и дестилира на заштитна атмосфера од CO2. Грињаровите и алкил литиумовите реагенси не се дестилабилни течности, и реагираат брзо со CO2 за да дадат соли на карбоксилните киселини.
Иако горните формули за алкил литиумовите и Грињаровите реагенси ја рефлектираат стехиометријата на реакциите и се користат нашироко во хемиската литература, тие не ја прикажуваат точно структурната природа на овие впечатливи супстанци. Смесите на полимерните и други асоцирани и комплексни соединенија се во рамнотежа под условите кои нормално се користат за нивна подготовка. На пример, едноставните алкил литиуми се големи хексамерни гроздови во јаглеводородни растворувачи, но се менуваат во тетрамерни и димерни форми во различни етерски растворувачи. За формацијата на Грињаровите реагенси е потребен етерски растворувач и тие се кристализирани како мономерни и димерни етерски комплекси. Следните рамнотежни соединенија (Шленкова рамнотежа) се идентификувани во етерски раствор:
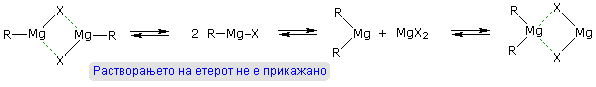
Бидејќи магнезиумовите халиди се средни Луисови киселини, нивното присуство во раствор може да влијае на текот на некои хемиски реакции. Еден пример за вакво растројување е реакцијата на циклохексан оксид со метилмагнезиум бромид, како што е прикажано десно во следната реакција. Магнезиум бромидот го прегрупира епоксидот во циклопентанкарбалдехид, кој потоа го адира Грињаровиот реагенс на очекуваниот начин. Диметилмагнезиумот, пак, едноставно се адира на епоксидот со отоврање на затегнатиот прстен. Метиллитиумот се адира на сличен начин.
Чистите диалкилмагнезиум реагенси можат да се подготват со алтернативни патишта или со отстранување на магнезиумовиот халид со таложење (се адира диоксан).

Реакции со метална замена[уреди | уреди извор]
Алтернативни методи на подготовка на голем број на органометални соединенија е со реакција на размена во која или даден метал се преместува на нова локација или се заменува со нов метал, како B, Al, Ti, V, Fe, Ni, Cu, Mo, Ru, Pd, Sn, Pt, Hg и Pb.
Поврзано[уреди | уреди извор]
| ||||||||||||||||||||||
|



