Гликолиза
Во метаболизмот, гликолизата е биохемиски пат со кој започнуваат процесите на ферментација и клеточно дишење. Всушност, гликолизата е процес при кој гликозата и фруктозата (кои имаат 6 С-атоми) се делат на две молекули со по 3 С-атоми познати како пирогроздова киселина (пируват). Со овој процес се добива енергија во форма на високоенергетското соединение АТР. Гликолизата е веројатно најстариот познат начин на производство на АТР. Постојат докази дека овој биохемиски пат постоел и пред појавата на кислородот во Земјината атмосфера и органелите во клетките. На ова укажуваат неколку факти:
- За одвивање на гликолизата не е потребен кислород. Таа е прва етапа во различните аеробни и анаеробни реакции за добивање на енергија
- Гликолизата се одвива во цитоплазмата на клетките, а не во некоја специјализирана органела
- Гликолизата е единствен метаболички (биохемиски) пат најден кај сите живи организми.
Краток преглед на гликолизата
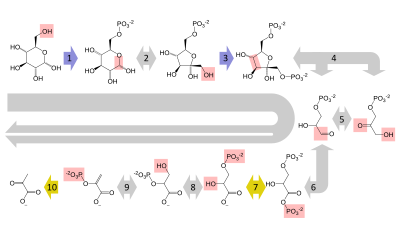
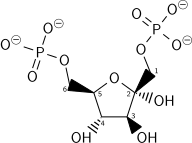
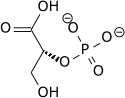
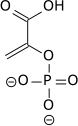
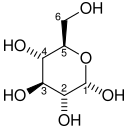
[уреди | уреди извор]Почетните и крајните учесници во гликолизата се:
| D-Гликоза | Пируват | ||||
|
2 NAD+ + 2 ADP + 2 Pi | 
|
2 | 
|
2 NADH + 2 H+ + 2 ATP + 2 H2O |
Сите производи имаат витални клеточни употреби:
- АТР е енергетски извор за многу клеточни функции.
- NADH + H+ дава редуцирачка моќ за други метаболички патишта или за понатамошна синтеза на АТР.
- Пируватот се користи во Кребсовиот циклус при аеробното дишење за производство на повеќе АТР или се претвора во други мали јаглеродни молекули при анаеробното дишење.
Реакции на гликолизата
[уреди | уреди извор]Фаза на енергетско инвестирање
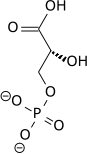
[уреди | уреди извор]Реакциите на гликолитичкиот метаболички пат се одвиваат во цитозолот на клетките. Гликозата влегува во гликолитичкиот пат претворена во гликоза-6-фосфат. Почетокот на процесот добива енергија од цепењето на две ~Р врски од АТР. Гликолизата се одвива во неколку етапи, односно фази:
|
||||||||||||||||||||
Хексокиназната реакција се состои од нуклеофилен напад на С6 хидроксилниот кислород на гликозата врз фосфорот од терминалниот фосфат на АТР. АТР се врзува за ензимот како комплекс со Mg++.
Позитивно наелектризираниот Mg++ стапува во интеракција со негативно наелектризираните фосфатокислородни атоми на АТР, овозможувајќи компензација на полнежите и давајќи поволна конформација на АТР на активниот центар на ензимот.
Реакцијата катализирана од хексокиназата е спонтана во голема мерка. Фосфоанхидридната врска на АТР (~Р) се цепи. Фосфатниот естер (гликоза-6-фосфат) има помал степен на хидролиза.
Гликозата која се сврзува за хексокиназата стабилизира конформација во која:
- С6 хидроксилот на врзаната гликоза е близу до терминалниот фосфат на АТР, со што ја овозможува катализата.
- Молекулата на водата не навлегува во активниот центар на ензимот. Ова го спречува ензимот да ја катализира хидролизата на АТР, а овозможува трансфер на фосфат до гликозата.
|
||||||||||||||||||||
Фосфогликозо изомеразниот механизам вклучува киселинско-базна катализа, со отворање на прстените, потоа изомеризација преку енедиолатен меѓупроизвод, а потоа затворање на прстенот.
|
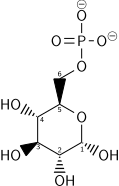
||||||||||||||||||||
Оваа високо спонтана реакција има механизам сличен со оној на хексокиназата. Фосфофруктокиназната реакција е ограничувачка етапа за степенот на гликолиза. Овој ензим е високо регулиран.
|
||||||||||||||||||||||||||
Алдолазната реакција се состои од делење на алдол, обратен процес од алдолна кондензација. Тука јаглеродните атоми добиваат нови бројни вредности во реакционите производи.
Остатокот од лизин на активниот центар на алдолазата делува при катализата. Кето-групата на фруктоза-1,6-бисфосфатот реагира со е-аминогрупата на лизинот и образува протониран меѓупроизвод - Шифова база. Потоа следи делење на врските помеѓу С3 и С4.
|
||||||||||||||||||||
Гликолизата продолжува од глицералдехид-3-фосфат. Константата на рамнотежа (Keq) за ТФИ реакцијата е во полза на дихидроксиацетон фосфат, но отстранувањето на глицералдехид-3-фосфатот од последователната спонтана реакција овозможува промена на истата.
Претворањето кетоза/алдоза на TФИ вклучува киселинско-базна катализа, и се претпоставува дека продолжува низ енедиолен меѓупроизвод, како во случајот со фосфогликозо изомеразата. Се мисли дека остатоците од Glu и His на активните центри на ензимот донираат протони за време на катализата.
2-фосфогликолатот е пример на преоден аналог кој се врзува за активниот центар на триоза фосфат изомеразата. Овој инхибитор на катализата со ТФИ е сличен во структурата со предложениот енедиолатен меѓупроизвод.
Фаза на енергетско генерирање
[уреди | уреди извор]
|
||||||||||||||||||||
Егзергонската оксидација на алдехидот глицералдехид-3-фосфат во карбоксилна киселина доведува до формација на ацил фосфат, високоенергетска врска (~Р) во 1,3-бисфосфоглицерат. Ова е единствениот чекор во гликолизата во кој NAD+ се редуцира до NADH.
Цистеински тиол на активниот центар на глицералдехид-3-фосфат дехидрогеназа има улога во катализата.
Глицералдехид-3-фосфатот реагира со цистеинскиот тиол и формира тиохемиацетален меѓупроизвод. Оксидацијата до карбоксилна киселина (во високоенергетски тиоестер) се случува, и NAD+ се редуцира до NADH.
Високоенергетскиот ацилен тиоестер е нападнат од Pi и дава ацил фосфатен (~Р) производ.
За потсетување, NAD+ прифаќа 2 e- и еден H+ (хидрид) кога се редуцира.
|
||||||||||||||||||||
Овој трансфер на фосфат до ADP, од карбоксилната група на 1,3-бисфосфоглицерат, е повратен бидејќи една ~Р врска се цепи, а друга се синтетизира. Ензинот подлежи на конформациона промена слична на онаа на хексокиназата.
|
||||||||||||||||||||
Фосфатот се преместува од хидроксилот на С3 од 3-фосфоглицератот на хидроксилот позициониран на С2.
Хистидинот од активниот центар на ензимот учествува во фосфатниот трансфер со донирање и прифаќање на фосфатот. Процесот го вклучува 2,3-бисфосфат како меѓупроизвод.
|
||||||||||||||||||||
Оваа дехидратациска реакција е зависна од Mg++. Два Mg++ јона стапуваат во интеракција со кислородните атоми на карбоксилната група на активниот центар. Овие јони помагаат да се стабилизира енолатниот анјонски меѓупроизвод кој се формира кога лизинската аминогрупа зема протон од С2.
|
||||||||||||||||||||
Овој трансфер на фосфат од ФЕП до ADP е спонтан. ФЕП има поголем степен на фосфатна хидролиза отколку АТР.
|