Аминокиселина
Аминокиселините се основните единици од кои се изградени белковините. Тие се аминодеривати на карбоксилните киселини и имаат општа формула:

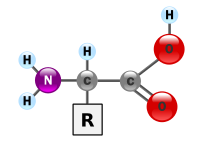
Од формулата се забележува дека секоја аминокиселина покрај остатокот R, содржи најмалку две функционални групи - една амино (лево) и една карбоксилна (десно) група. Фенилаланинот е една од стандардните аминокиселини:

Со оглед на структурата на аминокиселините, ги делиме на:
- моноаминокарбонски
- диаминокарбонски
- аминодикарбонски
- ароматски
- хетероциклични
Аминокиселините се структурни елементи на белковините во кои се поврзани со пептидна врска.
—NH—CO—.
Играат огромна улога во процесите на метаболизмот кај сите живи организми.
Наједноставна аминокиселина е глицин: H2N—CH2—COOH.
Во структурата на аминокиселините, аминогрупата во однос на карбоксилната група може да се наоѓа во различни положби. Во зависност од таа положба се разликуваат α, β, γ, δ итн. аминокиселини.
α-аминокиселини[уреди | уреди извор]
Сите пептиди и полипептиди (белковини) се полимери на α-аминокиселините. Постојат 20 α-аминокиселини кои се составен дел на белковините кај цицачите. Неколку други видови на аминокиселини се наоѓаат во телото како слободни соединенија или во комбинирана состојба (т.е. не се асоцирани со пептиди или белковини). Овие небелковински асоцирани аминокиселини имаат специјализирани функции. Еден дел од аминокиселините кои се составен дел на белковините исто така извршуваат и некои други функции, различни од образувањето на пептидите и белковините. На пример, тирозинот учествува во образувањето на тироидните хормони или, пак, глутаматот кој дејствува како невротрансмитер.
α-аминокиселините во пептидите и белковините (со исклучок на пролинот) се состојат од карбоксилна киселина, односно група (-COOH) и амино (-NH2) функционална група сврзани за истиот тетраедарски јаглероден атом. Овој атом се означува како α-јаглероден атом (оттука и α-аминокиселини). Одделни R-групи, со кои една аминокиселина се разликува од друга, се исто така сврзани за α-јаглеродот (со исклучок на глицинот, каде R-групата е водород). Четвртиот супституент прикачен за тетраедарскиот α-јаглерод кај аминокиселините е водородот.
Список на аминокиселини[уреди | уреди извор]
| Аминокиселина | Со 3 букви | Со 1 буква | Поларност | Киселост или базност |
|---|---|---|---|---|
| аланин | ala | A | неполарна | неутрална |
| аргинин | arg | R | поларна | силно базна |
| аспарагин | asn | N | поларна | неутрална |
| аспарагинска киселина | asp | D | поларна | кисела |
| аспарагин или аспартичка киселина* | asx | B | ||
| цистеин | cys | C | неполарна | неутрална |
| глутамат | glu | E | поларна | кисела |
| глутамин | gln | Q | поларна | неутрална |
| глутамин или глутамска киселина* | glx | Z | ||
| глицин | gly | G | неполарна | неутрална |
| хистидин | his | H | поларна | слабо базна |
| изолеуцин | ile | I | неполарна | неутрална |
| леуцин | leu | L | неполарна | неутрална |
| лизин | lys | K | поларна | базна |
| метионин | met | M | неполарна | неутрална |
| фенилаланин | phe | F | неполарна | неутрална |
| пролин | pro | P | неполарна | неутрална |
| серин | ser | S | поларна | неутрална |
| треонин | thr | T | поларна | неутрална |
| триптофан | trp | W | неполарна | неутрална |
| тирозин | tyr | Y | поларна | неутрална |
| валин | val | V | неполарна | неутрална |
Класификација на α-аминокиселините[уреди | уреди извор]
Секоја од дваесетте α-аминокиселини најдени во белковините можат да се разликуваат по R-групата (R-супституентот) на α-јаглеродот. Постојат две големи класи на аминокиселини чија поделба се основа на тоа дали R-групата е хидрофобна или хидрофилна.
Хидрофобните аминокиселини неможат да опстојат во водна средина и затоа најмногу се наоѓаат во внатрешноста на белковините. Оваа класа на аминокиселини не јонизира, ниту пак учествува во образувањето на водородни врски. Хидрофилните аминокиселини стапуваат во заемодејства со водната средина и често учествуваат во образувањето на водородни врски. Тие најчесто се наоѓаат на надворешните површини на белковинитеили во реактивните центри на ензимите.
Киселинско-базни својства на аминокиселините[уреди | уреди извор]
α-СООН и α-NH2 групите во аминокиселините се способни за јонизација (како што се и киселите и базни R-групи). Како резултат на нивната јонизациона способност, можат да се напишат следните реакции на јонска рамнотежа:
- и
Рамнотежните реакции, како што се напишани, покажуваат дека аминокиселините содржат барем две послаби кисели групи. Но, карбоксилната група е далеку посилна киселина отколку аминогрупата. При физиолошка pH-вредност (околу 7,4), карбоксилната група ќе биде депротонирана и аминогрупата ќе се протонира (ќе прими протон). Аминокиселина со R-група која не е способна за јонизација ќе биде електронеутрална при оваа pH-вредност. Ваквиот комплекс се нарекува цвитерјон.

Како и типичните органски киселини, киселинската сила на карбоксилната, амино и јонизационо способните R-групи во аминокиселините можат да се дефинираат со константата на асоцијација Ka, или поконкретно негативниот логаритам на Ka, pKa. Вкупниот полнеж (алгебарскиот збир на сите присутни наелектризирани групи) на било која аминокиселина, пептид или белковина, ќе зависи од pH на околната водна средина. Како што се менува pH на растворот од аминокиселини или белковини, така се менува и вкупниот полнеж. Овој феномен може да се набљудува за време на титрацијата на секоја аминокиселина или белковина. Кога вкупниот полнеж на една аминокиселина или белковина е нула, тогаш pH ќе биде еднаква на изоелектричната точка (pI).
Функционално значење на R-групите од аминокиселините[уреди | уреди извор]
Во раствор, сосема типично е што R-групите од аминокиселините ја диктираат структурно-функционалната поврзаност на пептиидте и белковините. Хидрофобните аминокиселини главно ќе се соберат во внатрешноста на белковините, заштитени од директниот контакт со водата. Обратно, хидрофилните аминокиселини главно се наоѓаат во надворешноста на белковините, како и во активните центри на ензимски активните белковини. Всушност, некои ензимски реакции се случуваат токму како резултат на присуството на R-групите.
Имидазолниот прстен на хистидинот овозможува тој да дејствува и како протон-дарител, и како протон-акцептор при физиолошка pH-вредност. Значи, тој често се наоѓа во реактивните центри на ензимите. Еднакво важна е и можноста на хистидинот во хемоглобинот да ги оттргнува H+ јоните при јонизацијата на јаглеродната киселина во еритроцитите. Токму како резултат на ова, хемоглобинот врши размена на гасови во ткивата и белите дробови.
Првичниот алкохол на серинот и треонинот, како и тиолот (-SH) на цистеинот им дозволуваат на овие аминокиселини да дејствуваат како нуклеофили за време на катализата. Додатно, тиолот од цистеинот е способен да образува дисулфидна врска со други цистеини:
Овој прост дисулфид е означен како цистин. Образувањето на дисулфидни врски помеѓу цистеините присутни во белковините е важно за образувањето на активни структурни домени кај голем број на белковини. Дисулфидното поврзување помеѓу цистеините во различни полипептидни ланци на олигомерни белковини игра значајна улога во уредувањето на структурата на комплексните белковини, како на пример, инсулинските рецептори.
Оптички својства на аминокиселините[уреди | уреди извор]

Тетраедарскиот јаглероден атом за кој се сврзани 4 различни супституенти се нарекува хирален C-атом. Единствената аминокиселина кај која не се среќава хиралност е глицинот, бидејќи неговата "R-група" е водороден атом. Хиралноста ја опишува способноста на дадена молекула да ја врти рамнината на поларизираната светлина на десно (декстроротаторно) или, пак, на лево (леворотаторно). Сите белковински аминокиселини ја даваат истата апсолутна стеричка конфигурација како јаглехидратот L-глицералдехид. Поради тоа тие се L-α-аминокиселини. D-α-аминокиселини не се најдени никогаш во белковините, иако постојат во природата. D-аминокиселините најчесто се наоѓаат во полипептидните антибиотици.
Ароматичните R-групи во аминокиселините апсорбираат ултравиолетова светлина со апсорпциски максимум од 280 nm. Можноста на белковините да ја апсорбираат ултравиолетовата светлина е главно резултат на присуството на триптофанот кој силно ја апсорбира истата.
Пептидна врска[уреди | уреди извор]
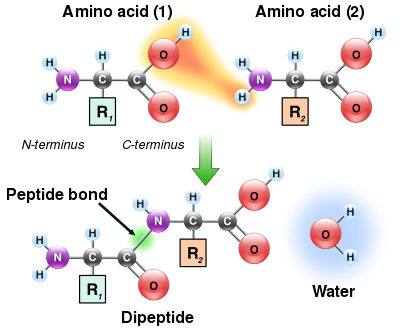
Образувањето на пептидна врска е реакција на кондензација која доведува до полимеризација на аминокиселините во пептиди и белковини. Пептидите се мали и се состојат од неколку аминокиселини. Некои хормони и невротрансмитери се пептиди. Исто така, неколку антибиотици и антитуморни агенси се пептиди. Белковините се полипептиди со голема молекулска маса. Најпростиот пептид (дипептид) се состои од една пептидна врска која се образува со кондензација на карбоксилната група на една аминокиселина со аминогрупата на втората аминокиселина, притоа одделувајќи една молекула на вода. Присуството на карбонилната група во пептидната врска овозможува електронско-резонантна стабилизација, таква што не дозволува слободна ротација околу самата пептидна врска, што е нетипично за другите двојни врски -C=C-. Се вели дека пептидната (или амидна) врска има делумен двоен карактер.
| ||||||||||||||||||||||||||||||
|




